Clear Sky Science · ru
TPTE, тестикуло-специфический член семейства PTEN, управляет сперматогенезом через синтез PI(4,5)P2
Почему это важно для мужской фертильности
Многие пары, испытывающие трудности с зачатием, так и не получают ясного ответа на вопрос, почему сперматозоидов мало или они плохо двигаются. В этом исследовании выявлен ранее малоизвестный тестикуло-специфический фермент TPTE, который участвует и в генетическом перемешивании предшественников сперматозоидов, и в построении их хлыстовидных хвостов. Показав, как TPTE влияет на ключевые сигнальные липиды в развивающихся сперматозоидах, работа даёт новые молекулярные объяснения некоторым формам мужского бесплодия и указывает пути для будущей диагностики и терапии.
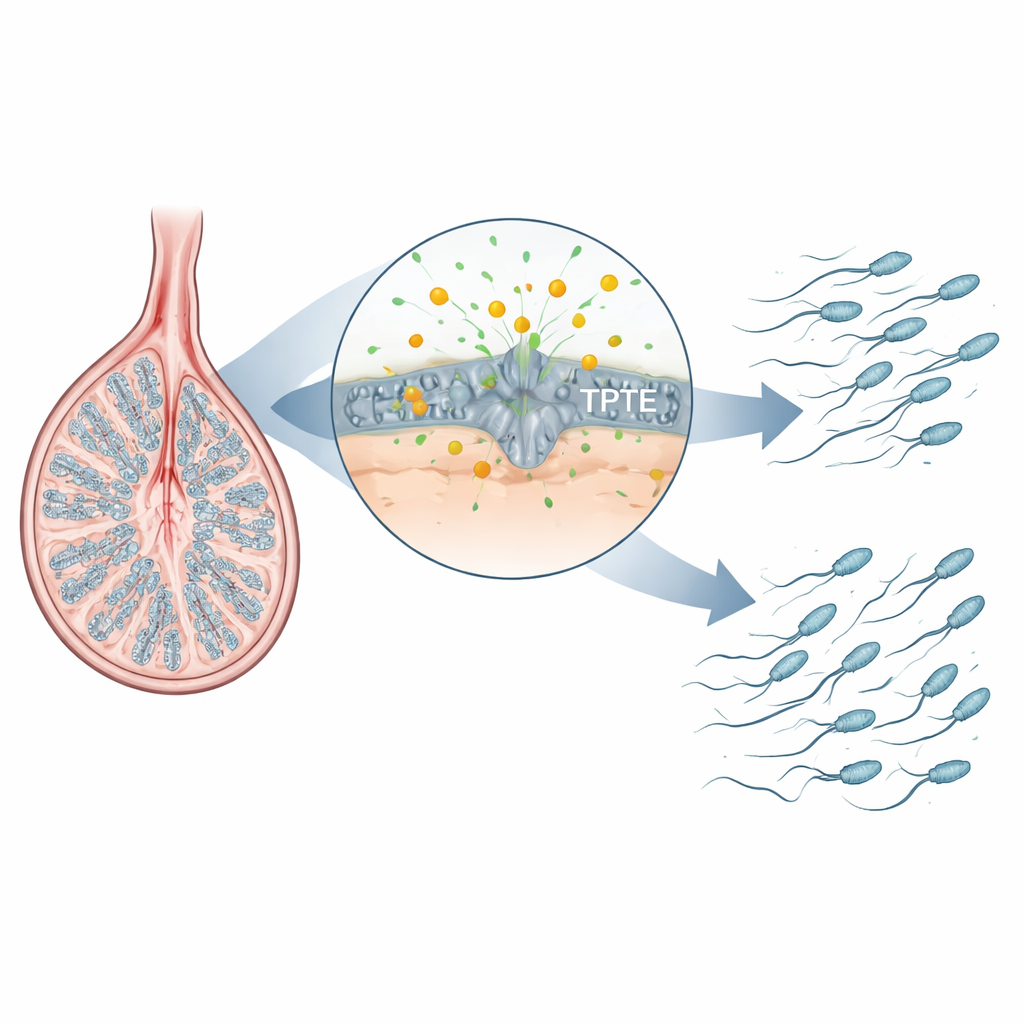
Скрытый помощник в развитии сперматозоидов
Сперматозоиды формируются в тестисе в строго организованной последовательности: стволовые клетки делятся, их потомки проходят мейоз с перестройкой ДНК, а затем округлые клетки преобразуются в обтекаемые, хвостовые сперматозоиды. Авторы сосредоточились на семействе ферментов, перерабатывающих жирные сигнальные молекулы в мембранах. Один из известных членов, PTEN, важен во многих тканях, но не обязателен для финальных этапов сперматогенеза. TPTE же синтезируется почти исключительно в герминативных клетках тестиса, и его функция была плохо изучена. Отслеживая распределение ключевого мембранного липида PI(4,5)P2 в семенниках мышей, исследователи обнаружили его обогащение в сперматоцитах и сперматидах — именно на этапах ремонта хромосом и сборки хвостов — что указывает на возможную критическую роль TPTE и этого липида в формировании здоровых сперматозоидов.
Связь утраты TPTE с плохими сперматозоидами и мужским бесплодием у людей
Команда сначала проверила, изменён ли TPTE у мужчин с тяжёлым бесплодием. Переанализировав общедоступные данные РНК-секвенирования из биопсий тестикул, они обнаружили резкое снижение уровня TPTE у пациентов с необструктивной азооспермией и других состояний, характеризующихся повреждением или истощением герминативных клеток. Чтобы проверить причинно-следственную связь, они удалили ген Tpte у мышей с помощью редактирования генома. Самцы без TPTE давали значительно меньшие помёты при нормальном размере яичек. В их эпидидимисах содержалось меньше сперматозоидов, а компьютерный анализ показал снижение подвижности и прогрессивного движения. При микроскопии многие сперматозоиды имели нормальные овальные головки, но свернутые или сложенные хвосты, что говорит о том, что TPTE не обязателен для формирования головки, но необходим для поддержания числа сперматозоидов и формирования функциональных хвостов.
Защита ремонта ДНК во время мейоза
Чтобы понять, почему падало число сперматозоидов, исследователи сосредоточились на мейозе, где хромосомы обмениваются участками через строго контролируемые разрывы и их последующий ремонт. В тестикулрах, лишённых TPTE, общая картина стадий герминативных клеток была похожа, но количество клеток начало снижаться на стадии диплотеновых сперматоцитов, и наблюдался всплеск гибели клеток, застревавших в метафазе I. Расположения хромосом показали дефекты в «лестничных» структурах, обеспечивающих выравнивание парных хромосом, а маркер разрывов ДНК γ-H2AX аномально сохранялся на аутосомах, указывая на неполный ремонт. Меньше формировалось фокусов белков RPA2 и DMC1 в местах разрывов. Молекулярный анализ показал гиперактивацию ключевого пути роста AKT/mTOR при отсутствии TPTE, сопутствовавшую снижению уровня RAD50 — основного компонента, инициирующего ремонт двунитевых разрывов. В совокупности эти данные свидетельствуют о том, что TPTE обычно продуцирует PI(4,5)P2, чтобы сдерживать активность AKT/mTOR, поддерживать уровни RAD50 и позволять протекать мейотическому ремонту ДНК, тем самым охраняя пополнение жизнеспособных сперматидов.
Построение прочных хвостов за счёт контроля белкового синтеза
TPTE также оказался важен на позднем этапе, когда округлые сперматиды перестраиваются в обтекаемые подвижные сперматозоиды. Электронная микроскопия хвостов сперматозоидов без TPTE показала несколько аксонемных поперечных сечений, застрявших в одной мембране, нарушение «9+2» микротрубочковой организации и деформацию поддерживающих волокон. Окрашивание компонентов хвоста, таких как ацетилированный тубулин и внешний плотный волоконный белок ODF2, выявило неравномерные, ослабленные структуры, а более удлинённые сперматиды чаще подвергались гибели в тестисе. Окраска липидов показала заметное уменьшение и неравномерное распределение PI(4,5)P2 вдоль жгутиков при отсутствии TPTE. Чтобы проследить, как это нарушение отражается на белковом аппарате клетки, авторы провели количественный протеомный анализ изолированных округлых сперматидов. Сотни белков, включая несколько компонентов рибосом, были повышены, а рибосомная профилировка показала усиление полисомной активности — признак повышенного трансляционного уровня. Среди них особенно отметили PDLIM1, известный тормоз организации микротрубочек: его уровень белка резко возрос без изменений в мРНК, а его трансплантаты (транскрипты) сместились в тяжёлые полисомные фракции, указывая на избыточную трансляцию. Эта картина снова восходит к чрезмерной активности AKT/mTOR, вызванной изменением липидного баланса при отсутствии TPTE.
Что это значит для понимания мужского бесплодия
Вместе взятые, результаты описывают TPTE как хранителя герминативных клеток, который регулирует мембранные липиды, чтобы сдерживать сигнальный путь AKT/mTOR, обеспечивая правильный ремонт ДНК и упорядоченный белковый синтез. Когда TPTE отсутствует или его уровни снижены, как это наблюдалось в ряде типов инфертильных человеческих тестикул, разрывы ДНК в мейозе не устраняются должным образом, часть развивающихся сперматозоидов погибает, а выжившие часто имеют структурно дефектные хвосты и плохо плавают. Для неспециалистов главный вывод таков: мужская фертильность зависит не только от уровня гормонов и числа сперматозоидов, но и от тонких молекулярных регуляторов, подобных TPTE, которые координируют генетическую целостность и архитектуру хвоста. В будущем скрининг TPTE и связанных с ним путей может помочь выявлять скрытые причины мужского бесплодия и вдохновить на разработку целевых терапий, восстанавливающих сбалансированную передачу сигналов в тестисе.
Цитирование: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Ключевые слова: мужское бесплодие, сперматогенез, подвижность сперматозоидов, передача сигналов, тестикуло-специфические гены