Clear Sky Science · es
TPTE, un miembro de la familia PTEN específico del testículo, impulsa la espermatogénesis mediante la síntesis de PI(4,5)P2
Por qué importa para la fertilidad masculina
Muchas parejas que tienen dificultades para concebir nunca obtienen una respuesta clara sobre por qué hay pocos espermatozoides o por qué se mueven mal. Este estudio desvela una enzima específica del testículo hasta ahora enigmática, llamada TPTE, que ayuda tanto a guiar la reorganización genética de los precursores espermáticos como a construir sus colas en forma de látigo. Al mostrar cómo TPTE moldea moléculas de señalización clave dentro de los espermatozoides en desarrollo, la investigación aporta nuevas explicaciones moleculares para ciertas formas de infertilidad masculina y sugiere vías futuras para el diagnóstico y el tratamiento.
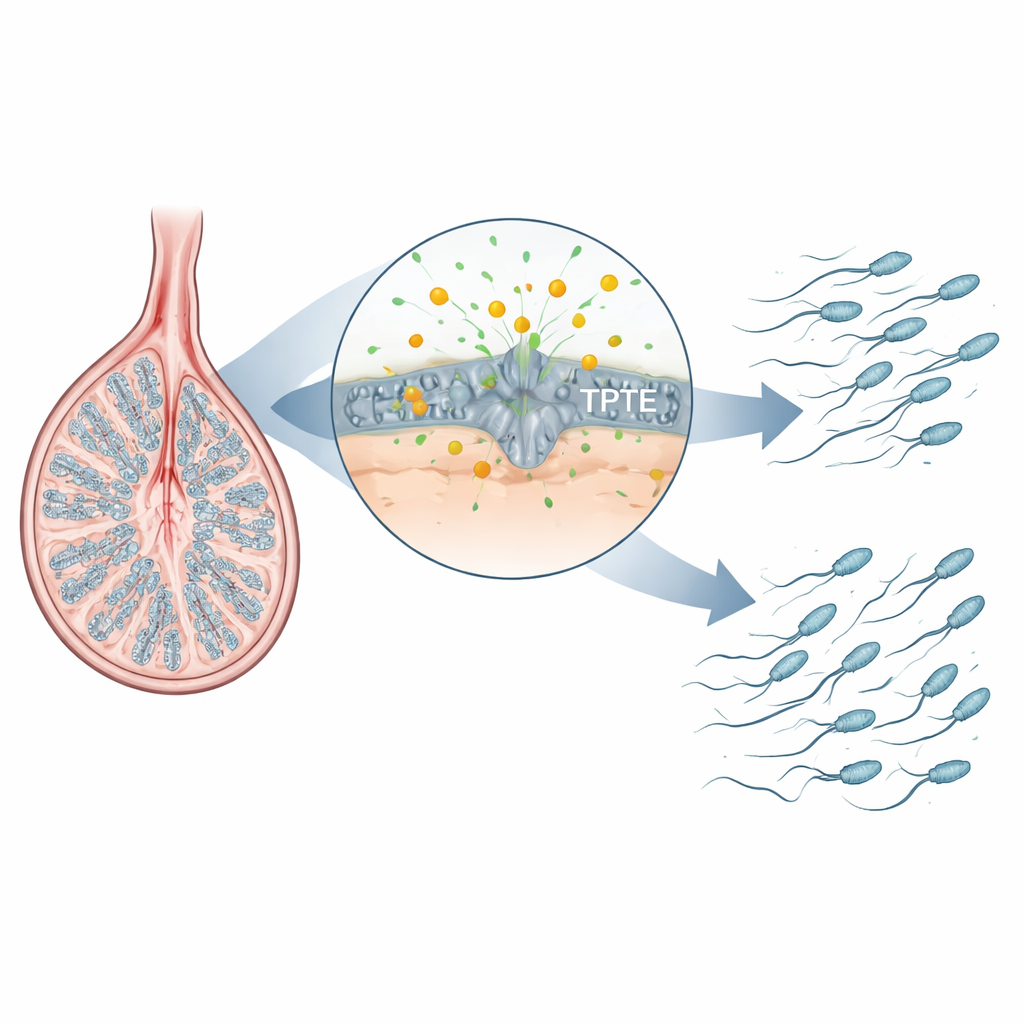
Un ayudante oculto en el desarrollo espermático
Los espermatozoides se forman en una secuencia estrictamente coreografiada de pasos dentro del testículo: las células madre se dividen, sus descendientes reorganizan el ADN durante la meiosis y las células redondas resultantes se remodelan en espermatozoides estilizados con cola. Los autores se centraron en una familia de enzimas que procesan lípidos de señalización en las membranas celulares. Un miembro bien conocido, PTEN, es importante en muchos tejidos pero no es esencial para las etapas finales del desarrollo espermático. TPTE, sin embargo, se produce casi exclusivamente en las células germinales del testículo, y su actividad se conocía poco. Al mapear dónde aparece un lípido de membrana clave, PI(4,5)P2, en testículos de ratón, los investigadores encontraron que está especialmente enriquecido en espermatocitos y espermátidas, las etapas en las que se reparan los cromosomas y se ensamblan las colas, lo que sugiere que TPTE y este lípido podrían ser críticos para la formación sana de esperma.
Vinculando la pérdida de TPTE con esperma de mala calidad y la infertilidad humana
El equipo preguntó primero si TPTE está alterado en hombres con infertilidad severa. Reanalizando datos públicos de secuenciación de ARN de biopsias testiculares, hallaron que los niveles de TPTE están notablemente reducidos en pacientes con azoospermia no obstructiva y otras condiciones marcadas por células germinales dañadas o agotadas. Para explorar causalidad, eliminaron el gen Tpte en ratones mediante edición genómica. Los machos sin TPTE produjeron camadas mucho más pequeñas a pesar de tener un tamaño testicular normal. Sus epidídimos contenían menos espermatozoides, y el análisis asistido por ordenador mostró motilidad reducida y menor natación progresiva. Al microscopio, muchos espermatozoides tenían cabezas normales, ovaladas, pero colas rizadas o plegadas, lo que sugiere que TPTE no es imprescindible para formar la cabeza pero sí crucial para mantener el número de espermatozoides y esculpir colas funcionales.
Protegiendo la reparación del ADN durante la meiosis
Para entender por qué caían los recuentos de espermatozoides, los investigadores se centraron en la meiosis, donde los cromosomas intercambian segmentos mediante roturas y reparaciones de ADN cuidadosamente controladas. En testículos deficientes en TPTE, la organización general de las etapas de las células germinales parecía similar, pero el número de células comenzó a disminuir en la etapa de espermatocito diploteno, y hubo un aumento de células moribundas atrapadas en metafase I. Extensiones cromosómicas revelaron defectos en la estructura en escalera que permite alinear cromosomas apareados, y un marcador de roturas de ADN, γ-H2AX, persistió de forma anormal en los autosomas, indicando reparaciones incompletas. Se formaron menos focos de las proteínas RPA2 y DMC1 en los sitios de rotura. El análisis molecular señaló una sobreactivación de la vía central de crecimiento AKT/mTOR en ausencia de TPTE, acompañada de niveles reducidos de RAD50, un componente esencial que inicia la reparación de roturas de doble hebra. En conjunto, estos hallazgos sugieren que TPTE normalmente genera PI(4,5)P2 para mantener la actividad de AKT/mTOR bajo control, preservando los niveles de RAD50 y permitiendo que la reparación del ADN en meiosis avance, salvaguardando así el suministro de espermátidas viables.
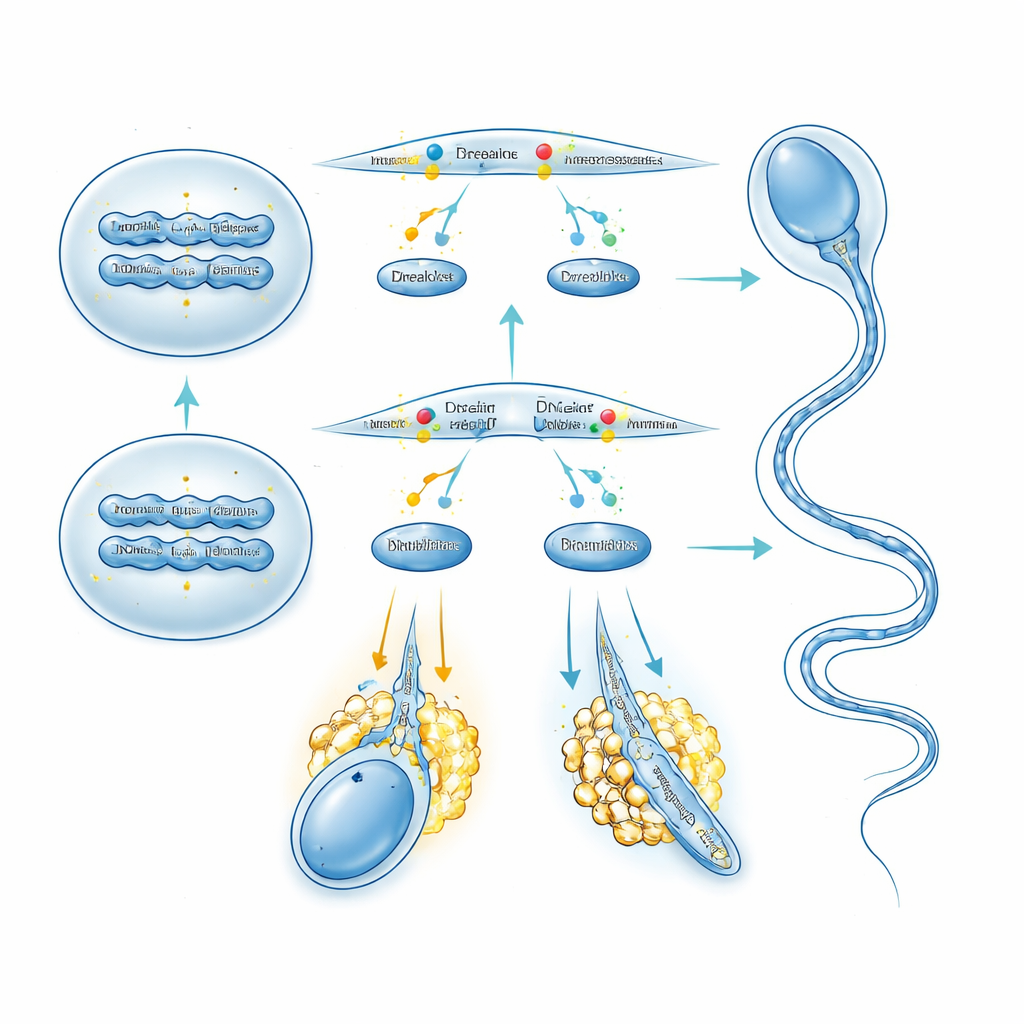
Construir colas fuertes mediante el control de la producción proteica
TPTE también resultó vital para la remodelación tardía de las espermátidas redondas en espermatozoides aerodinámicos y móviles. La microscopía electrónica de las colas de espermatozoides sin TPTE mostró múltiples secciones transversales del axonema atrapadas en una sola membrana y disposiciones de microtúbulos “9+2” alteradas, junto con fibras de soporte malformadas. La tinción de componentes de la cola como la tubulina acetilada y la proteína de la fibra densa externa ODF2 reveló estructuras parcheadas y debilitadas, y más espermátidas alargadas sufrieron muerte celular en el testículo. La tinción lipídica mostró que PI(4,5)P2 estaba marcadamente reducida y distribuida de forma desigual a lo largo de los flagelos cuando faltaba TPTE. Para ver cómo esta alteración afectaba la maquinaria de síntesis de proteínas de la célula, los autores realizaron proteómica cuantitativa en espermátidas redondas aisladas. Cientos de proteínas, incluidos varios componentes ribosómicos, estaban regulados al alza, y el perfilado de ribosomas indicó una mayor actividad de polisomas, signo de traducción aumentada. Entre estas proteínas, el equipo destacó PDLIM1, un conocido freno de la organización de microtúbulos: sus niveles proteicos se dispararon sin un cambio en su ARN mensajero, y sus transcritos se desplazaron a fracciones de polisomas pesados, lo que indica sobretraducción. Este patrón nuevamente se vinculó a la sobreactivación de AKT/mTOR desencadenada por el desequilibrio lipídico cuando falta TPTE.
Qué significa esto para entender la infertilidad masculina
En conjunto, el estudio retrata a TPTE como un guardián de las células germinales que ajusta los lípidos de membrana para contener la señalización AKT/mTOR, permitiendo una reparación correcta del ADN y una síntesis proteica ordenada. Cuando TPTE falta o se reduce, como se observa en varios tipos de testículos infértiles humanos, las roturas de ADN en la meiosis no se resuelven adecuadamente, algunas células espermáticas en desarrollo mueren y las que sobreviven a menudo presentan colas estructuralmente defectuosas que nadan mal. Para los no especialistas, el mensaje clave es que la fertilidad masculina depende no solo de los niveles hormonales y del recuento de espermatozoides, sino también de reguladores moleculares sutiles como TPTE que coordinan la integridad genética y la arquitectura de la cola. En el futuro, evaluar TPTE y sus socios en la vía podría ayudar a identificar causas ocultas de la infertilidad masculina e inspirar terapias dirigidas que restauren el equilibrio de la señalización en el testículo.
Cita: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Palabras clave: infertilidad masculina, espermatogénesis, motilidad espermática, transducción de señales, genes específicos del testículo