Clear Sky Science · pt
TPTE, um membro da família PTEN específico do testículo, dirige a espermatogênese via síntese de PI(4,5)P2
Por que isso importa para a fertilidade masculina
Muitos casais que têm dificuldade para conceber nunca recebem uma resposta clara sobre por que os espermatozoides são escassos ou se movem mal. Este estudo desvenda uma enzima específica do testículo antes pouco compreendida, chamada TPTE, que ajuda a orientar tanto o rearranjo genético dos precursores dos espermatozoides quanto a construção de suas caudas em forma de chicote. Ao mostrar como a TPTE molda moléculas de sinalização chave dentro de espermatozoides em desenvolvimento, a pesquisa aponta novas explicações moleculares para certas formas de infertilidade masculina e sugere caminhos futuros para diagnóstico e tratamento.
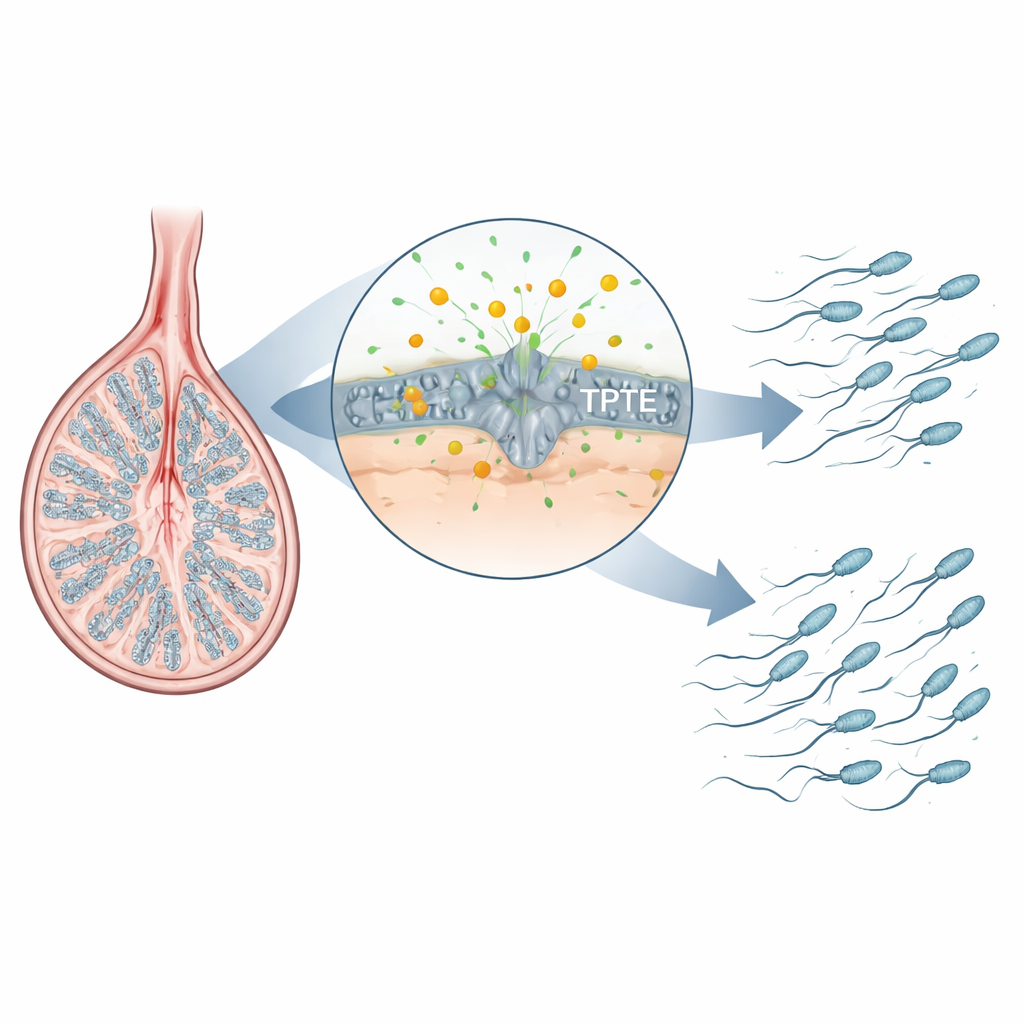
Um ajudante oculto no desenvolvimento dos espermatozoides
Os espermatozoides são formados em uma sequência rigorosamente coreografada de etapas dentro do testículo: células-tronco dividem-se, seus descendentes reordenam o DNA durante a meiose, e as células arredondadas resultantes se remodelam em espermatozoides alongados com cauda. Os autores focalizaram uma família de enzimas que processam lipídios de sinalização nas membranas celulares. Um membro bem conhecido, PTEN, é importante em muitos tecidos, mas não é essencial para as fases finais do desenvolvimento espermático. A TPTE, entretanto, é produzida quase exclusivamente em células germinativas do testículo, e sua atividade era pouco compreendida. Ao mapear onde um lipídio de membrana chave, PI(4,5)P2, aparece em testículos de camundongo, os pesquisadores descobriram que ele está especialmente enriquecido em espermatócitos e espermátides — as próprias fases em que os cromossomos são reparados e as caudas são montadas — sugerindo que TPTE e esse lipídio podem ser críticos para a formação saudável dos espermatozoides.
Ligando a perda de TPTE a espermatozoides ruins e infertilidade humana
A equipe primeiro investigou se a TPTE está alterada em homens com infertilidade severa. Ao reanalisar dados públicos de sequenciamento de RNA de biópsias testiculares, encontraram níveis de TPTE fortemente reduzidos em pacientes com azoospermia não obstrutiva e outras condições marcadas por células germinativas danificadas ou esgotadas. Para sondar causa e efeito, deletaram o gene Tpte em camundongos usando edição genômica. Machos sem TPTE geraram ninhadas muito menores apesar de tamanho testicular normal. Seus epidídimos continham menos espermatozoides, e análises assistidas por computador mostraram motilidade reduzida e natação progressiva prejudicada. Ao microscópio, muitos espermatozoides tinham cabeças normais e ovais, mas caudas enroladas ou dobradas, sugerindo que TPTE é dispensável para formar a cabeça, porém crucial para manter o número de espermatozoides e esculpir caudas funcionais.
Protegendo o reparo do DNA durante a meiose
Para entender por que os números de espermatozoides caíram, os pesquisadores concentraram-se na meiose, onde os cromossomos trocam segmentos por meio de quebras e reparos de DNA precisamente controlados. Em testículos deficientes em TPTE, a organização geral dos estágios das células germinativas parecia semelhante, mas as contagens celulares começaram a cair no estágio de espermatócito diplóteno, e houve um aumento de células morrendo presas na metáfase I. Preparações cromossômicas revelaram defeitos na estrutura em “escada” que permite o pareamento dos cromossomos, e um marcador de quebras de DNA, γ-H2AX, permaneceu anormalmente nos autossomos, indicando reparo incompleto. Houve menos focos dos auxiliadores de ligação ao DNA RPA2 e DMC1 nos sítios de quebra. Análises moleculares apontaram para sobreativação de uma via central de crescimento, AKT/mTOR, na ausência de TPTE, acompanhada por níveis reduzidos de RAD50, um componente central que inicia o reparo de quebras de fita dupla. Juntos, esses achados sugerem que a TPTE normalmente gera PI(4,5)P2 para manter a atividade AKT/mTOR sob controle, preservando os níveis de RAD50 e permitindo que o reparo meiótico do DNA prossiga, protegendo assim o suprimento de espermátides viáveis.
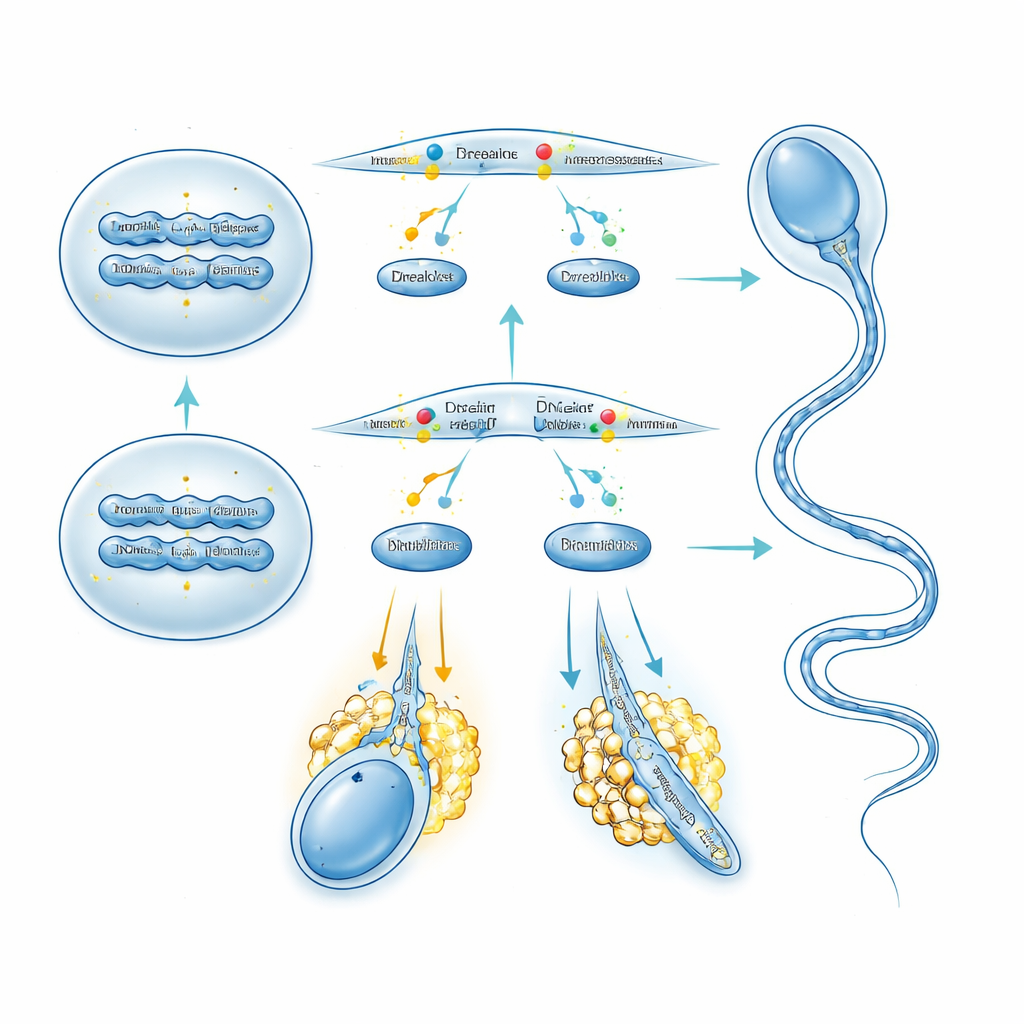
Construindo caudas fortes por meio do controle da produção de proteínas
A TPTE também se mostrou vital para o remodelamento posterior de espermátides arredondadas em espermatozoides aerodinâmicos e móveis. Microscopia eletrônica das caudas de espermatozoides sem TPTE mostrou múltiplas seções transversais do axonema aprisionadas em uma única membrana e arranjos “9+2” de microtúbulos perturbados, junto com fibras de suporte malformadas. Marcação de componentes da cauda, como tubulina acetilada e a proteína da fibra densa externa ODF2, revelou estruturas irregulares e enfraquecidas, e espermátides mais alongadas sofreram morte celular no testículo. Colorações lipídicas mostraram que PI(4,5)P2 estava marcadamente reduzido e distribuído de forma desigual ao longo dos flagelos quando TPTE estava ausente. Para ver como essa perturbação reverberava na maquinaria de síntese proteica da célula, os autores realizaram proteômica quantitativa em espermátides arredondadas isoladas. Centenas de proteínas, incluindo vários componentes ribossomais, foram reguladas para cima, e o mapeamento de ribossomos indicou atividade de polissomos aumentada, sinal de tradução elevada. Entre elas, o grupo destacou PDLIM1, um freio conhecido na organização de microtúbulos: seus níveis proteicos aumentaram acentuadamente sem mudança em seu RNA mensageiro, e seus transcritos deslocaram-se para frações pesadas de polissomos, indicando tradução excessiva. Esse padrão novamente remeteu à sinalização AKT/mTOR excessiva desencadeada pelo equilíbrio lipídico alterado quando TPTE está ausente.
O que isso significa para entender a infertilidade masculina
Em conjunto, o estudo retrata a TPTE como uma guardiã das células germinativas que ajusta lipídios de membrana para frear a sinalização AKT/mTOR, permitindo reparo adequado do DNA e síntese proteica ordenada. Quando a TPTE está ausente ou reduzida, como observado em vários tipos de testículos inférteis humanos, quebras de DNA na meiose não são resolvidas corretamente, alguns espermatozoides em desenvolvimento morrem, e os sobreviventes frequentemente emergem com caudas estruturalmente defeituosas que nadam mal. Para não especialistas, a mensagem principal é que a fertilidade masculina depende não apenas de níveis hormonais e contagem de espermatozoides, mas também de reguladores moleculares sutis como a TPTE que coordenam integridade genética e arquitetura da cauda. No futuro, rastrear a TPTE e seus parceiros de via pode ajudar a identificar causas ocultas de infertilidade masculina e inspirar terapias direcionadas para restaurar o equilíbrio da sinalização no testículo.
Citação: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Palavras-chave: infertilidade masculina, espermatogênese, motilidade espermática, transdução de sinal, genes específicos do testículo