Clear Sky Science · pl
TPTE, specyficzny dla jądra członek rodziny PTEN, napędza spermatogenezę przez syntezę PI(4,5)P2
Dlaczego to ma znaczenie dla męskiej płodności
Wiele par borykających się z zajściem w ciążę nigdy nie otrzymuje jasnej odpowiedzi, dlaczego plemników jest mało lub poruszają się słabo. To badanie odsłania wcześniej tajemniczy enzym specyficzny dla jądra, nazwany TPTE, który pomaga zarówno w kierowaniu genetycznym przestawianiem prekursorów plemników, jak i w budowie ich biczykowatych wici. Pokazując, jak TPTE kształtuje kluczowe cząsteczki sygnałowe wewnątrz rozwijających się plemników, praca wskazuje nowe molekularne wyjaśnienia pewnych form męskiej niepłodności i sugeruje przyszłe kierunki diagnostyki oraz terapii.
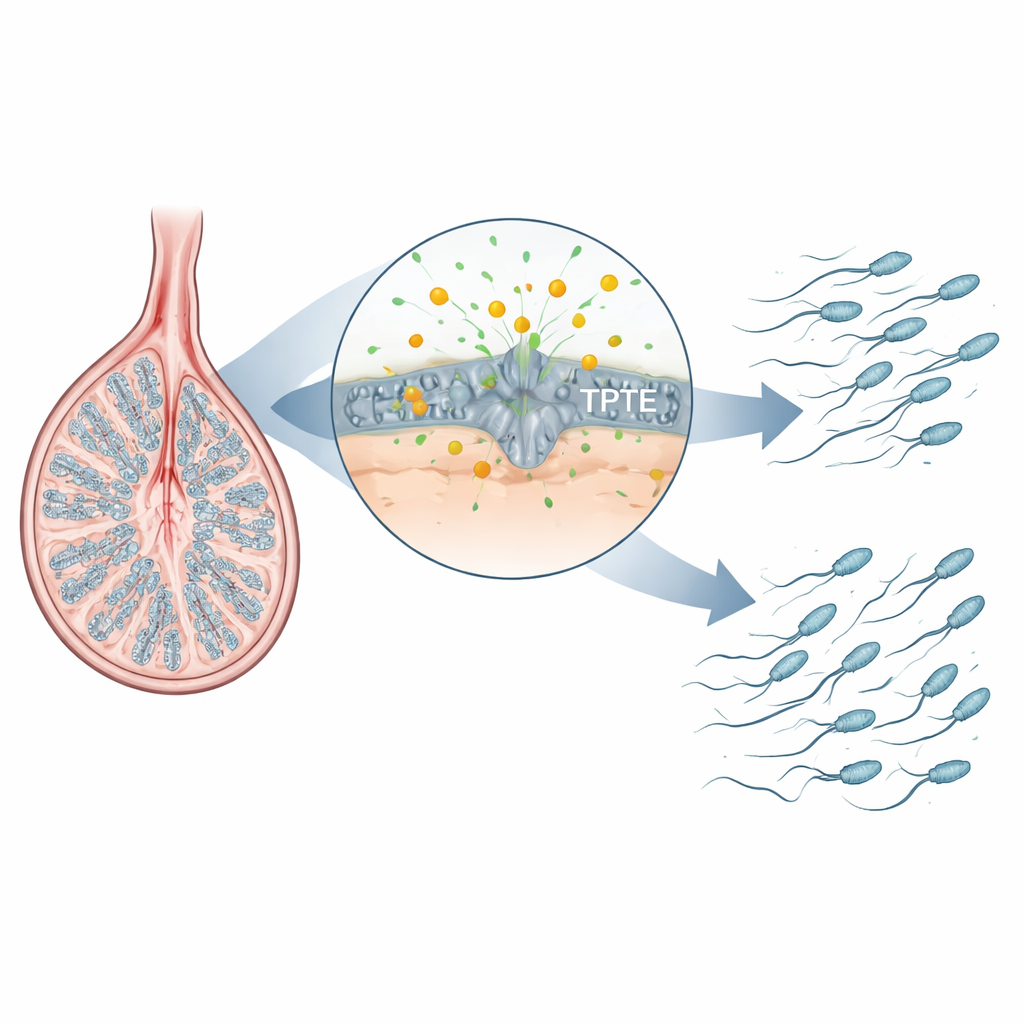
Ukryty pomocnik w rozwoju plemników
Plemniki powstają w ściśle zaaranżowanej sekwencji kroków w jądrze: komórki macierzyste dzielą się, ich potomstwo przestawia DNA podczas mejozy, a powstałe okrągłe komórki przebudowują się w smukłe, zogonalne plemniki. Autorzy skupili się na rodzinie enzymów przetwarzających lipidowe cząsteczki sygnałowe w błonach komórkowych. Jeden dobrze znany członek, PTEN, jest ważny w wielu tkankach, ale nie jest niezbędny dla późnych etapów rozwoju plemników. TPTE natomiast jest produkowane niemal wyłącznie w komórkach germinalnych jądra, a jego aktywność była słabo poznana. Mapując, gdzie kluczowy lipid błonowy PI(4,5)P2 pojawia się w jądrach myszy, badacze odkryli, że jest on szczególnie bogaty w spermatocytach i spermatydach — w tych stadiach, gdzie naprawiane są chromosomy i składane wici — co sugeruje, że TPTE i ten lipid mogą być krytyczne dla prawidłowego tworzenia plemników.
Powiązanie utraty TPTE ze słabymi plemnikami i ludzką niepłodnością
Zespół najpierw sprawdził, czy TPTE jest zmienione u mężczyzn z ciężką niepłodnością. Ponowna analiza publicznych danych z sekwencjonowania RNA z biopsji jądra wykazała, że poziomy TPTE są wyraźnie obniżone u pacjentów z niedrożnym azoospermią i innych stanów charakteryzujących się uszkodzeniem lub wyczerpaniem komórek germinalnych. Aby sprawdzić zależność przyczynowo-skutkową, usunęli gen Tpte u myszy za pomocą edycji genomu. Samce pozbawione TPTE wydawały znacznie mniejsze mioty pomimo normalnej wielkości jąder. Ich najądrza zawierała mniej plemników, a analiza komputerowa wykazała zmniejszoną ruchliwość i postępowe pływanie. Pod mikroskopem wiele plemników miało prawidłowe, owalne głowy, ale skręcone lub złożone wici, co sugeruje, że TPTE nie jest niezbędne do formowania głowy, lecz kluczowe dla utrzymania liczby plemników i kształtowania funkcjonalnych wici.
Ochrona naprawy DNA podczas mejozy
Aby zrozumieć, dlaczego liczba plemników spadła, badacze przyjrzeli się mejozie, w której chromosomy wymieniają fragmenty poprzez precyzyjnie kontrolowane pęknięcia i naprawy DNA. W jądrach pozbawionych TPTE ogólny układ stadiów komórek germinalnych wyglądał podobnie, lecz liczba komórek zaczęła spadać na etapie spermatocytu diplotenowego, a wystąpił wzrost komórek obumierających zatrzymanych w metafazie I. Rozpiętości chromosomów ujawniły defekty w strukturze przypominającej drabinę, umożliwiającej parowanie chromosomów, a znacznik uszkodzeń DNA, γ-H2AX, utrzymywał się nieprawidłowo na autosomach, wskazując na niepełną naprawę. Mniej ognisk białek wiążących DNA, RPA2 i DMC1, tworzyło się w miejscach pęknięć. Analiza molekularna wskazała na nadaktywację centralnej ścieżki wzrostu AKT/mTOR przy braku TPTE, towarzysząco z obniżonym poziomem RAD50, kluczowego komponentu inicjującego naprawę pęknięć dwuniciowych. Razem wyniki sugerują, że TPTE normalnie wytwarza PI(4,5)P2, aby powściągać aktywność AKT/mTOR, zachowując poziomy RAD50 i umożliwiając postęp naprawy DNA w mejozie, co chroni pulę żywotnych spermatydów.
Budowanie mocnych wici przez kontrolowaną produkcję białek
TPTE okazało się także niezbędne do późniejszej przebudowy okrągłych spermatydów w opływowe, ruchliwe plemniki. Mikroskopia elektronowa ogonów plemników pozbawionych TPTE ujawniła wiele przekrojów aksonemy uwięzionych w jednej membranie oraz zaburzoną aranżację „9+2” mikrotubul, wraz z zdeformowanymi włóknami podporowymi. Barwienie składników wici, takich jak acetylowana tubulina i białko zewnętrznych włókien gęstych ODF2, ujawniło nierówne, osłabione struktury, a bardziej wydłużone spermatydy częściej ulegały śmierci komórkowej w jądrze. Barwienia lipidowe pokazały wyraźne zmniejszenie i nierównomierne rozmieszczenie PI(4,5)P2 wzdłuż flagelli przy braku TPTE. Aby zobaczyć, jak to zaburzenie wpływa na maszynerię syntezy białek, autorzy przeprowadzili ilościową proteomikę na izolowanych okrągłych spermatydach. Setki białek, w tym kilka składników rybosomu, były podwyższone, a profilowanie rybosomów wskazało na zwiększoną aktywność polisomów, co jest znakiem nasilonej translacji. Wśród nich zespół wyróżnił PDLIM1, znany hamulec organizacji mikrotubul: jego poziomy białka gwałtownie wzrosły bez zmiany mRNA, a jego transkrypty przesunęły się do ciężkich frakcji polisomów, co wskazuje na nadmierną translację. Ten wzorzec znowu wiązał się z nadmiernym sygnalizowaniem AKT/mTOR wywołanym zmienioną równowagą lipidową przy braku TPTE.
Co to znaczy dla zrozumienia męskiej niepłodności
Podsumowując, badanie przedstawia TPTE jako strażnika komórek germinalnych, który dostraja lipidy błonowe, by ograniczać sygnalizację AKT/mTOR, umożliwiając prawidłową naprawę DNA i uporządkowaną syntezę białek. Gdy TPTE jest nieobecne lub zmniejszone, jak zaobserwowano w kilku typach infertylnych ludzkich jąder, pęknięcia DNA w mejozie nie są prawidłowo rozwiązywane, część rozwijających się plemników obumiera, a ocalałe często mają strukturalnie wadliwe wici i słabo pływają. Dla osób niezajmujących się na co dzień tą dziedziną kluczowe przesłanie jest takie, że męska płodność zależy nie tylko od poziomów hormonów i liczby plemników, lecz także od subtelnych regulatorów molekularnych, takich jak TPTE, które koordynują integralność genetyczną i architekturę wici. W przyszłości badanie TPTE i jego partnerów szlakowych może pomóc zidentyfikować ukryte przyczyny męskiej niepłodności i zainspirować ukierunkowane terapie przywracające zrównoważone sygnalizowanie w jądrze.
Cytowanie: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Słowa kluczowe: męska niepłodność, spermatogeneza, ruchliwość plemników, transdukcja sygnału, geny specyficzne dla jądra