Clear Sky Science · fr
TPTE, un membre de la famille PTEN spécifique aux testicules, pilote la spermatogenèse via la synthèse de PI(4,5)P2
Pourquoi cela compte pour la fertilité masculine
Beaucoup de couples peinant à concevoir n’obtiennent jamais de réponse claire expliquant pourquoi les spermatozoïdes sont peu nombreux ou peu mobiles. Cette étude dévoile une enzyme jusque-là mystérieuse, spécifique aux testicules, appelée TPTE, qui aide à orienter à la fois le réarrangement génétique des précurseurs spermatiques et la construction de leurs flagelles. En montrant comment TPTE module des molécules de signalisation clés à l’intérieur des spermatozoïdes en développement, la recherche fournit de nouvelles explications moléculaires pour certaines formes d’infertilité masculine et suggère des pistes pour le diagnostic et le traitement.
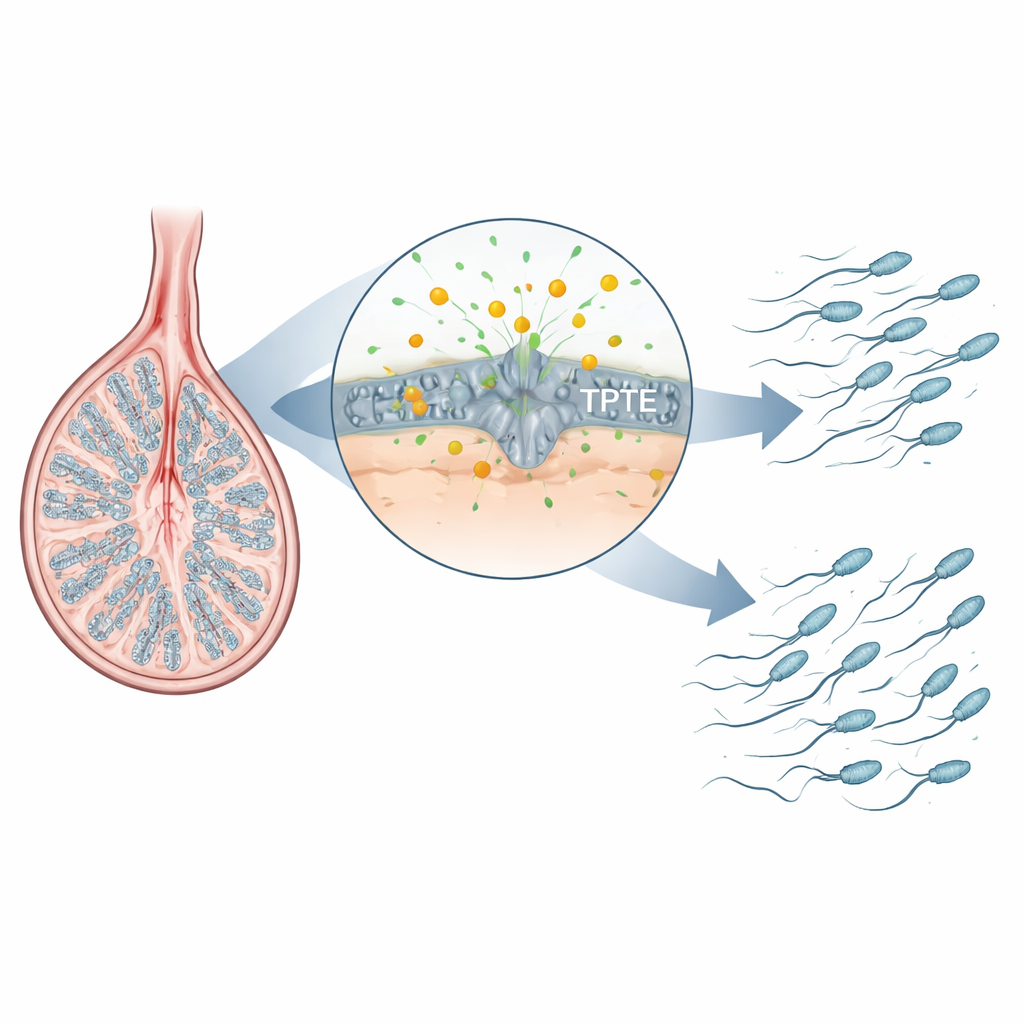
Un assistant caché dans le développement des spermatozoïdes
La fabrication des spermatozoïdes suit une séquence étroitement chorégraphiée dans le testicule : les cellules souches se divisent, leurs descendants réarrangent l’ADN pendant la méiose, et les cellules rondes résultantes se transforment en spermatozoïdes fuselés avec des flagelles. Les auteurs se sont intéressés à une famille d’enzymes qui traitent des lipides de signalisation membranaire. Un membre bien connu, PTEN, est important dans de nombreux tissus mais n’est pas essentiel aux stades tardifs de la spermatogenèse. TPTE, en revanche, est produit presque exclusivement dans les cellules germinales du testicule, et son activité était mal comprise. En cartographiant l’apparition d’un lipide membranaire clé, le PI(4,5)P2, dans les testicules de souris, les chercheurs ont constaté qu’il est particulièrement enrichi dans les spermatocytes et les spermatides — précisément aux stades où les chromosomes sont réparés et où les flagelles sont assemblés — suggérant que TPTE et ce lipide pourraient être critiques pour la formation de spermatozoïdes sains.
Relier la perte de TPTE à des spermatozoïdes déficients et à l’infertilité humaine
L’équipe a d’abord cherché si TPTE est altéré chez des hommes souffrant d’une infertilité sévère. En réanalysant des données publiques de séquençage ARN provenant de biopsies testiculaires, ils ont trouvé que les niveaux de TPTE sont fortement réduits chez des patients atteints d’azoospermie non obstructive et d’autres pathologies caractérisées par des cellules germinales endommagées ou appauvries. Pour tester le lien de causalité, ils ont supprimé le gène Tpte chez la souris par édition du génome. Les mâles dépourvus de TPTE ont engendré des portées beaucoup plus petites malgré des testicules de taille normale. Leurs épididymes contenaient moins de spermatozoïdes, et l’analyse assistée par ordinateur a montré une motilité réduite et une progression altérée. Au microscope, de nombreux spermatozoïdes avaient des têtes normales et ovales mais des flagelles enroulés ou pliés, suggérant que TPTE n’est pas indispensable à la formation de la tête mais qu’il est crucial pour maintenir le nombre de spermatozoïdes et façonner des flagelles fonctionnels.
Protéger la réparation de l’ADN durant la méiose
Pour comprendre pourquoi le nombre de spermatozoïdes diminuait, les chercheurs ont examiné la méiose, où les chromosomes échangent des segments via des cassures et réparations d’ADN finement régulées. Dans les testicules déficients en TPTE, l’organisation générale des stades des cellules germinales semblait similaire, mais les effectifs cellulaires commençaient à chuter au stade des spermatocytes en diplotène, avec une augmentation de cellules en voie de mort bloquées en métaphase I. Les étalements chromosomiques ont révélé des anomalies dans la structure en « échelle » qui permet l’alignement des chromosomes appariés, et un marqueur des cassures d’ADN, γ-H2AX, persistait anormalement sur les autosomes, indiquant une réparation incomplète. Moins de foyers des protéines d’appoint RPA2 et DMC1 se formaient aux sites de cassures. L’analyse moléculaire a mis en évidence une suractivation de la voie de croissance centrale AKT/mTOR en l’absence de TPTE, accompagnée d’une baisse des niveaux de RAD50, un composant clé initiant la réparation des cassures double-brin. Ensemble, ces résultats suggèrent que TPTE génère normalement du PI(4,5)P2 pour contenir l’activité AKT/mTOR, préservant les niveaux de RAD50 et permettant la progression de la réparation méiotique de l’ADN, protégeant ainsi la production de spermatides viables.
Construire des flagelles solides via un contrôle de la production protéique
TPTE s’est aussi avéré vital pour le remodelage tardif des spermatides rondes en spermatozoïdes profilés et mobiles. La microscopie électronique des flagelles dépourvus de TPTE a montré plusieurs sections transversales axonémales coincées dans une même membrane et des arrangements « 9+2 » de microtubules perturbés, ainsi que des fibres de soutien mal formées. Le marquage de composants de la queue, comme la tubuline acétylée et la protéine des fibres denses externes ODF2, révélait des structures irrégulières et affaiblies, et davantage de spermatides allongés subissaient la mort cellulaire dans le testicule. Le marquage lipidique montrait que le PI(4,5)P2 était fortement réduit et distribué de manière inégale le long du flagelle en l’absence de TPTE. Pour voir comment ce déséquilibre affectait la machinerie de production protéique, les auteurs ont réalisé une protéomique quantitative sur des spermatides rondes isolés. Des centaines de protéines, dont plusieurs composants ribosomiques, étaient surexprimées, et le profilage des ribosomes indiquait une activité polysomique accrue, signe d’une traduction renforcée. Parmi elles, l’équipe souligne PDLIM1, un frein connu de l’organisation des microtubules : son niveau protéique augmentait fortement sans changement de son ARN messager, et ses transcrits migraient vers des fractions polysomiques lourdes, indiquant une sur-traduction. Ce schéma renvoie encore une fois à une activation excessive de la voie AKT/mTOR déclenchée par le déséquilibre lipidique en l’absence de TPTE.
Ce que cela signifie pour la compréhension de l’infertilité masculine
Dans l’ensemble, l’étude présente TPTE comme un gardien des cellules germinales qui ajuste les lipides membranaires pour freiner la signalisation AKT/mTOR, permettant une réparation correcte de l’ADN et une synthèse protéique ordonnée. Quand TPTE manque ou est réduit, comme observé dans plusieurs types de testicules infertiles humains, les cassures d’ADN en méiose ne sont pas correctement résolues, certains spermatozoïdes en développement meurent, et les survivants présentent souvent des flagelles structurellement défectueux qui nuisent à leur nage. Pour un public non spécialiste, le message clé est que la fertilité masculine dépend non seulement des hormones et du nombre de spermatozoïdes, mais aussi de régulateurs moléculaires subtils comme TPTE qui coordonnent l’intégrité génétique et l’architecture des flagelles. À l’avenir, le dépistage de TPTE et de ses partenaires de voie pourrait aider à identifier des causes cachées d’infertilité masculine et inspirer des thérapies ciblées pour rétablir un signalement équilibré dans le testicule.
Citation: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Mots-clés: infertilité masculine, spermatogenèse, motilité des spermatozoïdes, transduction du signal, gènes spécifiques aux testicules