Clear Sky Science · nl
TPTE, een testis-specifiek lid van de PTEN-familie, stuurt spermatogenese aan via PI(4,5)P2-synthese
Waarom dit van belang is voor mannelijke vruchtbaarheid
Veel koppels die moeite hebben om zwanger te worden krijgen nooit een duidelijke verklaring waarom er weinig zaadcellen zijn of waarom ze slecht bewegen. Deze studie brengt een eerder raadselachtig, testis-specifiek enzym aan het licht, genaamd TPTE, dat zowel het genetische herschikken van zaadcelvoorlopers als de opbouw van hun zweepstaarten helpt sturen. Door te laten zien hoe TPTE sleutel-signaalmoleculen in zich ontwikkelende zaadcellen vormt, wijst het onderzoek op nieuwe moleculaire verklaringen voor bepaalde vormen van mannelijke onvruchtbaarheid en suggereert het toekomstige wegen voor diagnose en behandeling.
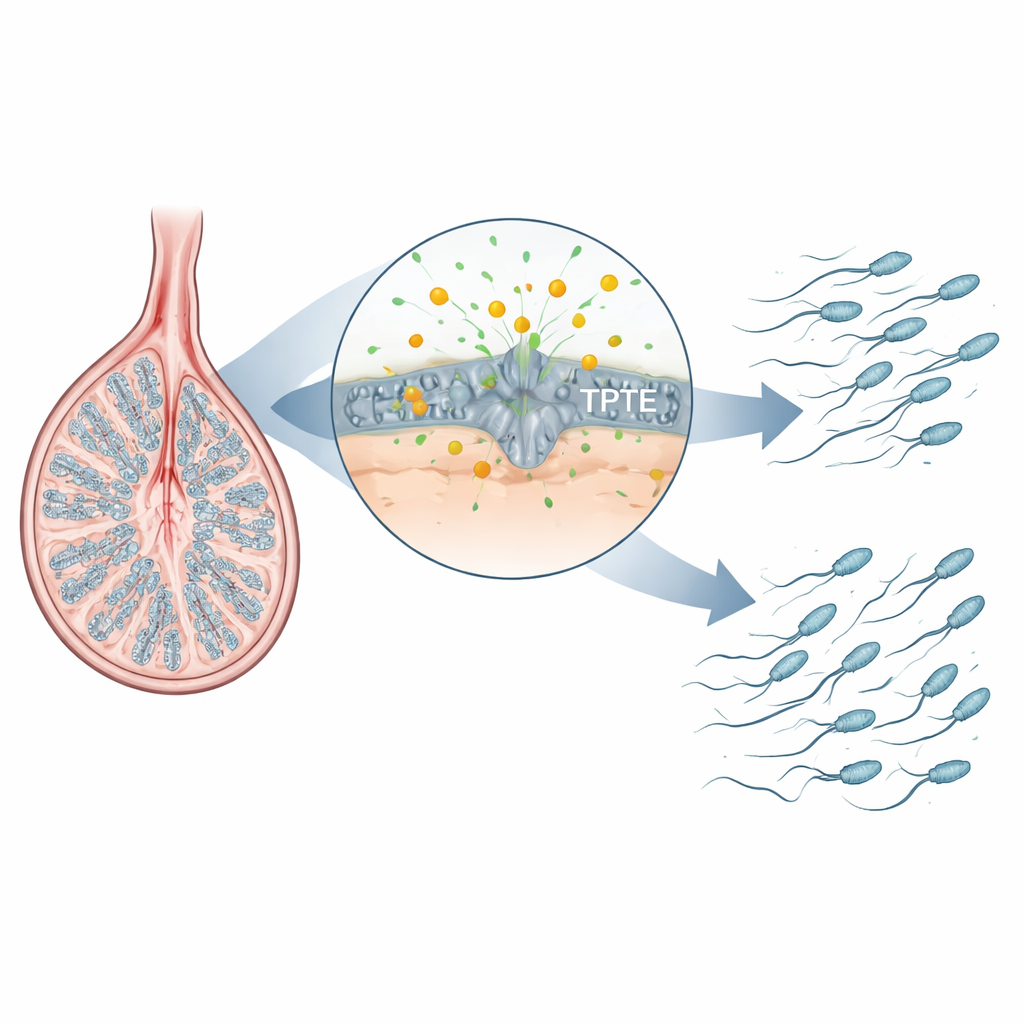
Een verborgen helper in zaadcelontwikkeling
Zaadcellen ontstaan in een nauwgezet georkestreerde reeks stappen in de testis: stamcellen delen zich, hun nakomelingen herschikken DNA tijdens meiose, en de resulterende ronde cellen remodelen tot gestroomlijnde, getailleerde zaadcellen. De auteurs richtten zich op een familie enzymen die vetachtige signaalmoleculen in celmembranen verwerken. Eén bekend lid, PTEN, is belangrijk in veel weefsels maar is niet essentieel voor de latere stadia van zaadcelontwikkeling. TPTE daarentegen wordt vrijwel uitsluitend geproduceerd in germinale cellen van de testis, en de activiteit ervan was slecht begrepen. Door in muizen testis te bepalen waar een sleutel-membraanlipide, PI(4,5)P2, voorkomt, vonden de onderzoekers dat dit lipide bijzonder verrijkt is in spermatocyten en spermatiden—de stadia waarin chromosomen worden gerepareerd en staarten worden opgebouwd—wat suggereert dat TPTE en dit lipide cruciaal zijn voor gezonde zaadcelvorming.
Het verband tussen verlies van TPTE, slechte zaadcellen en menselijke onvruchtbaarheid
Het team vroeg eerst of TPTE veranderd is bij mannen met ernstige onvruchtbaarheid. Door openbare RNA-sequencinggegevens van testisbiopten opnieuw te analyseren, vonden ze dat TPTE-niveaus sterk verlaagd zijn bij patiënten met niet-obstructieve azoöspermie en andere aandoeningen gekenmerkt door beschadigde of uitgeputte germinale cellen. Om oorzaak en gevolg te onderzoeken verwijderden ze het Tpte-gen in muizen met behulp van genbewerking. Mannelijke muizen zonder TPTE kregen veel kleinere nestjes ondanks normale testisgrootte. Hun epididymiden bevatten minder zaadcellen, en computerondersteunde analyse toonde verminderde beweeglijkheid en progressief zwemmen. Onder de microscoop hadden veel zaadcellen normale, ovale koppen maar gekromde of gevouwen staarten, wat suggereert dat TPTE niet nodig is voor de kopopbouw maar cruciaal is voor het behouden van zaadcelaantallen en het vormen van functionele staarten.
Beschermen van DNA-reparatie tijdens meiose
Om te begrijpen waarom het aantal zaadcellen afnam, zochten de onderzoekers dieper in de meiose, waar chromosomen stukken uitwisselen via precies gecontroleerde DNA-breuken en reparaties. In TPTE-deficiënte testissen zag de algehele verdeling van germinale stadia er vergelijkbaar uit, maar het aantal cellen nam af vanaf het diploteen spermatocytstadium, en er was een toename van stervende cellen die vastliepen in metafase I. Chromosoomspreidingen toonden defecten in de ladderachtige structuur die gepaarde chromosomen uitlijnt, en een marker voor DNA-breuken, γ-H2AX, bleef abnormaal lang op autosomen aanwezig, wat duidt op onvolledige reparatie. Er vormden zich minder foci van DNA-bindende helper-eiwitten RPA2 en DMC1 op breuklocaties. Moleculaire analyses wezen op overactivatie van een centraal groeipad, AKT/mTOR, in afwezigheid van TPTE, vergezeld van verlaagde niveaus van RAD50, een kerncomponent die dubbelstrengsbreukreparatie initieert. Samen suggereren deze bevindingen dat TPTE normaal gesproken PI(4,5)P2 produceert om AKT/mTOR-activiteit onder controle te houden, RAD50-niveaus te behouden en meiose-DNA-reparatie te laten verlopen, waarmee de aanvoer van levensvatbare spermatiden wordt beschermd.
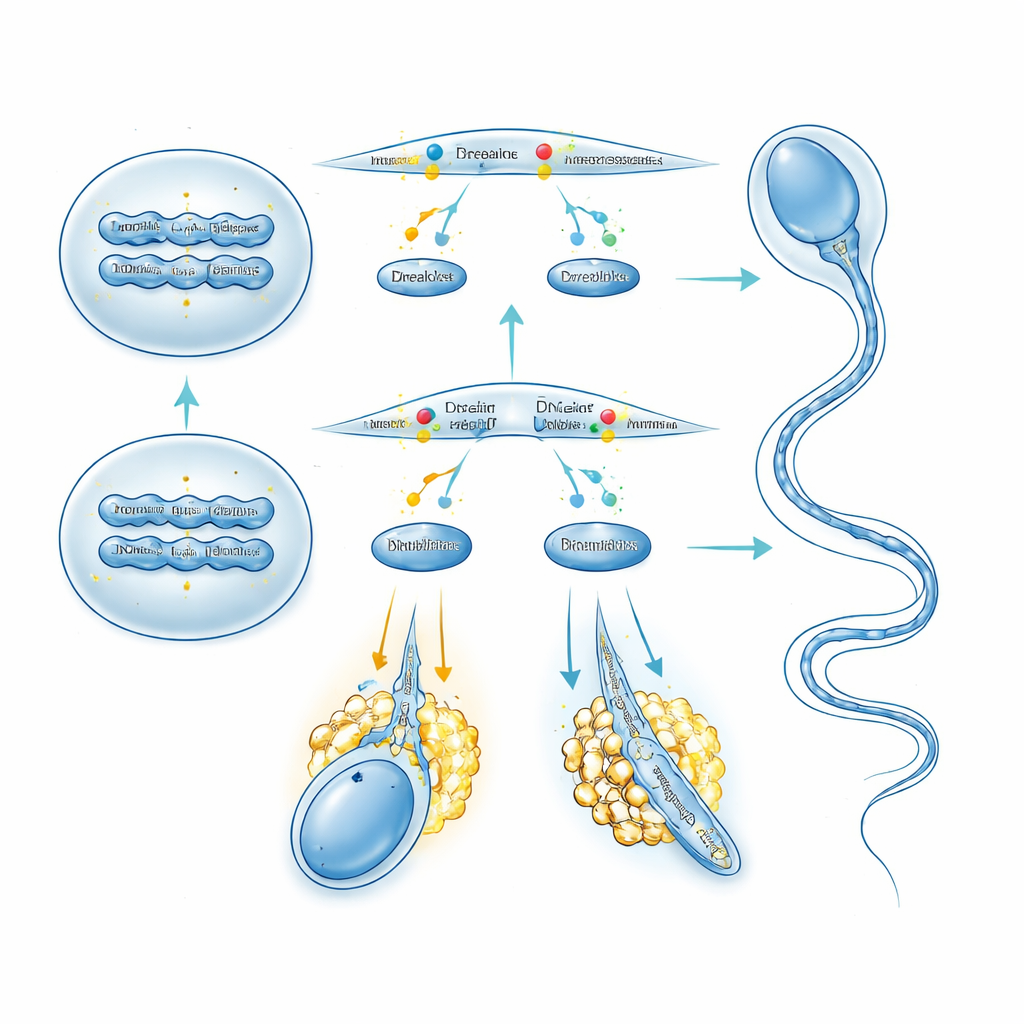
Het bouwen van sterke staarten via gecontroleerde eiwitsynthese
TPTE bleek ook essentieel voor de latere remodelering van ronde spermatiden naar gestroomlijnde, beweeglijke zaadcellen. Elektronenmicroscopie van staarten van TPTE-loze zaadcellen toonde meerdere axonemale dwarsdoorsneden gevangen in één membraan en verstoorde “9+2” microtubule-arrangementen, samen met misvormde ondersteunende vezels. Kleuring van staartcomponenten zoals geacetyleerd tubuline en het outer dense fiber-eiwit ODF2 toonde vlekkerige, verzwakte structuren, en meer verlengde spermatiden ondergingen celdood in de testis. Lipidekleuring liet zien dat PI(4,5)P2 duidelijk verminderd en ongelijk verdeeld langs flagellen was wanneer TPTE ontbrak. Om te zien hoe deze verstoring doorwerkte op het eiwitsynthese-apparaat van de cel, voerden de auteurs kwantitatieve proteomica uit op geïsoleerde ronde spermatiden. Honderden eiwitten, waaronder verschillende ribosomale componenten, waren omhoog gereguleerd, en ribosoomprofilering toonde verhoogde polysoomactiviteit, een teken van versnelde translatie. Onder deze eiwitten belichtte het team PDLIM1, een bekende rem op microtubule-organisatie: zijn eiwitniveaus stegen sterk zonder verandering in zijn boodschapper-RNA, en zijn transcripts verschoof naar zware polysoomfracties, wat wijst op overmatige translatie. Dit patroon leidde opnieuw terug naar excessieve AKT/mTOR-signalisatie die werd veroorzaakt door de verstoorde lipidebalans wanneer TPTE ontbreekt.
Wat dit betekent voor het begrip van mannelijke onvruchtbaarheid
Al met al portretteert de studie TPTE als een bewaker in germinale cellen die membraanlipiden afstemt om AKT/mTOR-signalisatie te remmen, waardoor juiste DNA-reparatie en ordelijke eiwitsynthese mogelijk worden. Wanneer TPTE ontbreekt of verminderd is, zoals waargenomen in meerdere typen onvruchtbare menselijke testissen, worden DNA-breuken in de meiose niet correct opgelost, sterven sommige zich ontwikkelende zaadcellen, en komen overlevenden vaak voort met structureel gebrekkige staarten die slecht zwemmen. Voor niet-specialisten is de kernboodschap dat mannelijke vruchtbaarheid niet alleen afhankelijk is van hormoonspiegels en zaadcelaantallen, maar ook van subtiele moleculaire regelaars zoals TPTE die genetische integriteit en staartarchitectuur coördineren. In de toekomst kan het screenen van TPTE en zijn padpartners helpen verborgen oorzaken van mannelijke onvruchtbaarheid te identificeren en gerichte therapieën inspireren die gebalanceerde signalisatie in de testis herstellen.
Bronvermelding: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Trefwoorden: mannelijke onvruchtbaarheid, spermatogenese, spermasterkte, signaaltransductie, testis-specifieke genen