Clear Sky Science · de
TPTE, ein testisspezifisches PTEN-Familienmitglied, steuert die Spermatogenese über die Synthese von PI(4,5)P2
Warum das für die männliche Fruchtbarkeit wichtig ist
Viele Paare, die Schwierigkeiten haben, ein Kind zu zeugen, erhalten nie eine klare Erklärung dafür, warum Spermien selten sind oder sich schlecht bewegen. Diese Studie entlarvt ein zuvor rätselhaftes, testisspezifisches Enzym namens TPTE, das sowohl die genetische Umstrukturierung von Spermienvorläufern als auch den Aufbau ihrer peitschenartigen Schwänze unterstützt. Indem gezeigt wird, wie TPTE wichtige Signalmoleküle in sich entwickelnden Spermien formt, liefert die Forschung neue molekulare Erklärungen für bestimmte Formen männlicher Unfruchtbarkeit und deutet auf zukünftige Wege für Diagnose und Behandlung hin.
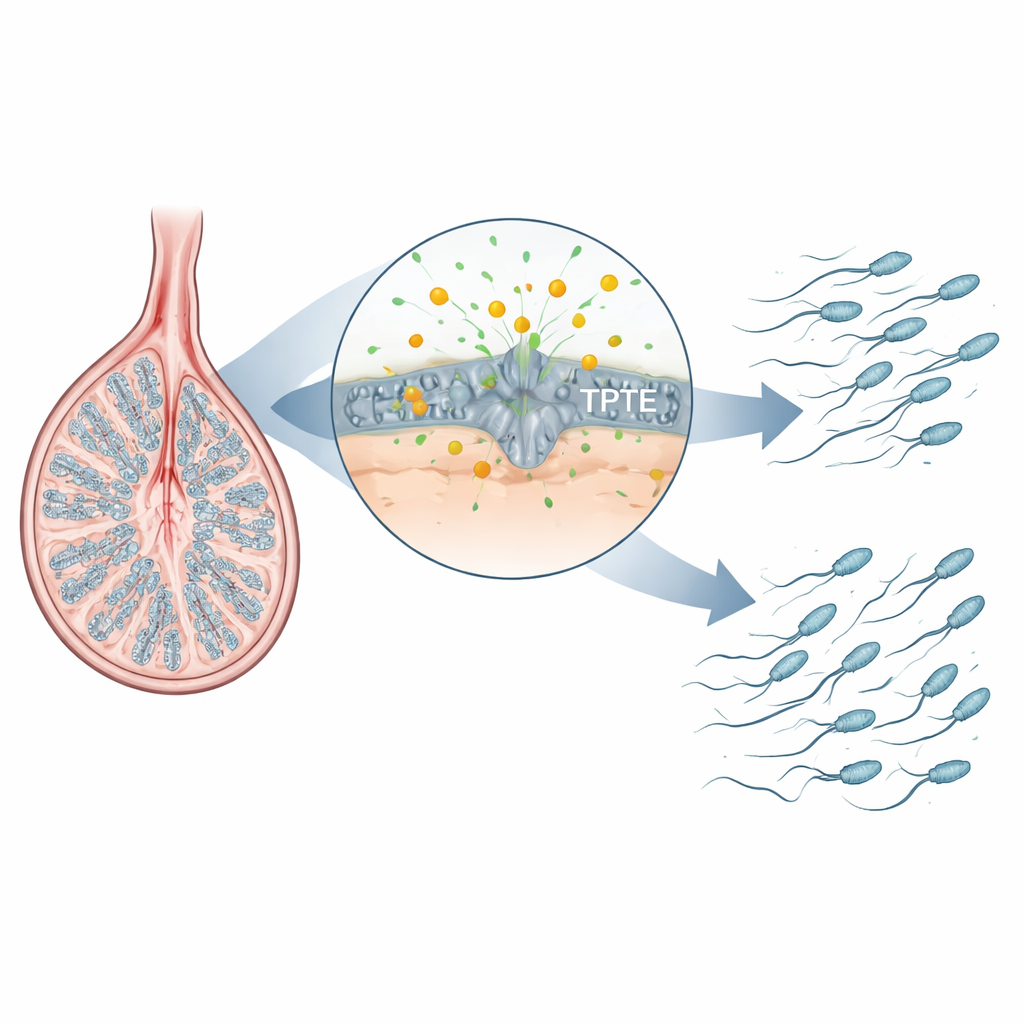
Ein verborgener Helfer in der Spermienentwicklung
Spermien entstehen in einem eng abgestimmten Ablauf im Hoden: Stammzellen teilen sich, ihre Nachkommen restrukturieren während der Meiose die DNA, und die resultierenden runden Zellen bauen sich zu stromlinienförmigen, geschwänzten Spermien um. Die Autoren konzentrierten sich auf eine Enzymfamilie, die fettartige Signalmoleküle in Zellmembranen verarbeitet. Ein bekanntes Mitglied, PTEN, ist in vielen Geweben wichtig, aber für die späten Stadien der Spermienentwicklung nicht essentiell. TPTE hingegen wird nahezu ausschließlich in Keimzellen des Hodens produziert, und seine Aktivität war wenig verstanden. Durch Kartierung, wo ein zentrales Membranlipid, PI(4,5)P2, in Maus-Hoden vorkommt, fanden die Forschenden heraus, dass es besonders in Spermatocyten und Spermatiden angereichert ist – genau in den Stadien, in denen Chromosomen repariert und Schwänze zusammengebaut werden – was darauf hindeutet, dass TPTE und dieses Lipid für die gesunde Spermienbildung entscheidend sein könnten.
Verbindung zwischen TPTE-Verlust, schlechten Spermien und männlicher Unfruchtbarkeit beim Menschen
Das Team fragte zunächst, ob TPTE bei Männern mit schwerer Unfruchtbarkeit verändert ist. Durch die Neubewertung öffentlicher RNA-Sequenzierungsdaten aus Hodenbiopsien stellten sie fest, dass die TPTE-Spiegel bei Patienten mit nicht-obstruktiver Azoospermie und anderen Zuständen mit geschädigten oder erschöpften Keimzellen auffallend reduziert sind. Um Ursache und Wirkung zu prüfen, löschten sie das Tpte-Gen in Mäusen mittels Genomeditierung. Männliche Mäuse ohne TPTE zeugten deutlich kleinere Würfe, obwohl die Hoden normal groß waren. Ihre Nebenhoden enthielten weniger Spermien, und computerunterstützte Analysen zeigten verminderte Motilität und Fortschrittlichkeit beim Schwimmen. Unter dem Mikroskop hatten viele Spermien normale, ovale Köpfe, aber gekrümmte oder gefaltete Schwänze, was darauf hindeutet, dass TPTE für den Kopfaufbau verzichtbar, aber entscheidend für die Erhaltung der Spermienzahl und die Formung funktioneller Schwänze ist.
Schutz der DNA-Reparatur während der Meiose
Um zu verstehen, warum die Spermienzahlen sanken, zoomten die Forschenden in die Meiose hinein, in der Chromosomen Segmente durch präzise gesteuerte DNA-Brüche und -Reparaturen austauschen. In TPTE-defizienten Hoden sah die allgemeine Verteilung der Keimzellstadien ähnlich aus, doch die Zellzahlen begannen im Diplotän-Spermatocyten-Stadium zu sinken, und es gab einen Anstieg abgestorbener Zellen, die in der Metaphase I gestoppt waren. Chromosomenpräparate zeigten Defekte in der leiternähnlichen Struktur, die das Paaren der Chromosomen ermöglicht, und ein Marker für DNA-Brüche, γ-H2AX, verweilte ungewöhnlich lang auf den Autosomen, was auf unvollständige Reparatur hinweist. Weniger Foki der DNA-Bindungshelfer RPA2 und DMC1 bildeten sich an Bruchstellen. Molekulare Analysen deuteten auf eine Überaktivierung eines zentralen Wachstumswegs, AKT/mTOR, in Abwesenheit von TPTE hin, einhergehend mit verminderten RAD50-Spiegeln, einem Kernbestandteil, der die Reparatur von Doppelstrangbrüchen initiiert. Zusammen deuten diese Befunde darauf hin, dass TPTE normalerweise PI(4,5)P2 erzeugt, um die AKT/mTOR-Aktivität in Schach zu halten, dadurch RAD50-Spiegel bewahrt und die meiotische DNA-Reparatur ermöglicht, womit die Versorgung mit lebensfähigen Spermatiden geschützt wird.
Starke Schwänze durch kontrollierte Proteinproduktion
TPTE erwies sich auch als wesentlich für die spätere Umgestaltung runder Spermatiden zu stromlinienförmigen, beweglichen Spermien. Elektronenmikroskopie an Spermien ohne TPTE zeigte mehrere Axonem-Querschnitte, die in einer einzigen Membran gefangen waren, sowie gestörte „9+2“-Mikrotubulus-Anordnungen und deformierte Stützfasern. Färbungen von Schwanzkomponenten wie acetylierter Tubulin und dem äußeren dichten Faserprotein ODF2 offenbarten fleckige, geschwächte Strukturen, und vermehrt längliche Spermatiden gingen im Hoden durch Zelltod verloren. Lipidfärbungen zeigten, dass PI(4,5)P2 deutlich reduziert und ungleichmäßig entlang der Flagellen verteilt war, wenn TPTE fehlte. Um zu sehen, wie diese Störung die Proteinproduktionsmaschinerie der Zelle beeinflusst, führten die Autoren quantitative Proteomik an isolierten runden Spermatiden durch. Hunderte Proteine, darunter mehrere ribosomale Komponenten, waren hochreguliert, und Ribosomprofilierung zeigte erhöhte Polysomenaktivität, ein Zeichen gesteigerter Translation. Besonders hoben die Forschenden PDLIM1 hervor, einen bekannten Bremsfaktor für die Mikrotubulusorganisation: seine Proteinmengen stiegen stark an, ohne dass sich die mRNA änderte, und seine Transkripte verschoben sich in schwere Polysomenfraktionen, was auf Übertranslation hinweist. Dieses Muster führte wiederum auf übermäßige AKT/mTOR-Signalisierung zurück, ausgelöst durch das veränderte Lipidgleichgewicht bei fehlendem TPTE.
Was das für das Verständnis männlicher Unfruchtbarkeit bedeutet
In der Zusammenfassung zeichnet die Studie TPTE als einen Keimzellwächter, der Membranlipide abstimmt, um AKT/mTOR-Signale zu dämpfen und so korrekte DNA-Reparatur und geordnete Proteinsynthese zu ermöglichen. Fehlt TPTE oder ist es reduziert, wie bei mehreren Formen infertiler menschlicher Hoden beobachtet, werden DNA-Brüche in der Meiose nicht richtig aufgelöst, einige sich entwickelnde Spermien sterben, und Überlebende weisen häufig strukturell fehlerhafte Schwänze auf, die schlecht schwimmen. Für Nicht-Fachleute ist die Kernbotschaft: Männliche Fruchtbarkeit hängt nicht nur von Hormonspiegeln und Spermienzahlen ab, sondern auch von subtilen molekularen Regulatoren wie TPTE, die genetische Integrität und Schwanzarchitektur koordinieren. Zukünftig könnten Tests auf TPTE und seine Weg-Partner dabei helfen, verborgene Ursachen männlicher Unfruchtbarkeit zu identifizieren und gezielte Therapien zu entwickeln, die das Signalgleichgewicht im Hoden wiederherstellen.
Zitation: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Schlüsselwörter: männliche Unfruchtbarkeit, Spermatogenese, Spermienmotilität, Signaltransduktion, testisspezifische Gene