Clear Sky Science · it
TPTE, un membro della famiglia PTEN specifico per il testicolo, guida la spermatogenesi tramite la sintesi di PI(4,5)P2
Perché questo è importante per la fertilità maschile
Molte coppie che faticano a concepire non ottengono mai una risposta chiara sul perché gli spermatozoi siano pochi o si muovano male. Questo studio mette in luce un enzima specifico del testicolo finora misterioso, chiamato TPTE, che contribuisce sia al rimescolamento genetico dei precursori degli spermatozoi sia alla costruzione delle loro code filamentose. Mostrando come TPTE modelli importanti molecole di segnalazione lipidiche all’interno degli spermatozoi in sviluppo, la ricerca indica nuove spiegazioni molecolari per certe forme di infertilità maschile e suggerisce possibili direzioni future per diagnosi e terapie.
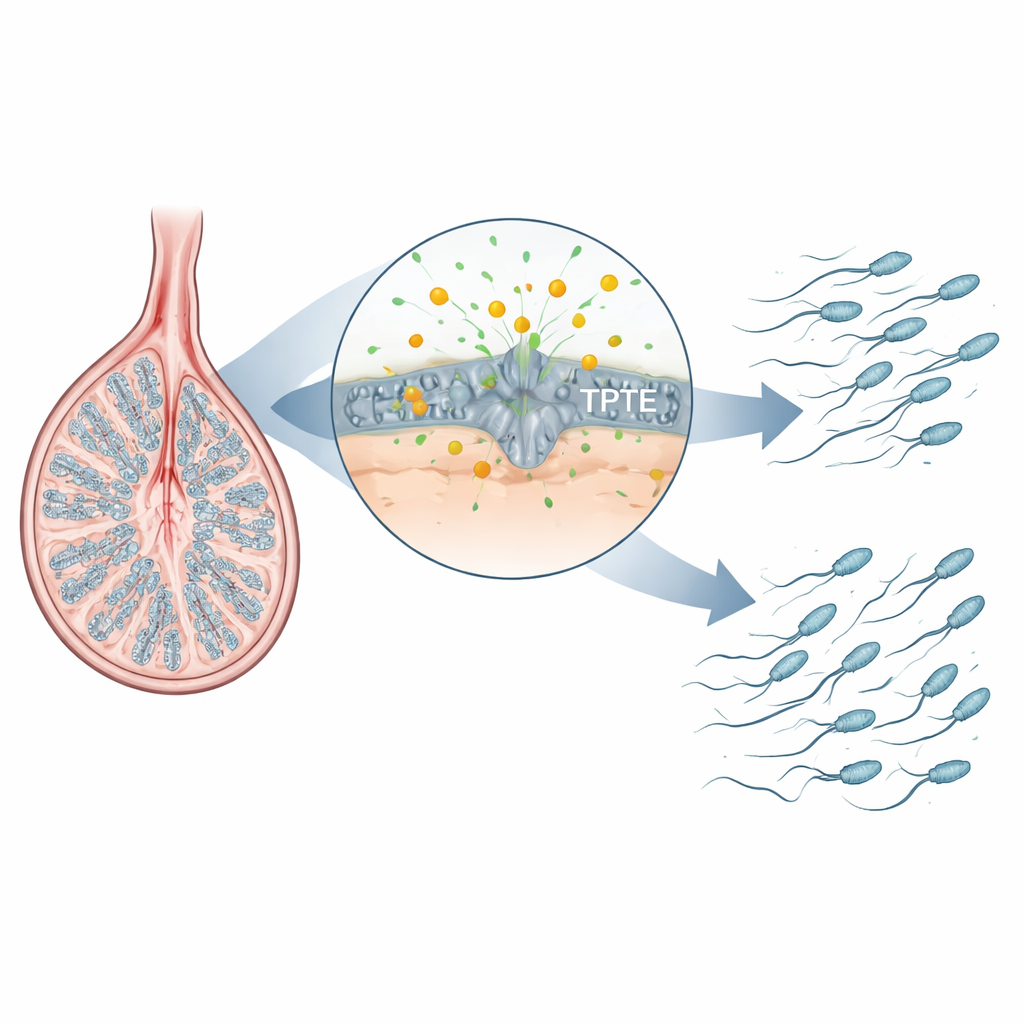
Un aiutante nascosto nello sviluppo degli spermatozoi
Gli spermatozoi si formano attraverso una sequenza strettamente coreografata di passaggi all’interno del testicolo: le cellule staminali si dividono, i loro discendenti rimescolano il DNA durante la meiosi e le cellule tonde risultanti si rimodellano in spermatozoi snelli e provvisti di coda. Gli autori si sono concentrati su una famiglia di enzimi che processano lipidi di segnalazione nelle membrane cellulari. Un membro ben noto, PTEN, è importante in molti tessuti ma non è essenziale per le fasi avanzate della formazione degli spermatozoi. TPTE, invece, è prodotto quasi esclusivamente nelle cellule germinali del testicolo e la sua attività era poco compresa. Mappando dove compare un importante lipide di membrana, PI(4,5)P2, nei testicoli di topo, i ricercatori hanno scoperto che è particolarmente arricchito in spermatociti e spermatidi — le stesse fasi in cui i cromosomi vengono riparati e si assemblano le code — suggerendo che TPTE e questo lipide potrebbero essere critici per una formazione sana degli spermatozoi.
Collegare la perdita di TPTE a spermatozoi difettosi e all’infertilità umana
Il gruppo ha prima verificato se TPTE fosse alterato negli uomini con infertilità severa. Rianalizzando dati pubblici di RNA-seq da biopsie testicolari, hanno trovato che i livelli di TPTE risultano drasticamente ridotti in pazienti con azoospermia non ostruttiva e in altre condizioni caratterizzate da cellule germinali danneggiate o esaurite. Per esplorare causa ed effetto, hanno eliminato il gene Tpte nei topi tramite editing genomico. I maschi privi di TPTE hanno generato cucciolate molto più piccole nonostante dimensioni testicolari normali. Gli epididimi contenevano meno spermatozoi e l’analisi computerizzata ha mostrato motilità ridotta e minore progressione nel nuoto. Al microscopio molti spermatozoi avevano teste normali e ovali ma code arricciate o piegate, suggerendo che TPTE non è indispensabile per costruire la testa ma è cruciale per mantenere il numero di spermatozoi e plasmare code funzionali.
Proteggere la riparazione del DNA durante la meiosi
Per capire perché il numero di spermatozoi calasse, i ricercatori si sono concentrati sulla meiosi, dove i cromosomi si scambiano segmenti tramite rotture e riparazioni del DNA strettamente controllate. Nei testicoli privi di TPTE, l’ordine complessivo delle fasi delle cellule germinali appariva simile, ma i conteggi cellulari iniziavano a diminuire allo stadio di spermatocita diplotene e si osservava un aumento di cellule morenti bloccate in metafase I. Gli spread cromosomici hanno rivelato difetti nella struttura a scala che permette l’allineamento dei cromosomi appaiati, e un marcatore delle rotture del DNA, γ-H2AX, persisteva anormalmente sugli autosomi, indicando riparazione incompleta. Si formavano meno foci dei fattori leganti il DNA RPA2 e DMC1 nei siti di rottura. L’analisi molecolare ha indicato una iperattivazione della via di crescita centrale AKT/mTOR in assenza di TPTE, accompagnata da livelli ridotti di RAD50, un componente chiave che avvia la riparazione dei doppi filamenti. Nel complesso, questi risultati suggeriscono che TPTE normalmente genera PI(4,5)P2 per tenere sotto controllo l’attività AKT/mTOR, preservare i livelli di RAD50 e permettere la riparazione meiotica del DNA, proteggendo così la fornitura di spermatidi vitali.
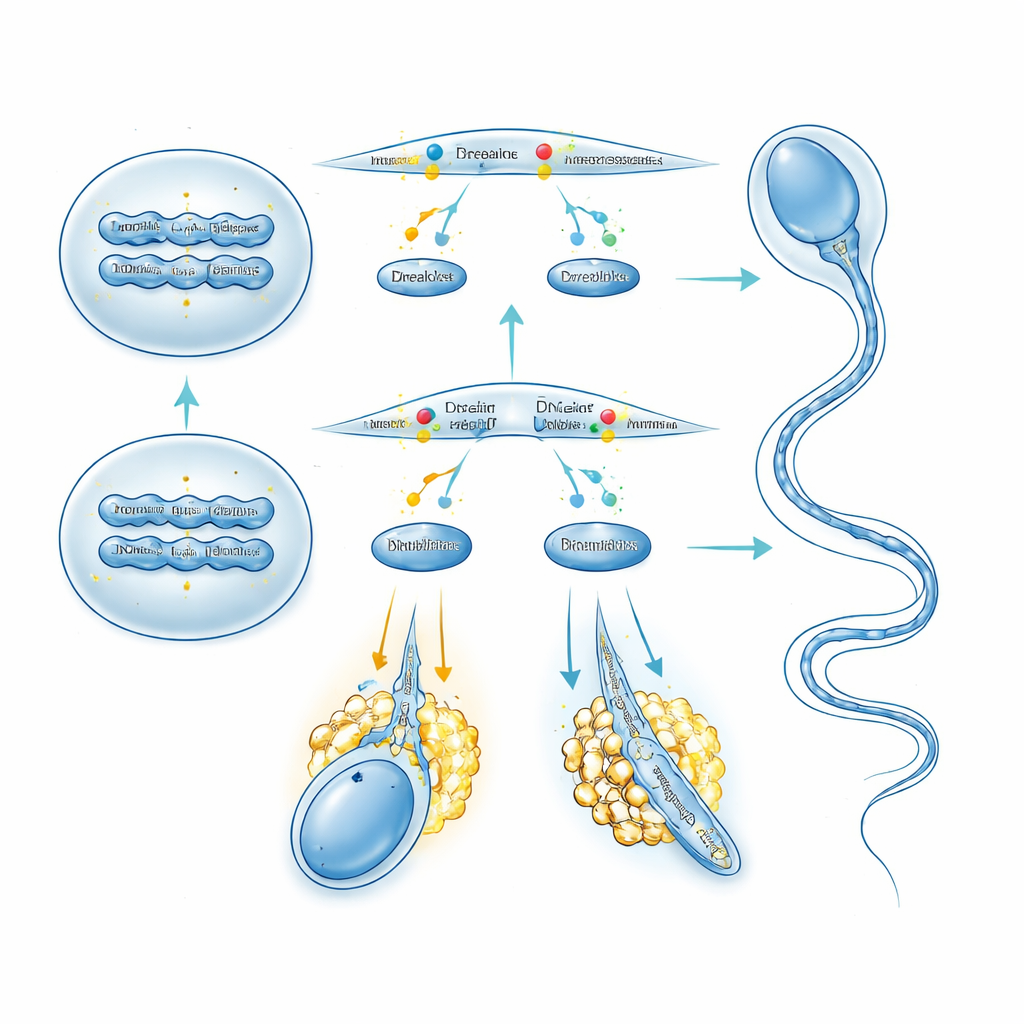
Costruire code robuste tramite il controllo della produzione proteica
TPTE si è rivelato inoltre essenziale per il rimodellamento finale degli spermatidi tondi in spermatozoi snelli e mobili. La microscopia elettronica delle code degli spermatozoi privi di TPTE ha mostrato multiple sezioni assonemali intrappolate in una singola membrana e disposizioni “9+2” dei microtubuli disturbate, insieme a fibre di sostegno malformate. Colorazioni per componenti della coda come la tubulina acetilata e la proteina della fibra esterna ODF2 hanno rivelato strutture irregolari e indebolite, e un maggior numero di spermatidi allungati è andato incontro a morte cellulare nel testicolo. La colorazione lipidica ha mostrato che PI(4,5)P2 era marcatamente ridotta e distribuita in modo non uniforme lungo il flagello quando mancava TPTE. Per capire come questa alterazione influenzasse la macchina proteica della cellula, gli autori hanno eseguito proteomica quantitativa su spermatidi tondi isolati. Centinaia di proteine, inclusi diversi componenti ribosomiali, risultavano sovraregolate, e il profilo dei ribosomi indicava una maggiore attività dei polisomi, segno di traduzione aumentata. Tra queste, il gruppo ha evidenziato PDLIM1, noto freno sull’organizzazione dei microtubuli: i suoi livelli proteici sono aumentati nettamente senza cambiamenti nel suo mRNA, e i suoi trascritti si sono spostati in frazioni di polisomi pesanti, indicando sovratraduzione. Questo quadro ricondurrebbe nuovamente all’eccessiva segnalazione AKT/mTOR scatenata dallo squilibrio lipidico quando TPTE è assente.
Cosa significa per la comprensione dell’infertilità maschile
Nel complesso, lo studio descrive TPTE come un guardiano delle cellule germinali che modula i lipidi di membrana per contenere la segnalazione AKT/mTOR, permettendo una corretta riparazione del DNA e una sintesi proteica ordinata. Quando TPTE è mancante o ridotto, come osservato in diversi tipi di testicoli umani infertili, le rotture del DNA durante la meiosi non vengono risolte correttamente, alcuni spermatozoi in via di sviluppo muoiono e i sopravvissuti spesso presentano code strutturalmente difettose che nuotano male. Per i non specialisti, il messaggio chiave è che la fertilità maschile dipende non solo da livelli ormonali e conteggi degli spermatozoi, ma anche da regolatori molecolari sottili come TPTE che coordinano l’integrità genetica e l’architettura della coda. In futuro, lo screening di TPTE e dei suoi partner di via potrebbe aiutare a identificare cause nascoste di infertilità maschile e ispirare terapie mirate che ristabiliscano un segnale bilanciato nel testicolo.
Citazione: Chen, X., Wang, T., Wu, H. et al. TPTE, a testis-specific PTEN family member, drives spermatogenesis via PI(4,5)P2 synthesis. Cell Death Dis 17, 378 (2026). https://doi.org/10.1038/s41419-026-08614-3
Parole chiave: infertilità maschile, spermatogenesi, motilità degli spermatozoi, trasduzione del segnale, geni specifici del testicolo