Clear Sky Science · ru
Таргетирование пролил-3-гидроксилазы 1 тормозит прогрессирование рака поджелудочной железы и влияет на макрофагальный иммунитет
Почему это исследование важно
Рак поджелудочной железы — один из самых смертоносных видов рака: его часто выявляют на поздних стадиях, и он устойчив к лечению. В этом исследовании изучают скрытый молекулярный «переключатель», который способствует росту опухолей поджелудочной железы и их уклонению от иммунного ответа, и показывают, что отключение этого переключателя может замедлить прогрессирование болезни и повысить эффективность стандартной химиотерапии.
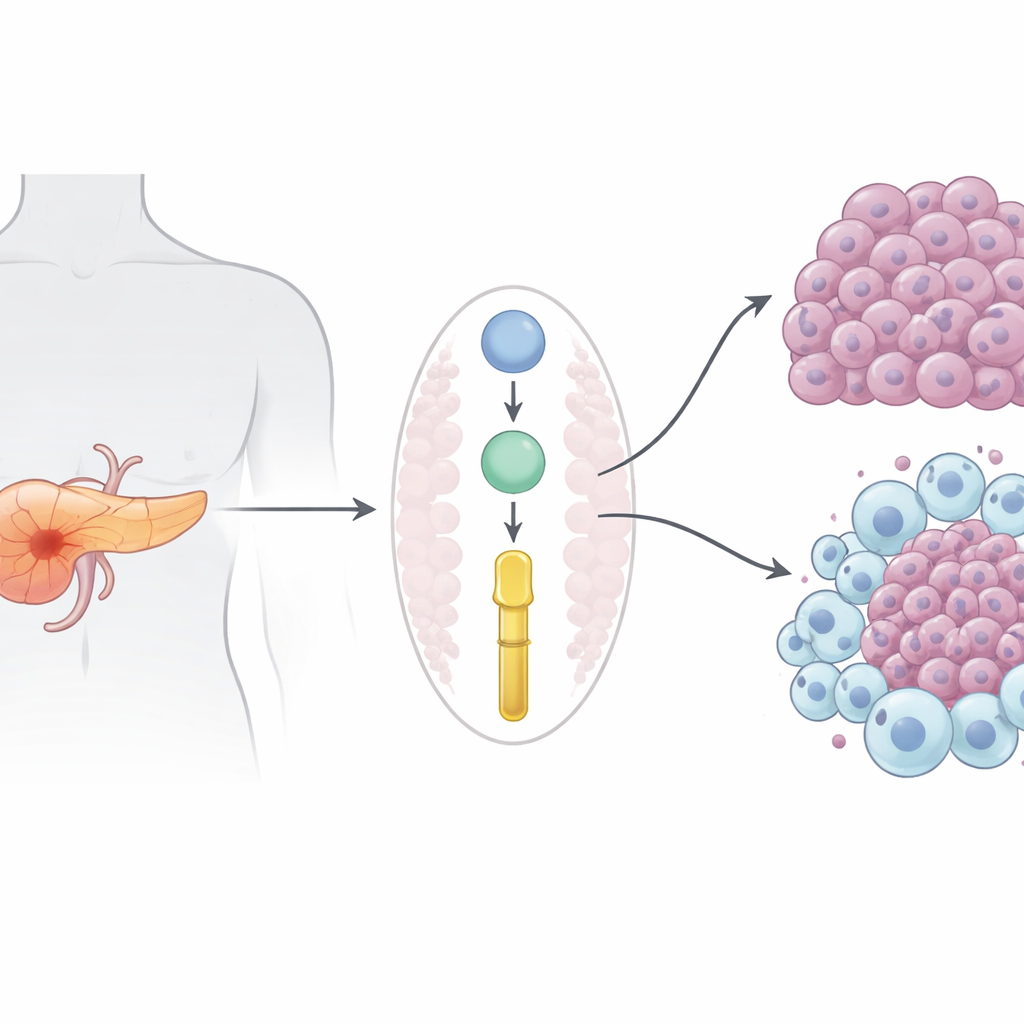
Смертоносный рак с немногими эффективными опциями
Аденокарцинома протоков поджелудочной железы, наиболее распространённая форма рака поджелудочной железы, убивает почти столько же людей, сколько поражает. Поскольку её обычно диагностируют уже после распространения, хирургическое вмешательство часто невозможно, а препараты, такие как гемцитабин, дают лишь скромный и кратковременный эффект. Современные иммунотерапии, изменившие подход к лечению меланомы и рака лёгких, здесь в основном не работают — отчасти потому, что опухоли поджелудочной железы формируют иммунологически «холодное» окружение, которое отталкивает полезные иммунные клетки и поддерживает клетки, защищающие опухоль.
Скрытый помощник: фермент коллагена, вышедший из-под контроля
Авторы сосредоточились на белках, секретируемых опухолевыми клетками, которые могут формировать как рост опухоли, так и окружающее иммунное окружение. При повторном анализе больших наборов данных по белкам у пациентов и в хорошо изученной мышиной модели они выделили пролил-3-гидроксилазу 1 (P3H1) — фермент, прежде всего известный своей ролью в модификации коллагена в костях и коже. У людей и у мышей уровни P3H1 в тканях опухоли поджелудочной железы были значительно выше, чем в здоровой поджелудочной, а у пациентов с опухолями, содержащими больше P3H1, наблюдались более ранние рецидивы и более короткая выживаемость. Важно, что повышенный уровень P3H1 ассоциировался с более обширным поражением, что указывает на его активную роль, а не просто сопутствующее явление роста опухоли.
Отключение P3H1 замедляет опухоли и перестраивает иммунные клетки
Чтобы проверить, действительно ли P3H1 стимулирует рак, исследователи создали мышей с утраченным геном P3H1 в панкреатических клетках, при этом сохранив классические онкогенные мутации, которые обычно приводят к агрессивным опухолям. У мышей без P3H1 опухоли были меньшими, сохранялось больше нормальной ткани поджелудочной железы, и они жили примерно на 20% дольше, чем их сиблинги с интактным P3H1. В опухолях мышей и в культурах человеческих раковых клеток in vitro потеря P3H1 резко снижала пролиферацию опухолевых клеток. Одновременно в опухолях без P3H1 значительно уменьшалось количество «M2-подобных» ассоциированных с опухолью макрофагов — иммунных клеток, которые обычно помогают опухоли, стимулируя рост, ангиогенез и лекарственную устойчивость. Раковые клетки с высоким уровнем P3H1 секретировали больше трёх сигнальных белков (CXCL1, CXCL5 и CXCL8), привлекающих и перенаправляющих макрофаги; снижение P3H1 понижало эти сигналы и ослабляло набор и поляризацию макрофагов.
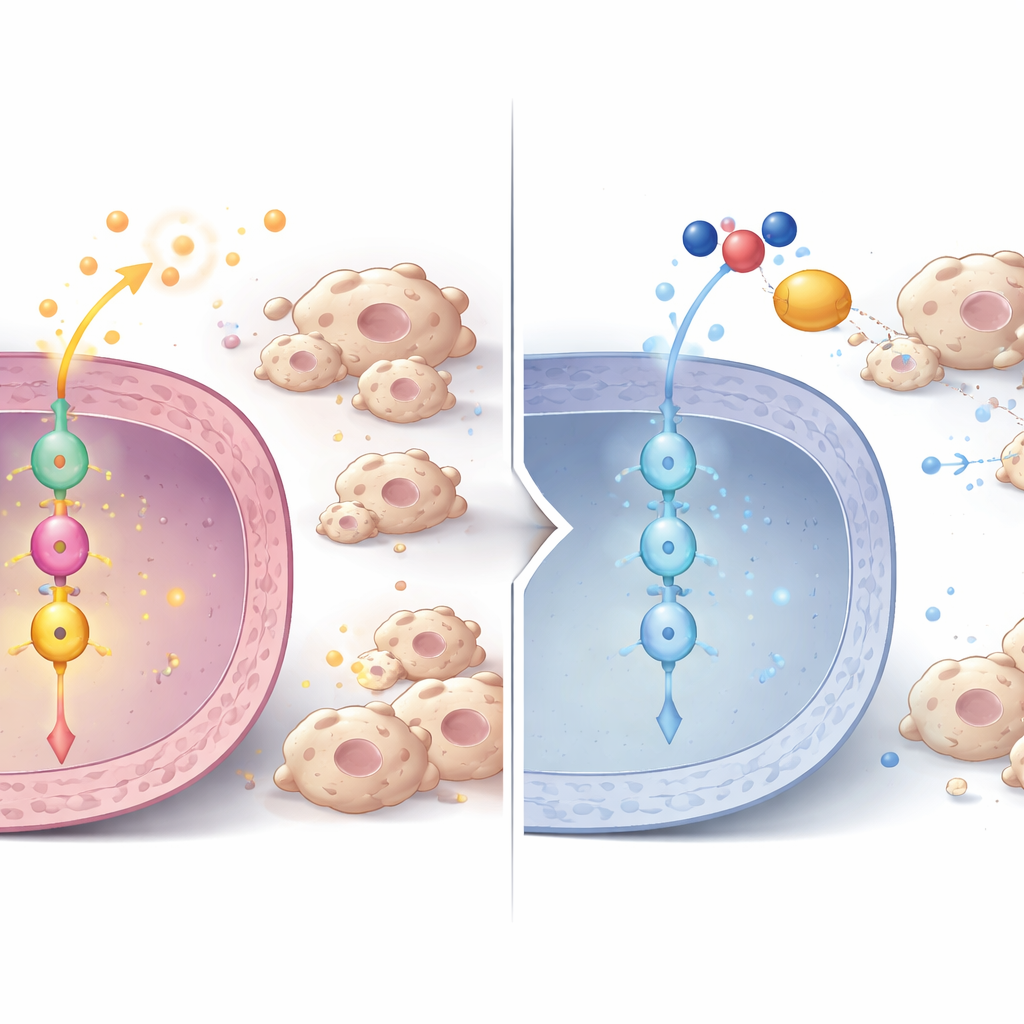
Сигнальная цепочка от P3H1 к делению клеток и иммунному контролю
Углубляясь, исследователи выявили внутри опухолевых клеток сигнальную цепочку. При уменьшении P3H1 снижался уровень другого белка — Polo-подобной киназы 1 (PLK1) — как на белковом, так и на РНК-уровне в клетках, мышиных опухолях и образцах пациентов. PLK1 — ключевой регулятор клеточного деления, уже известный своей гиперактивностью во многих видах рака. С помощью фосфопротеомики команда показала, что активность PLK1 обычно усиливает центральный онкогенный регулятор β-катенин, модифицируя его в конкретной позиции, необходимой для проникновения в ядро клетки. В клетках без P3H1 метка активации на β-катенине падала, его ядерная локализация уменьшалась, и снижалась экспрессия генов-мишеней β-катенина. Среди этих мишеней — не только драйверы клеточного цикла, такие как c-Myc и Cyclin D1, стимулирующие деление клеток, но и цитокины, привлекающие макрофаги, которые поддерживают опухоль. Восстановление P3H1 или PLK1 в клетках, лишённых P3H1, возвращало активность β-катенина, пролиферацию раковых клеток и набор макрофагов, что подчёркивает центральную роль оси P3H1–PLK1–β-катенин.
Усиление действия химиотерапии
Поскольку сигналинг β-катенина и макрофаги, поддерживающие опухоль, были связаны с резистентностью к гемцитабину и другим стандартным схемам, авторы проверили, улучшит ли блокирование этой оси терапевтический эффект. Они сочетали гемцитабин (и другие стандартные комбинации) с ингибитором PLK1, BI2536, в опытных мышах с человеческими опухолями поджелудочной железы. При тщательно подобранной дозе, избегающей токсичности для органов, комбинация дала значительно меньшие опухоли, меньше делящихся раковых клеток и меньше ассоциированных с опухолью макрофагов по сравнению только с химиотерапией. Пациент-ассоциированные органоиды поджелудочной железы — мини-опухоли, выращенные из хирургических образцов — показали схожую картину: подавление P3H1 замедляло их рост, снижало PLK1 и делало их более уязвимыми к гемцитабину в сочетании с наб-паклитакселом, а ингибитор PLK1 дополнительно усиливал чувствительность к лекарствам.
Что это значит для будущего лечения
Проще говоря, работа выделяет трио молекул — P3H1, PLK1 и β-катенин — которые вместе действуют как педаль акселератора для опухолей поджелудочной железы, стимулируя интенсивное деление клеток и привлечение иммунных клеток, которые помогают раку вместо того, чтобы его уничтожать. Отключение этой оси замедляет рост опухоли и делает существующую химиотерапию более эффективной в мышиных моделях и на материалах, полученных от пациентов. Хотя препаратов, напрямую блокирующих P3H1, пока нет, ингибиторы PLK1 уже разрабатываются, что даёт надежду на то, что в будущем их сочетание со стандартной химиотерапией может обеспечить пациентам с раком поджелудочной железы более долговременный контроль над болезнью.
Цитирование: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
Ключевые слова: рак поджелудочной железы, микроокружение опухоли, макрофаги, сигнальный путь β-катенина, таргетная химиотерапия