Clear Sky Science · es
Dirigir la prolil 3-hidroxilasa 1 inhibe la progresión del cáncer de páncreas y la inmunidad de los macrófagos
Por qué importa esta investigación
El cáncer de páncreas está entre los más mortales, con frecuencia se detecta tarde y es notoriamente resistente al tratamiento. Este estudio explora un “interruptor” molecular oculto que ayuda a los tumores pancreáticos a crecer y evadir al sistema inmunitario, y muestra cómo apagar ese interruptor puede frenar la enfermedad y mejorar la eficacia de la quimioterapia convencional.
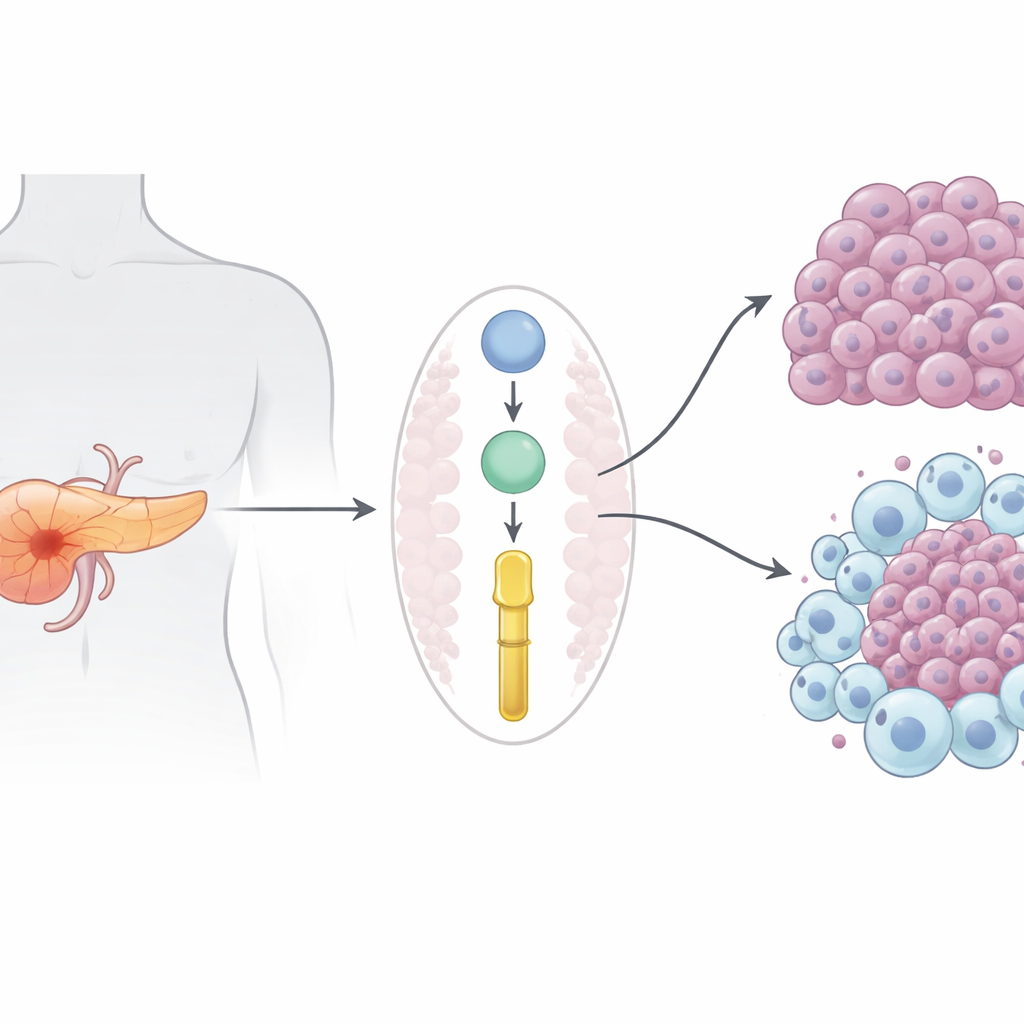
Un cáncer letal con pocas opciones
El adenocarcinoma ductal pancreático, la forma más común de cáncer de páncreas, mata a casi tantas personas como las que afecta. Debido a que suele diagnosticarse después de haberse diseminado, la cirugía a menudo no es posible, y fármacos como la gemcitabina ofrecen solo un beneficio modesto y de corta duración. Las inmunoterapias modernas que han transformado el tratamiento del melanoma y el cáncer de pulmón han fracasado en gran medida aquí, en parte porque los tumores pancreáticos crean un entorno inmunológicamente “frío” que mantiene fuera a las células inmunitarias útiles y alimenta a las células que protegen al cáncer.
El colaborador oculto: una enzima de colágeno fuera de control
Los investigadores se centraron en proteínas secretadas por las células tumorales que podrían moldear tanto el crecimiento del cáncer como el entorno inmune circundante. Al reanalizar grandes conjuntos de datos proteómicos de pacientes humanos y de un modelo de ratón bien establecido, identificaron la Prolil 3-hidroxilasa 1 (P3H1), una enzima conocida por modificar el colágeno en hueso y piel. En humanos y ratones, los niveles de P3H1 eran mucho más altos en los tumores pancreáticos que en el páncreas sano, y los pacientes cuyos tumores presentaban más P3H1 tendían a recaer antes y a morir antes. De forma importante, el aumento de P3H1 se asoció con una enfermedad más extensa, lo que sugiere que hace algo más que acompañar el crecimiento tumoral.
Apagar P3H1 ralentiza los tumores y remodela las células inmunitarias
Para comprobar si P3H1 impulsa realmente el cáncer, el equipo diseñó ratones cuyos linajes pancreáticos carecían del gen P3H1, aunque conservaban las mutaciones clásicas que normalmente producen tumores agresivos. Estos ratones deficientes en P3H1 desarrollaron tumores más pequeños, conservaron más tejido pancreático normal y vivieron aproximadamente un 20 % más que sus homólogos con P3H1 intacta. En tumores de ratón y en líneas celulares humanas cultivadas en el laboratorio, la pérdida de P3H1 redujo drásticamente la proliferación de células tumorales. Al mismo tiempo, los tumores sin P3H1 contenían muchos menos macrófagos asociados al tumor de tipo «M2», células inmunitarias que normalmente ayudan a los tumores promoviendo el crecimiento, la formación de vasos y la resistencia a los fármacos. Las células cancerosas con alta P3H1 secretaban más de tres proteínas señal (CXCL1, CXCL5 y CXCL8) que atraen y reprograman macrófagos; reducir P3H1 bajó estas señales y atenuó el reclutamiento y la polarización de macrófagos.
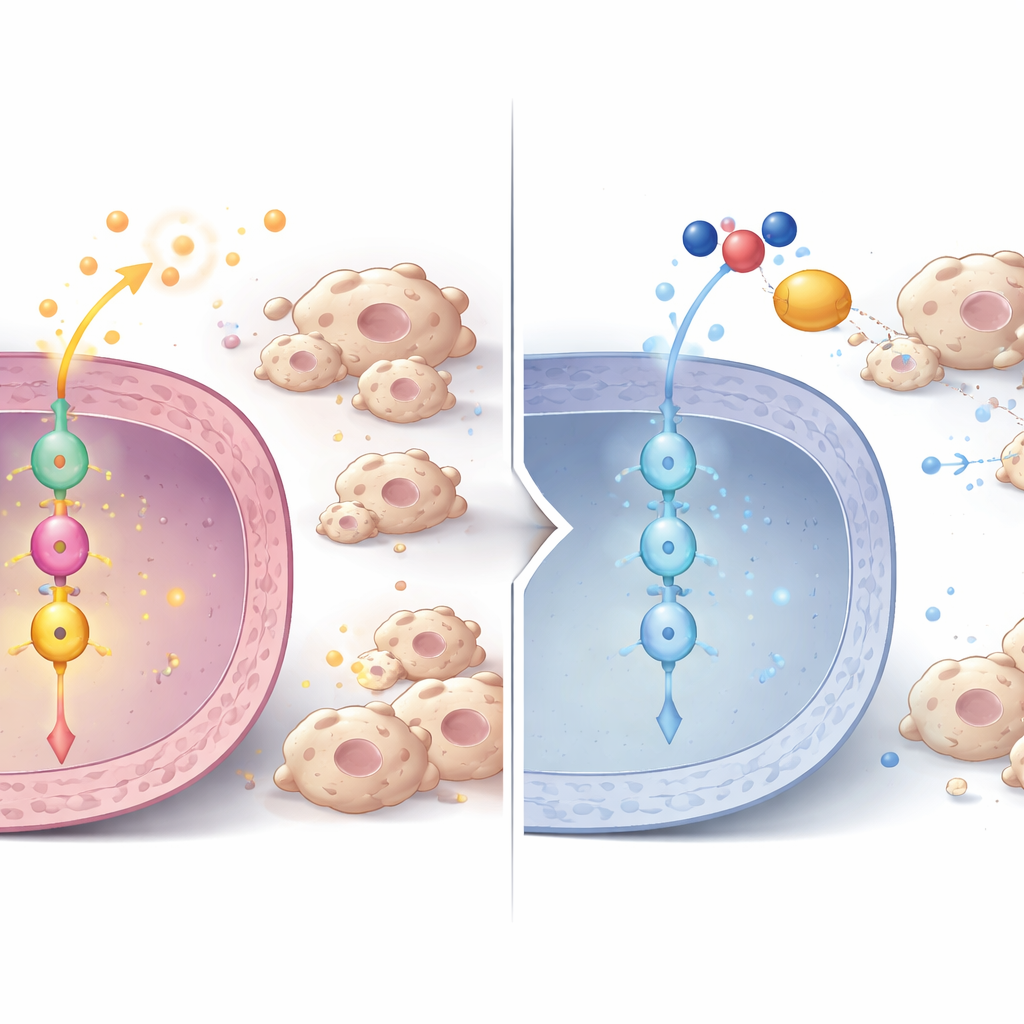
Una cadena de señalización desde P3H1 hasta la división celular y el control inmunitario
Al profundizar más, los investigadores descubrieron una cadena de señalización dentro de las células tumorales. Cuando P3H1 se redujo, los niveles de otra proteína, la quinasa Polo-like 1 (PLK1), cayeron tanto a nivel de proteína como de ARN, en células, tumores de ratón y muestras de pacientes. PLK1 es un regulador clave de la división celular y ya se sabe que está sobreactivada en muchos cánceres. Usando fosfoproteómica, el equipo mostró que la actividad de PLK1 normalmente potencia a un regulador central del cáncer llamado β-catenina modificándolo en un sitio específico necesario para su entrada al núcleo celular. En las células deficientes en P3H1, esta marca activadora en β-catenina disminuyó, su presencia nuclear se redujo y la expresión de los genes diana de β-catenina cayó. Esos dianas incluyen no solo impulsores del ciclo celular como c-Myc y Ciclinas D1, que empujan a las células a dividirse, sino también las propias citocinas que atraen a macrófagos que apoyan al tumor. Restaurar P3H1 o PLK1 en células carentes de P3H1 reactivó la actividad de β-catenina, la proliferación celular y el reclutamiento de macrófagos, lo que subraya que el eje P3H1–PLK1–β-catenina es un centro de control central.
Hacer que la quimioterapia sea más eficaz
Dado que la señalización de β-catenina y los macrófagos que favorecen al tumor se han implicado en la resistencia a la gemcitabina y a otros regímenes estándar, los autores preguntaron si bloquear este eje podría mejorar el tratamiento. Combinaron gemcitabina (y otros cócteles estándar) con un inhibidor de PLK1, BI2536, en ratones portadores de tumores pancreáticos humanos. A una dosis cuidadosamente seleccionada que evitó toxicidad orgánica, la combinación produjo tumores mucho más pequeños, menos células cancerosas en división y menos macrófagos asociados al tumor que la quimioterapia sola. Los organoides pancreáticos derivados de pacientes —mini-tumores cultivados a partir de muestras quirúrgicas— mostraron un patrón similar: reducir P3H1 frenó su crecimiento, bajó PLK1 y los hizo más vulnerables a gemcitabina más nab-paclitaxel, mientras que el inhibidor de PLK1 incrementó aún más la sensibilidad a los fármacos.
Qué significa esto para tratamientos futuros
En términos sencillos, este trabajo identifica un trío de moléculas —P3H1, PLK1 y β-catenina— que actúan como un pedal de acelerador para los tumores pancreáticos, impulsando tanto la división celular descontrolada como el reclutamiento de células inmunitarias que ayudan al cáncer en lugar de combatirlo. Deshabilitar este eje ralentiza el crecimiento tumoral y hace que la quimioterapia existente sea más efectiva en modelos de ratón y derivados de pacientes. Aunque aún no existen fármacos que bloqueen directamente P3H1, los inhibidores de PLK1 ya están en desarrollo, lo que plantea la posibilidad de que, en el futuro, combinarlos con la quimioterapia estándar pueda ofrecer a los pacientes con cáncer de páncreas un control más duradero de su enfermedad.
Cita: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
Palabras clave: cáncer de páncreas, microambiente tumoral, macrófagos, señalización de β-catenina, quimioterapia dirigida