Clear Sky Science · it
Inibire la prolil 3-idrossilasi 1 rallenta la progressione del cancro pancreatico e modifica l’immunità dei macrofagi
Perché questa ricerca è importante
Il cancro al pancreas è tra i più letali, spesso diagnosticato in fase avanzata e notoriamente resistente alle terapie. Questo studio indaga un “interruttore” molecolare nascosto che favorisce la crescita dei tumori pancreatici e la loro fuga dal controllo immunitario, e mostra come disattivarlo possa rallentare la malattia e rendere la chemioterapia convenzionale più efficace.
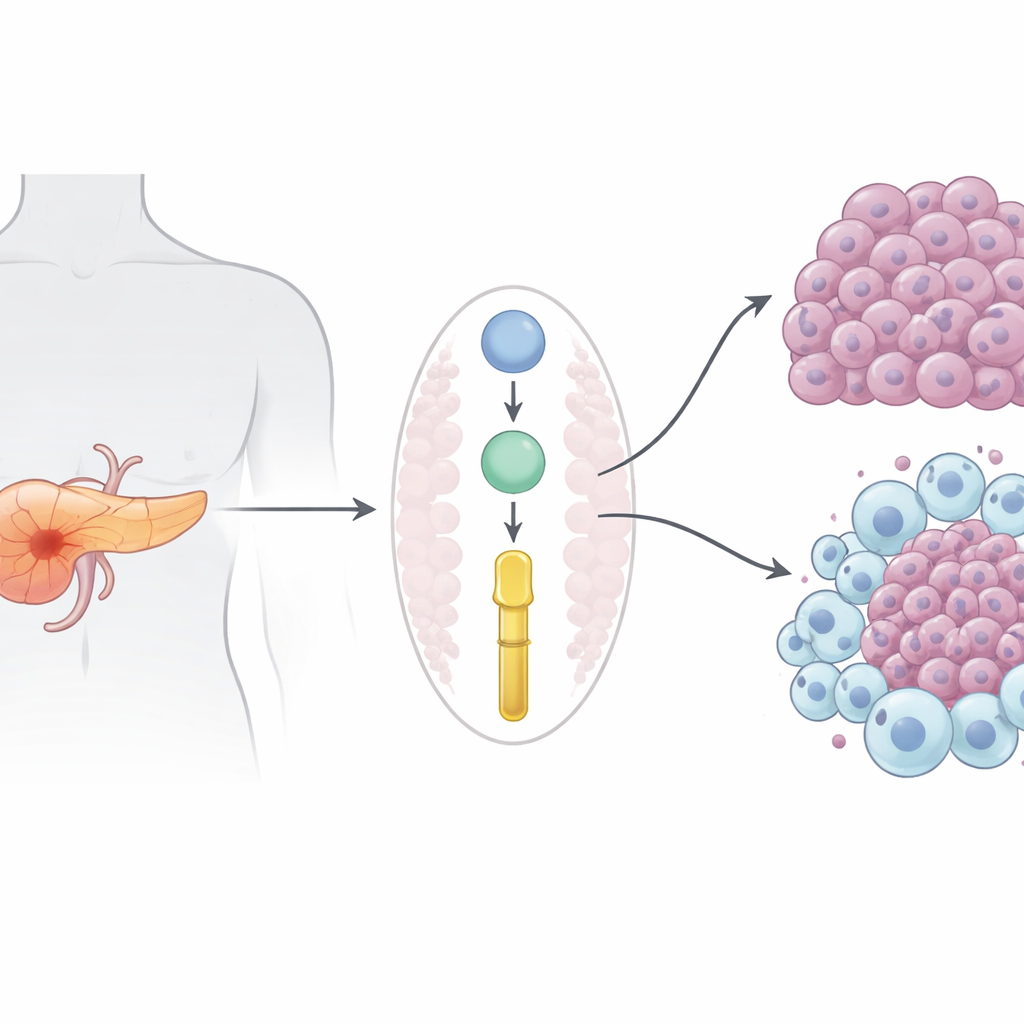
Un cancro letale con poche opzioni valide
L’adenocarcinoma duttale pancreatico, la forma più comune di cancro al pancreas, uccide quasi tante persone quante ne colpisce. Poiché viene in genere diagnosticato dopo che si è già diffuso, l’intervento chirurgico spesso non è possibile e farmaci come la gemcitabina offrono benefici modesti e di breve durata. Le immunoterapie moderne che hanno trasformato il trattamento di melanoma e tumore polmonare qui hanno fallito in larga parte, in parte perché i tumori pancreatici creano un ambiente immunologicamente “freddo” che esclude le cellule immunitarie utili e favorisce quelle che proteggono il cancro.
L’aiutante nascosto: un enzima del collagene fuori controllo
I ricercatori si sono concentrati sulle proteine secrete dalle cellule tumorali che potrebbero plasmare sia la crescita del cancro sia l’ambiente immunitario circostante. Rianalizzando ampi dataset proteomici di pazienti umani e di un modello murino consolidato, hanno individuato la prolil 3‑idrossilasi 1 (P3H1), un enzima noto soprattutto per modificare il collagene in ossa e pelle. In persone e topi i livelli di P3H1 erano molto più alti nei tumori pancreatici rispetto al pancreas sano, e i pazienti i cui tumori esprimevano maggiormente P3H1 tendevano a recidivare prima e a morire più precocemente. Importante, l’aumento di P3H1 era associato a malattia più estesa, suggerendo che non si limita a comparire insieme alla crescita tumorale ma contribuisce attivamente alla progressione.
Spegnere P3H1 rallenta i tumori e rimodella i macrofagi
Per verificare se P3H1 guidasse effettivamente il cancro, il team ha ingegnerizzato topi con cellule pancreatiche prive del gene P3H1, pur mantenendo le mutazioni classiche che normalmente producono tumori aggressivi. Questi topi privi di P3H1 hanno sviluppato tumori più piccoli, conservato più tessuto pancreatico normale e vissuto circa il 20% in più rispetto ai controlli con P3H1 intatto. Nei tumori murini e in linee cellulari umane coltivate in vitro, la perdita di P3H1 ha ridotto drasticamente la proliferazione delle cellule tumorali. Allo stesso tempo, i tumori privi di P3H1 contenevano molti meno macrofagi associati al tumore di tipo “M2”, cellule immunitarie che normalmente aiutano i tumori promuovendo crescita, formazione di vasi e resistenza ai farmaci. Le cellule tumorali con alto P3H1 secern evano livelli maggiori di tre proteine segnale (CXCL1, CXCL5 e CXCL8) che attraggono e riprogrammano i macrofagi; abbassare P3H1 ha diminuito questi segnali e attenuato il reclutamento e la polarizzazione dei macrofagi.
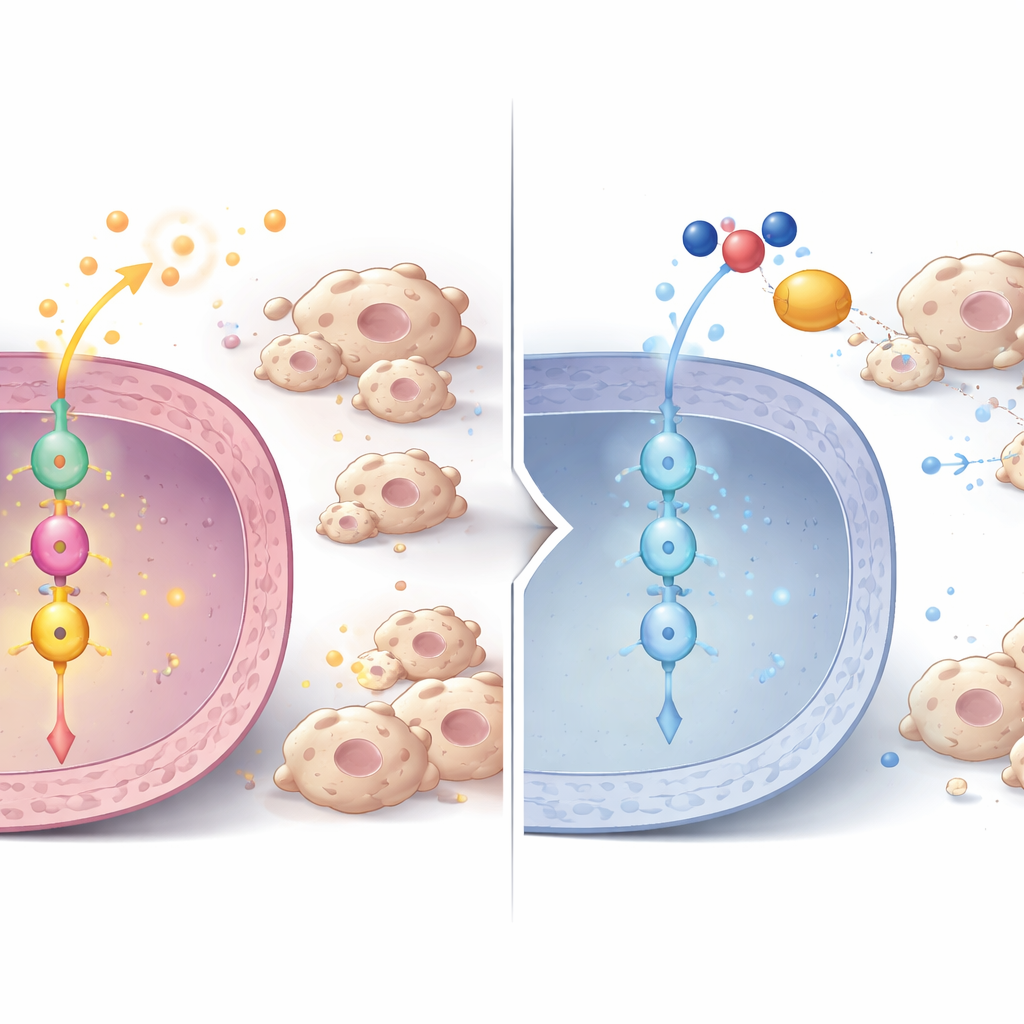
Una catena di segnalazione da P3H1 alla divisione cellulare e al controllo immunitario
Approfondendo, i ricercatori hanno scoperto una catena di segnalazione all’interno delle cellule tumorali. Quando P3H1 veniva ridotto, i livelli di un’altra proteina, la Polo‑like kinase 1 (PLK1), calavano sia a livello proteico sia a livello di RNA, in cellule, tumori murini e campioni di pazienti. PLK1 è un regolatore chiave della divisione cellulare ed è noto per essere iperattivo in molti tumori. Tramite fosfoproteomica, il team ha mostrato che l’attività di PLK1 normalmente potenzia un regolatore centrale del cancro chiamato β‑catenina modificandolo in un sito specifico necessario per l’ingresso nel nucleo cellulare. Nelle cellule prive di P3H1 questo marchio attivante sulla β‑catenina si riduceva, la sua presenza nucleare diminuiva e l’espressione dei geni target della β‑catenina calava. Questi target includono non solo driver del ciclo cellulare come c‑Myc e Cyclin D1, che spingono le cellule a dividersi, ma anche le stesse citochine che richiamano macrofagi che sostengono il tumore. Ripristinare P3H1 o PLK1 in cellule prive di P3H1 riattivava β‑catenina, la proliferazione tumorale e il reclutamento dei macrofagi, sottolineando che l’asse P3H1–PLK1–β‑catenina è un hub di controllo centrale.
Rendere la chemioterapia più efficace
Poiché la segnalazione della β‑catenina e i macrofagi che sostengono il tumore sono stati implicati nella resistenza alla gemcitabina e ad altri regimi standard, gli autori hanno testato se bloccare questo asse potesse migliorare la terapia. Hanno combinato gemcitabina (e altri cocktail standard) con un inibitore di PLK1, BI2536, in topi portatori di tumori pancreatici umani. A una dose accuratamente scelta per evitare tossicità d’organo, la combinazione ha prodotto tumori molto più piccoli, meno cellule tumorali in divisione e meno macrofagi associati al tumore rispetto alla sola chemioterapia. Organoidi pancreatici derivati da pazienti—mini‑tumori coltivati da campioni chirurgici—hanno mostrato un pattern simile: il knockdown di P3H1 ha rallentato la loro crescita, abbassato PLK1 e li ha resi più sensibili a gemcitabina più nab‑paclitaxel, mentre l’inibitore di PLK1 ha ulteriormente aumentato la sensibilità ai farmaci.
Cosa significa per i trattamenti futuri
In termini semplici, questo lavoro identifica un trio di molecole—P3H1, PLK1 e β‑catenina—that insieme funzionano come un pedale dell’acceleratore per i tumori pancreatici, promuovendo sia la divisione cellulare incontrollata sia il reclutamento di cellule immunitarie che aiutano il cancro anziché combatterlo. Disabilitare questo asse rallenta la crescita tumorale e rende la chemioterapia esistente più efficace in modelli murini e derivati da pazienti. Sebbene farmaci che bloccano direttamente P3H1 non siano ancora disponibili, gli inibitori di PLK1 sono già in sviluppo, aprendo la prospettiva che, in futuro, combinarli con la chemioterapia standard possa offrire ai pazienti con cancro pancreatico un controllo della malattia più duraturo.
Citazione: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
Parole chiave: cancro pancreatico, microambiente tumorale, macrofagi, segnalazione della β-catenina, chemioterapia mirata