Clear Sky Science · nl
Het remmen van prolyl 3-hydroxylase 1 remt de progressie van alvleesklierkanker en herstelt macrofaagimmuniteit
Waarom dit onderzoek ertoe doet
Alvleesklierkanker behoort tot de dodelijkste vormen van kanker: vaak wordt de ziekte laat ontdekt en is ze berucht ongevoelig voor behandeling. Deze studie onderzoekt een verborgen moleculaire “schakelaar” die alvleeskliertumoren helpt groeien en het immuunsysteem te ontwijken, en toont aan dat het uitzetten van die schakelaar de ziekte kan vertragen en standaardchemotherapie effectiever kan maken.
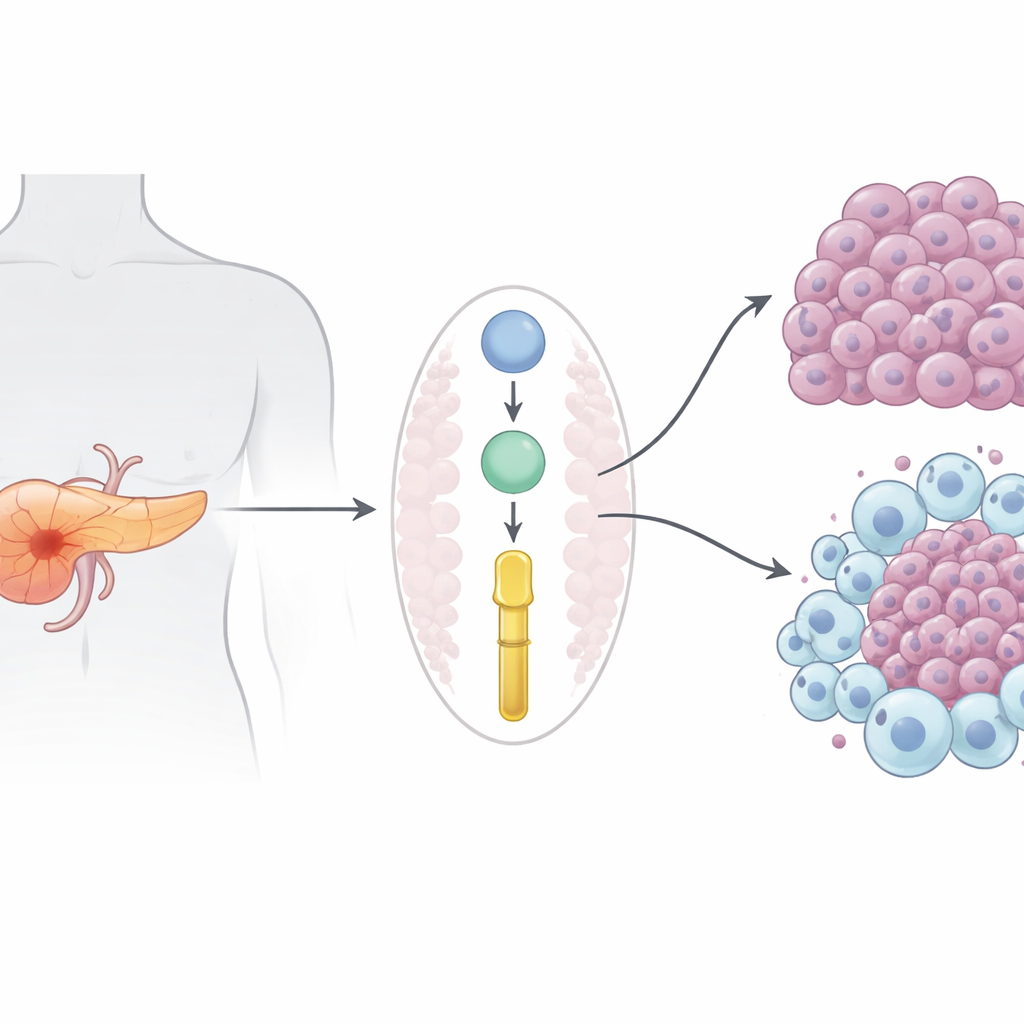
Een dodelijke kanker met weinig goede opties
Pancreasductaal adenocarcinoom, de meest voorkomende vorm van alvleesklierkanker, eist bijna evenveel levens als het aantal diagnoses. Omdat de ziekte meestal wordt vastgesteld nadat ze zich heeft uitgezaaid, is chirurgie vaak niet mogelijk, en geneesmiddelen zoals gemcitabine leveren slechts bescheiden en kortdurend voordeel. Moderne immunotherapieën die melanomen en longkanker hebben veranderd, faalden grotendeels bij deze kanker; deels omdat alvleeskliertumoren een immunologisch “koude” omgeving creëren die behulpzame immuuncellen buiten houdt en cellen koestert die de tumor beschermen.
De verborgen helper: een collageenenzym dat ontspoort
De onderzoekers richtten zich op eiwitten die door tumoren worden uitgescheiden en die zowel de kankergroei als de omliggende immuunomgeving zouden kunnen vormen. Door grote eiwitdatasets van menselijke patiënten en een goed onderzocht muismodel opnieuw te analyseren, identificeerden ze Prolyl 3-hydroxylase 1 (P3H1), een enzym dat vooral bekendstaat om het aanpassen van collageen in bot en huid. Zowel bij mensen als bij muizen werden P3H1-niveaus veel hoger gevonden in alvleeskliertumoren dan in gezond pancreas, en patiënten met tumoren met meer P3H1 kregen eerder een terugval en overleden eerder. Belangrijk is dat verhoogde P3H1 gekoppeld was aan uitgebreidere ziekte, wat suggereert dat het meer doet dan alleen met tumorgroei gepaard gaan.
Het uitschakelen van P3H1 vertraagt tumoren en herformeert immuuncellen
Om te testen of P3H1 daadwerkelijk kanker aanjaagt, maakten de onderzoekers muizen waarin pancreascellen het P3H1-gen misten, terwijl ze nog steeds de klassieke kankerveroorzakende mutaties droegen die normaal agressieve tumoren geven. Deze P3H1-deficiënte muizen ontwikkelden kleinere tumoren, behielden meer normaal pancreasweefsel en leefden ongeveer 20% langer dan hun tegenhangers met intacte P3H1. In zowel muizen tumoren als menselijke kankercellijnen in het laboratorium verminderde het verlies van P3H1 sterk de proliferatie van kankercellen. Tegelijkertijd bevatten tumoren zonder P3H1 veel minder “M2-achtige” tumorgeassocieerde macrofagen — immuuncellen die normaal gesproken tumoren helpen door groei, bloedvatvorming en medicijnresistentie te bevorderen. De kankercellen met hoge P3H1 scheidden meer van drie signaalproteïnen uit (CXCL1, CXCL5 en CXCL8) die macrofagen aantrekken en herprogrammeren; het terugschakelen van P3H1 verlaagde deze signalen en dempte zowel macrofaagrecruitment als polarizatie.
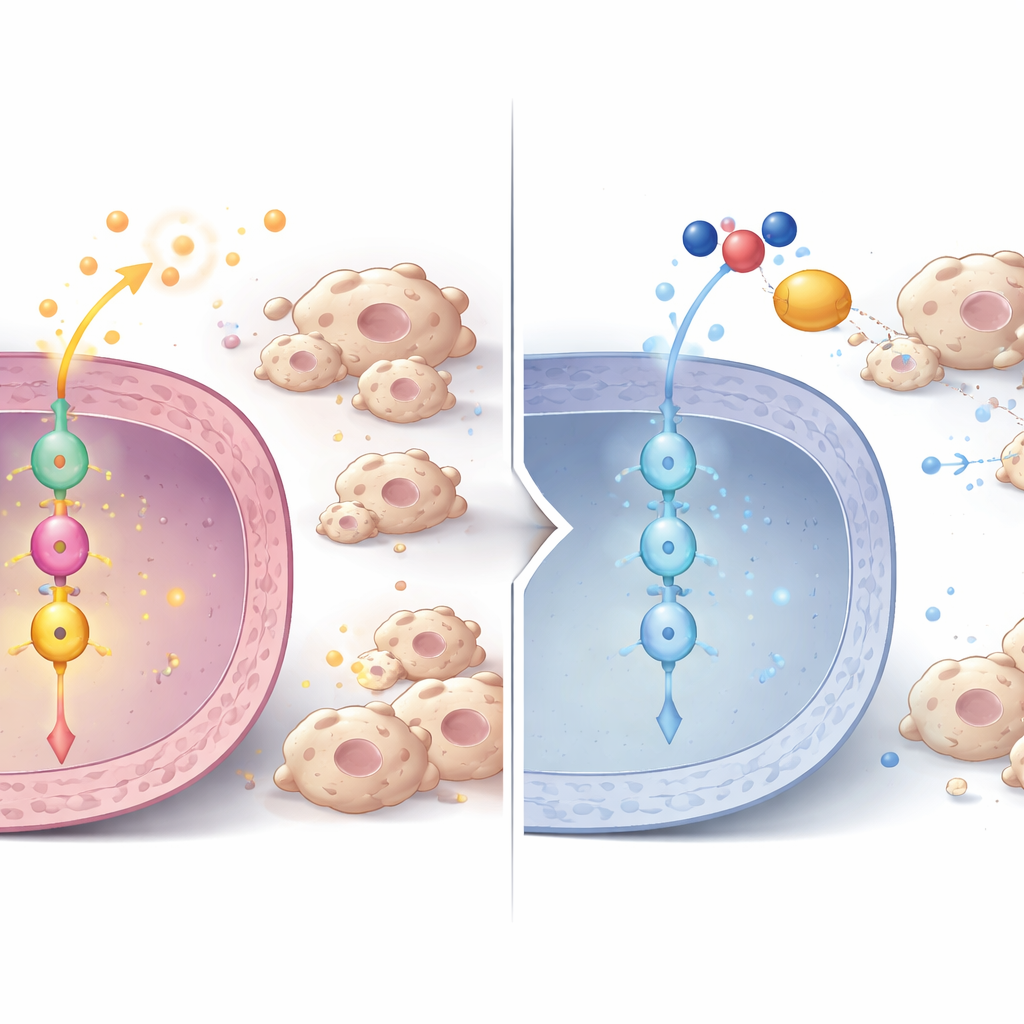
Een signaleringsketen van P3H1 naar celdeling en immuuncontrole
Dieper gravend ontdekten de onderzoekers een signaalketen binnen tumorcellen. Wanneer P3H1 werd verminderd, daalden de niveaus van een ander eiwit, Polo-like kinase 1 (PLK1), zowel op eiwit- als op RNA-niveau, in cellen, muizentumoren en patiëntmonsters. PLK1 is een sleutelregulator van celdeling en staat bekend als overactief in veel kankers. Met behulp van fosfoproteomica toonden ze aan dat PLK1-activiteit normaal gesproken een centrale kankerregulator, β-catenine, versterkt door het op een specifieke plaats te modificeren die nodig is voor de insluiting in de celkern. In P3H1-deficiënte cellen nam dit activerende merkteken op β-catenine af, verminderde zijn aanwezigheid in de kern en daalde de expressie van β-cateninetargetgenen. Die targets omvatten niet alleen celcyclusdrijvers zoals c-Myc en Cyclin D1, die celdeling stimuleren, maar ook de cytokines die tumorondersteunende macrofagen aantrekken. Het herstellen van P3H1 of PLK1 in P3H1-deficiënte cellen bracht β-catenine-activiteit, kankercelproliferatie en macrofaagrecruitment terug, wat benadrukt dat de P3H1–PLK1–β-catenine-as een centraal regelpunt is.
De chemotherapie harder laten toeslaan
Aangezien β-catenine-signaleringsroutes en tumorondersteunende macrofagen beide zijn gekoppeld aan resistentie tegen gemcitabine en andere standaardregimes, vroegen de auteurs zich af of blokkeren van deze as de behandeling kon verbeteren. Ze combineerden gemcitabine (en andere standaardcocktails) met een PLK1-remmer, BI2536, in muizen met menselijke alvleeskliertumoren. Bij een zorgvuldig gekozen dosis die orgaantoxiciteit vermijdt, leverde de combinatie veel kleinere tumoren, minder delende kankercellen en minder tumorgeassocieerde macrofagen op dan chemotherapie alleen. Patiënt-afgeleide pancreas-organoïden — mini-tumoren gekweekt uit chirurgische monsters — lieten een vergelijkbaar patroon zien: het onderdrukken van P3H1 vertraagde hun groei, verlaagde PLK1 en maakte ze kwetsbaarder voor gemcitabine plus nab-paclitaxel, terwijl de PLK1-remmer de geneesmiddelgevoeligheid verder verhoogde.
Wat dit betekent voor toekomstige behandeling
In eenvoudige bewoordingen identificeert dit werk een trio van moleculen — P3H1, PLK1 en β-catenine — die samen als een gaspedaal voor alvleeskliertumoren fungeren, zowel door ongecontroleerde celdeling te stimuleren als door immuuncellen aan te trekken die de kanker eerder helpen dan bestrijden. Het uitschakelen van deze as vertraagt tumorgroei en maakt bestaande chemotherapie effectiever in muizen en patiëntafgeleide modellen. Hoewel er nog geen geneesmiddelen bestaan die P3H1 direct blokkeren, zijn PLK1-remmers al in ontwikkeling, wat het vooruitzicht opent dat het combineren ervan met standaardchemotherapie in de toekomst patiënten met alvleesklierkanker betere en duurzamere controle over hun ziekte kan bieden.
Bronvermelding: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
Trefwoorden: alvleesklierkanker, tumormicro-omgeving, macrofagen, β-catenine signalering, gerichte chemotherapie