Clear Sky Science · pt
Alvo na Prolil 3-hidroxilase 1 inibe a progressão do câncer de pâncreas e a imunidade de macrófagos
Por que esta pesquisa importa
O câncer de pâncreas está entre os tumores mais letais, frequentemente detectado tardiamente e notoriamente resistente ao tratamento. Este estudo explora um “interruptor” molecular oculto que ajuda os tumores pancreáticos a crescerem e a escaparem do sistema imunológico, e mostra como desligar esse interruptor pode retardar a doença e tornar a quimioterapia padrão mais eficaz.
Um câncer letal com poucas opções eficazes
Adenocarcinoma ductal pancreático, a forma mais comum de câncer de pâncreas, mata quase tantos quanto acomete. Como geralmente é diagnosticado depois de já ter se espalhado, a cirurgia muitas vezes não é possível, e fármacos como a gemcitabina oferecem benefício modesto e de curta duração. Imunoterapias modernas que transformaram o tratamento do melanoma e do câncer de pulmão falharam em grande parte aqui, em parte porque os tumores pancreáticos criam um ambiente imunologicamente “frio” que mantém fora células imunes úteis e nutre células que protegem o câncer.
O ajudante oculto: uma enzima do colágeno fora de controle
Os pesquisadores focaram em proteínas secretadas pelas células tumorais que poderiam moldar tanto o crescimento do câncer quanto o ambiente imune ao redor. Ao reanalisar grandes conjuntos de dados proteômicos de pacientes humanos e de um modelo murino bem estabelecido, eles identificaram a Prolil 3-hidroxilase 1 (P3H1), uma enzima mais conhecida por modificar o colágeno em osso e pele. Em humanos e camundongos, os níveis de P3H1 foram muito maiores em tumores pancreáticos do que no pâncreas saudável, e pacientes cujos tumores tinham mais P3H1 tenderam a recidivar mais cedo e a morrer mais rapidamente. Importante, o aumento de P3H1 esteve ligado a doença mais extensa, sugerindo que ela faz mais do que apenas acompanhar o crescimento tumoral.
Inibir a P3H1 freia tumores e remodela células imunes
Para testar se a P3H1 realmente impulsiona o câncer, a equipe gerou camundongos cujas células pancreáticas não possuíam o gene P3H1, mantendo, contudo, as mutações oncogênicas clássicas que normalmente produzem tumores agressivos. Esses camundongos deficientes em P3H1 desenvolveram tumores menores, conservaram mais tecido pancreático normal e viveram cerca de 20% mais que os equivalentes com P3H1 intacta. Tanto em tumores de camundongo quanto em linhas celulares humanas cultivadas em laboratório, a perda de P3H1 reduziu fortemente a proliferação celular tumoral. Ao mesmo tempo, tumores sem P3H1 continham muito menos macrófagos associados ao tumor do tipo “M2” — células imunes que normalmente ajudam os tumores promovendo crescimento, formação de vasos sanguíneos e resistência a medicamentos. As células cancerígenas com alto P3H1 secretaram mais de três proteínas sinalizadoras (CXCL1, CXCL5 e CXCL8) que atraem e reprogramam macrófagos; reduzir a P3H1 diminuiu esses sinais e enfraqueceu o recrutamento e a polarização dos macrófagos.
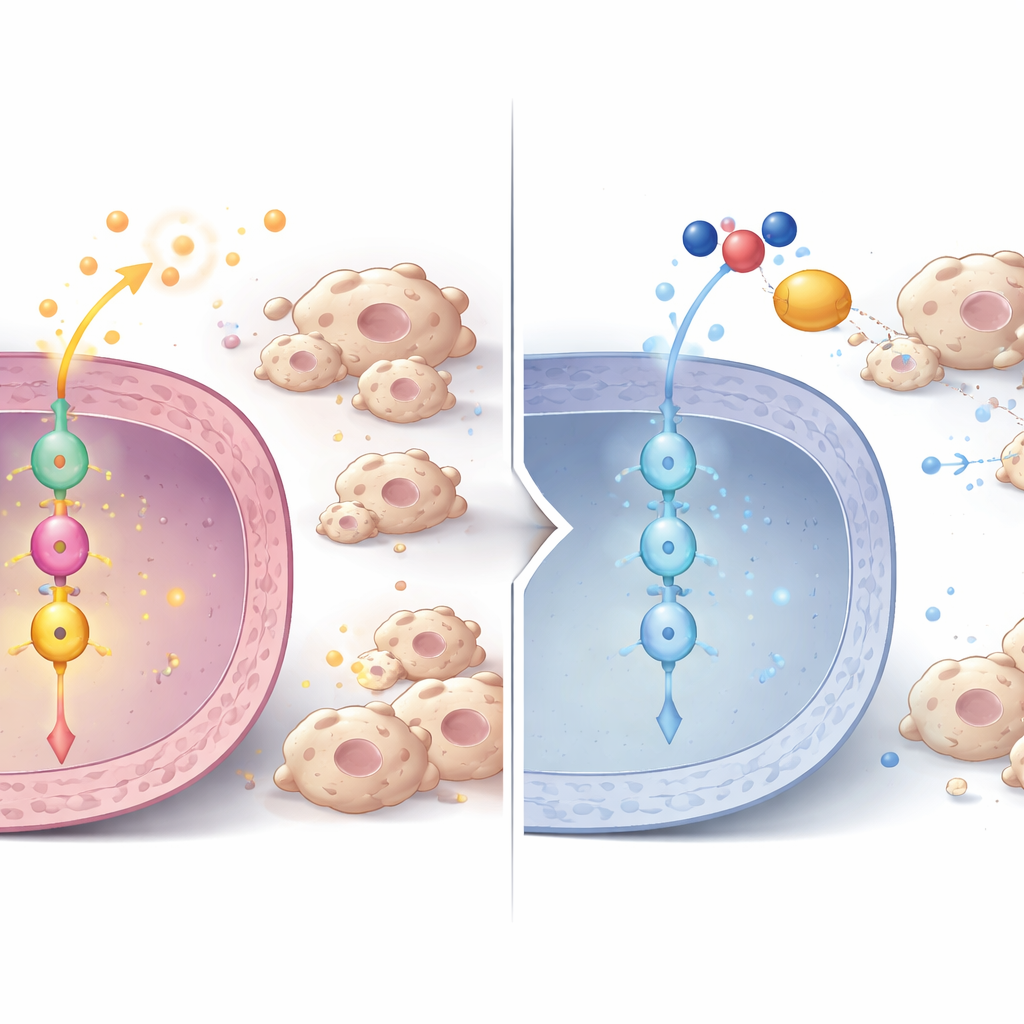
Uma cadeia de sinalização da P3H1 à divisão celular e ao controle imune
Investigando mais a fundo, os pesquisadores descobriram uma cadeia de sinalização dentro das células tumorais. Quando a P3H1 foi reduzida, os níveis de outra proteína, Polo-like kinase 1 (PLK1), caíram tanto na proteína quanto no RNA, em células, tumores de camundongo e amostras de pacientes. A PLK1 é um regulador chave da divisão celular e já se sabe que está hiperativa em muitos cânceres. Usando fosfoproteômica, a equipe mostrou que a atividade da PLK1 normalmente aumenta um regulador central do câncer chamado β-catenina ao modificá-lo em um sítio específico necessário para sua entrada no núcleo celular. Em células deficientes em P3H1, essa marca ativadora na β-catenina diminuiu, sua presença nuclear enfraqueceu e a expressão de genes alvos da β-catenina caiu. Esses alvos incluem não apenas condutores do ciclo celular como c-Myc e Ciclo D1, que impulsionam a divisão celular, mas também as próprias citocinas que atraem macrófagos que apoiam o tumor. Restaurar P3H1 ou PLK1 em células deficientes em P3H1 reativou a atividade da β-catenina, a proliferação das células cancerígenas e o recrutamento de macrófagos, ressaltando que o eixo P3H1–PLK1–β-catenina é um centro de controle central.
Tornando a quimioterapia mais eficaz
Como a sinalização da β-catenina e os macrófagos que apoiam tumores foram implicados na resistência à gemcitabina e a outros regimes padrão, os autores perguntaram se bloquear esse eixo poderia melhorar o tratamento. Eles combinaram gemcitabina (e outros coquetéis padrão) com um inibidor de PLK1, BI2536, em camundongos portadores de tumores pancreáticos humanos. Em uma dose criteriosamente escolhida que evitou toxicidade aos órgãos, a combinação produziu tumores muito menores, menos células cancerígenas em divisão e menos macrófagos associados ao tumor do que a quimioterapia isolada. Organoides pancreáticos derivados de pacientes — mini-tumores cultivados a partir de amostras cirúrgicas — mostraram padrão semelhante: redução de P3H1 retardou seu crescimento, diminuiu PLK1 e os deixou mais vulneráveis à gemcitabina mais nab-paclitaxel, enquanto o inibidor de PLK1 aumentou ainda mais a sensibilidade ao medicamento.
O que isso significa para tratamentos futuros
De forma simples, este trabalho identifica um trio de moléculas — P3H1, PLK1 e β-catenina — que, juntas, atuam como um pedal de aceleração para tumores pancreáticos, impulsionando tanto a divisão celular descontrolada quanto o recrutamento de células imunes que ajudam o câncer em vez de combatê-lo. Desabilitar esse eixo retarda o crescimento tumoral e torna a quimioterapia existente mais eficaz em modelos murinos e derivados de pacientes. Embora fármacos que bloqueiem diretamente a P3H1 ainda não existam, inibidores de PLK1 já estão em desenvolvimento, o que levanta a perspectiva de que, no futuro, combiná-los com a quimioterapia padrão possa oferecer aos pacientes com câncer de pâncreas um controle mais duradouro da doença.
Citação: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
Palavras-chave: câncer de pâncreas, microambiente tumoral, macrófagos, sinalização β-catenina, quimioterapia direcionada