Clear Sky Science · de
Zielgerichtete Hemmung von Prolyl-3‑Hydroxylase‑1 hemmt das Fortschreiten von Bauchspeicheldrüsenkrebs und die Makrophagen‑Immunität
Warum diese Forschung wichtig ist
Bauchspeicheldrüsenkrebs zählt zu den tödlichsten Krebsarten: Er wird häufig spät erkannt und ist berüchtigt für seine Therapieresistenz. Diese Studie untersucht einen verborgenen molekularen „Schalter“, der dem Tumorwachstum und der Immunflucht Vorschub leistet, und zeigt, wie das Ausschalten dieses Schalters das Fortschreiten verlangsamen und Standardchemotherapien wirksamer machen kann.
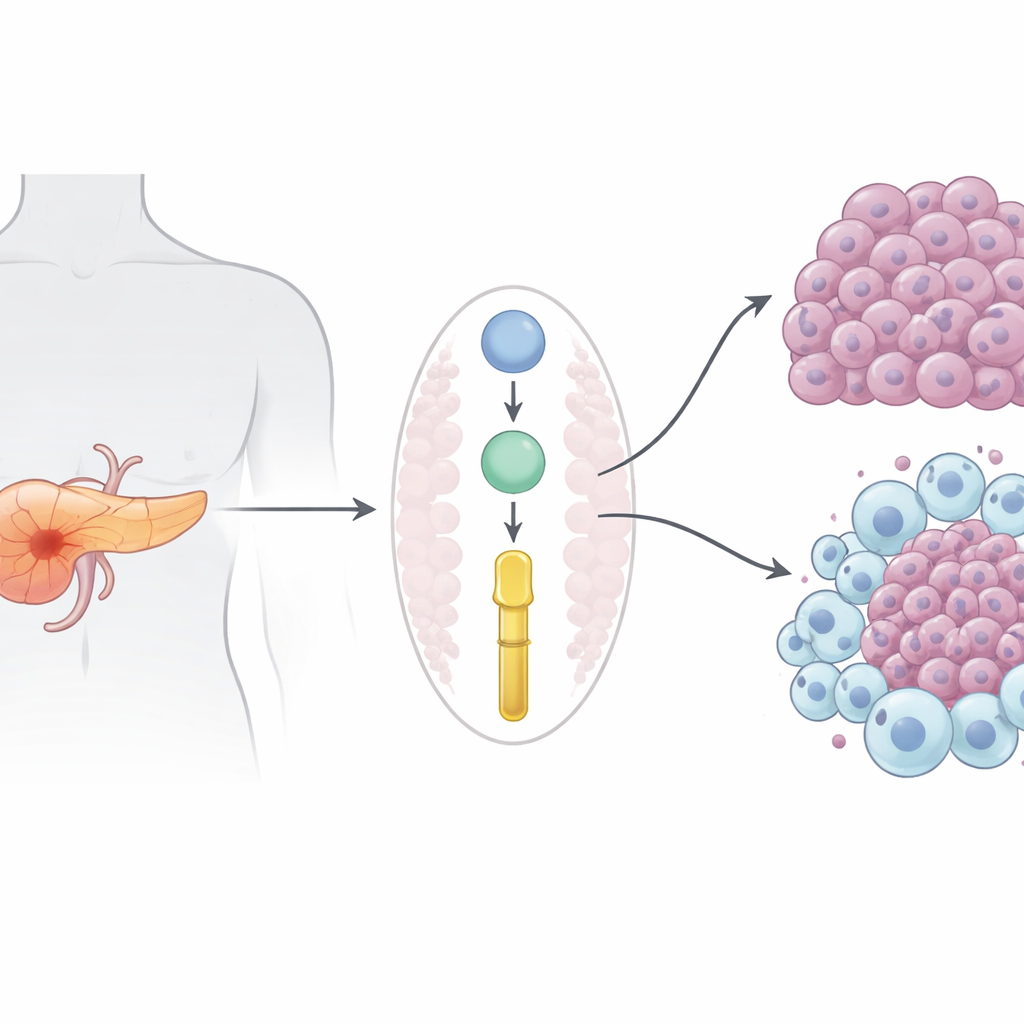
Eine tödliche Krebsart mit wenigen guten Optionen
Das duktale Adenokarzinom der Bauchspeicheldrüse, die häufigste Form des Bauchspeicheldrüsenkrebses, fordert fast genauso viele Todesopfer wie Erkrankte. Da es meist erst nach Metastasierung diagnostiziert wird, kommt eine Operation oft nicht in Frage, und Medikamente wie Gemcitabin erzielen nur geringe und kurzlebige Vorteile. Moderne Immuntherapien, die Melanom und Lungenkrebs revolutioniert haben, versagen hier weitgehend — unter anderem weil Pankreastumoren eine immunologisch „kalte“ Umgebung schaffen, die schützende Immunzelltypen fernhält und Zellen fördert, die den Tumor unterstützen.
Der verborgene Helfer: ein entgleistes Kollagen‑Enzym
Die Forschenden konzentrierten sich auf von Tumorzellen sezernierte Proteine, die sowohl das Krebswachstum als auch das umgebende Immunmilieu beeinflussen könnten. Durch die Neuanalyse großer Proteindatensätze von Patient:innen und einem etablierten Mausmodell identifizierten sie Prolyl‑3‑Hydroxylase‑1 (P3H1), ein Enzym, das vor allem dafür bekannt ist, Kollagen in Knochen und Haut zu modifizieren. In Mensch und Maus fanden sich in Pankreastumoren deutlich höhere P3H1‑Spiegel als im gesunden Pankreas; Patient:innen mit höheren Tumor‑P3H1‑Werten litten zudem früher Rezidive und hatten kürzere Überlebenszeiten. Wichtig ist, dass erhöhte P3H1‑Werte mit ausgeprägterer Erkrankung einhergingen, was darauf hindeutet, dass P3H1 mehr ist als nur ein Begleiter des Tumorwachstums.
P3H1 auszuschalten verlangsamt Tumoren und verändert Immunzellen
Um zu prüfen, ob P3H1 tatsächlich treibend wirkt, erzeugte das Team Mäuse, deren Pankreaszellen kein P3H1 mehr exprimierten, während gleichzeitig die klassischen krebsauslösenden Mutationen vorhanden blieben, die sonst aggressive Tumoren hervorrufen. Diese P3H1‑defizienten Mäuse entwickelten kleinere Tumoren, bewahrten mehr normales Pankreasgewebe und lebten etwa 20 % länger als ihre Altersgenossen mit intaktem P3H1. Sowohl in Mäusetumoren als auch in humanen Krebszelllinien im Labor führte der Verlust von P3H1 zu einem starken Rückgang der Tumorzellproliferation. Gleichzeitig enthielten Tumoren ohne P3H1 deutlich weniger „M2‑ähnliche“ tumorassoziierte Makrophagen — Immunzellen, die Tumoren normalerweise unterstützen, indem sie Wachstum, Angiogenese und Medikamentenresistenz fördern. Die Krebszellen mit hohem P3H1 sezernierten mehr von drei Signalproteinen (CXCL1, CXCL5 und CXCL8), die Makrophagen anziehen und umprogrammieren; die Herunterregulierung von P3H1 verringerte diese Signale und schwächte Makrophagen‑Rekrutierung und ‑Polarisation ab.
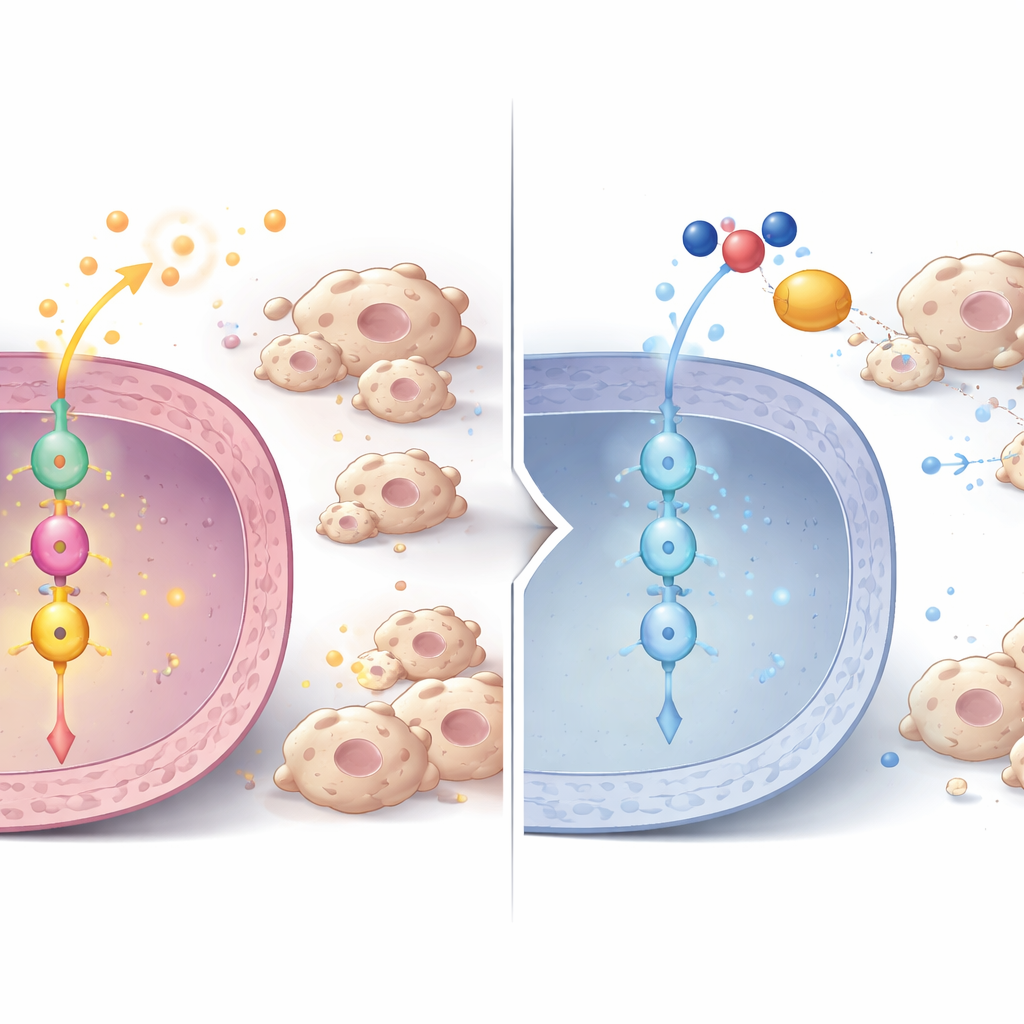
Eine Signal‑Kette von P3H1 zu Zellteilung und Immunsteuerung
Bei genauerer Untersuchung entdeckten die Forschenden eine Signalkette innerhalb der Tumorzellen. Nach Reduktion von P3H1 sanken die Spiegel eines weiteren Proteins, Polo‑like‑Kinase 1 (PLK1), sowohl auf Proteinebene als auch auf RNA‑Ebene — in Zellen, Mäusetumoren und Patientenproben. PLK1 ist ein Schlüsselregulator der Zellteilung und bereits in vielen Krebsarten überaktiv. Mithilfe von Phosphoproteomik zeigten die Autor:innen, dass PLK1 normalerwiese einen zentralen Krebsregulator, β‑Catenin, durch Modifikation an einer spezifischen Stelle aktiviert, die für dessen Eintritt in den Zellkern notwendig ist. In P3H1‑defizienten Zellen nahm diese aktivierende Markierung auf β‑Catenin ab, seine nukleäre Präsenz schwand und die Expression von β‑Catenin‑Zielgenen fiel. Zu diesen Zielgenen gehören nicht nur Zellzyklus‑Treiber wie c‑Myc und Cyclin D1, die die Zellteilung vorantreiben, sondern auch die Zytokine, die tumorunterstützende Makrophagen anziehen. Die Wiederherstellung von P3H1 oder PLK1 in P3H1‑defizienten Zellen belebte β‑Catenin‑Aktivität, Tumorzellproliferation und Makrophagenrekrutierung erneut — ein Hinweis darauf, dass die P3H1–PLK1–β‑Catenin‑Achse ein zentrales Steuerungszentrum darstellt.
Chemotherapie wirksamer machen
Da β‑Catenin‑Signalgebung und tumorunterstützende Makrophagen beide mit Resistenz gegen Gemcitabin und andere Standardregime in Verbindung gebracht wurden, fragten die Autor:innen, ob die Blockade dieser Achse die Therapie verbessern könnte. Sie kombinierten Gemcitabin (und andere Standardcocktails) mit einem PLK1‑Inhibitor, BI2536, in Mäusen mit humanen Pankreastumoren. In einer sorgfältig gewählten Dosis, die Organtoxizität vermied, führte die Kombination zu deutlich kleineren Tumoren, weniger teilenden Krebszellen und weniger tumorassoziierten Makrophagen als die Chemotherapie allein. Aus Patienten gewonnene Pankreas‑Organoide — Mini‑Tumoren, die aus Operationsproben gezüchtet wurden — zeigten ein ähnliches Muster: Die Herunterregulierung von P3H1 verlangsamte ihr Wachstum, senkte PLK1 und machte sie anfälliger für Gemcitabin plus Nab‑Paclitaxel; der PLK1‑Inhibitor verstärkte zusätzlich die Arzneimittelwirkung.
Was das für die künftige Behandlung bedeutet
Vereinfacht gesagt, identifiziert diese Arbeit ein Trio von Molekülen — P3H1, PLK1 und β‑Catenin — das zusammen wie ein Gaspedal für Pankreastumoren wirkt, indem es sowohl die unkontrollierte Zellteilung als auch die Rekrutierung von Immunzellen antreibt, die dem Krebs eher nützen als schaden. Das Ausschalten dieser Achse verlangsamt das Tumorwachstum und macht bestehende Chemotherapien in Mäusen und patienten‑abgeleiteten Modellen wirksamer. Obwohl Wirkstoffe, die direkt P3H1 blockieren, noch nicht existieren, befinden sich PLK1‑Inhibitoren bereits in der Entwicklung, was die Aussicht eröffnet, dass eine Kombination mit Standardchemotherapie künftig eine dauerhaftere Kontrolle der Erkrankung für Patient:innen mit Bauchspeicheldrüsenkrebs ermöglichen könnte.
Zitation: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
Schlüsselwörter: Bauchspeicheldrüsenkrebs, tumoröses Mikroenvironment, Makrophagen, β‑Catenin‑Signalgebung, gezielte Chemotherapie