Clear Sky Science · ar
استهداف بْرُوليل 3-هيدروكسيلاز 1 يثبط تقدم سرطان البنكرياس والمناعة المعتمدة على البلاعم
لماذا يهم هذا البحث
يعد سرطان البنكرياس من أكثر السرطانات فتكًا، غالبًا ما يُكتشف متأخرًا ومقاومًا للعلاج بشكل ملحوظ. يستكشف هذا البحث "مفتاحًا" جزيئيًا مخفيًا يساعد أورام البنكرياس على النمو والتهرب من الجهاز المناعي، ويُظهر كيف أن تعطيل هذا المفتاح يمكن أن يبطئ المرض ويجعل العلاج الكيميائي التقليدي أكثر فعالية.
سرطان قاتل وخيارات محدودة
سرطان الغدد القنوية للبنكرياس، الشكل الأكثر شيوعًا لسرطان البنكرياس، يودي بحياة عدد يقارب عدد المصابين به. وبما أنه يُشخَّص في الغالب بعد أن يكون قد انتشر، غالبًا ما تكون الجراحة غير ممكنة، وتعطي أدوية مثل جيمسيتابين فوائد محدودة ومؤقتة فقط. لقد فشلت العلاجات المناعية الحديثة التي غيّرت نتاج الميلانوما وسرطان الرئة إلى حد كبير هنا، جزئيًا لأن أورام البنكرياس تخلق بيئة مناعية "باردة" تحجب الخلايا المناعية المفيدة وتدعم الخلايا التي تحمي السرطان.
المساعد الخفي: إنزيم كولاجين يتحول إلى عامل ضار
ركز الباحثون على البروتينات التي تفرزها خلايا الورم والتي قد تشكّل نمو السرطان والبيئة المناعية المحيطة به. من خلال إعادة تحليل مجموعات بيانات بروتينية كبيرة من مرضى بشريين ونموذج فأري راسخ، حددوا إنزيم برُوليل 3-هيدروكسيلاز 1 (P3H1)، وهو إنزيم معروف بشكل رئيسي بتعديله للكولاجين في العظام والجلد. في كل من البشر والفئران، كانت مستويات P3H1 أعلى بكثير في أورام البنكرياس مقارنةً بالبنكرياس السليم، وكان المرضى الذين تحتوي أورامهم على مستويات أعلى من P3H1 يميلون إلى الانتكاس مبكرًا والوفاة في وقت أبكر. والأهم أن ارتفاع P3H1 ارتبط بمرض أوسع انتشارًا، مما يشير إلى أنه doet أكثر من مصاحبة نمو الورم فحسب.
إيقاف P3H1 يبطئ الأورام ويعيد تشكيل الخلايا المناعية
لاختبار ما إذا كان P3H1 يدفع السرطان فعلًا، صمّم الفريق فئرانًا بحيث تفتقر خلايا البنكرياس لديها إلى جين P3H1، بينما تحمل في الوقت نفسه الطفرات المسببة للسرطان التي عادة ما تولد أورامًا عدوانية. طورت هذه الفئران الخالية من P3H1 أورامًا أصغر، واحتفظت بنسيج بنكرياسي أكثر طبيعية، وعاشت حوالي 20% أطول من نظرائها الذين لديهم P3H1 سليم. في كل من أورام الفئران وخطوط خلايا السرطان البشرية المزروعة في المختبر، أدى فقدان P3H1 إلى تقليل حاد في تكاثر خلايا الورم. في الوقت نفسه، احتوت الأورام التي تفتقر إلى P3H1 على عدد أقل بكثير من البلاعم المرتبطة بالأورام من النوع "M2"—وهي خلايا مناعية عادةً ما تساعد الأورام من خلال تعزيز النمو وتكوين الأوعية الدموية ومقاومة الأدوية. أفرزت خلايا السرطان ذات مستويات P3H1 العالية المزيد من ثلاث بروتينات إشارية (CXCL1 وCXCL5 وCXCL8) التي تجذب البلاعم وتعيد برمجتها؛ وخفض P3H1 قلل هذه الإشارات وكبح تجنيد البلاعم واستقطابها.
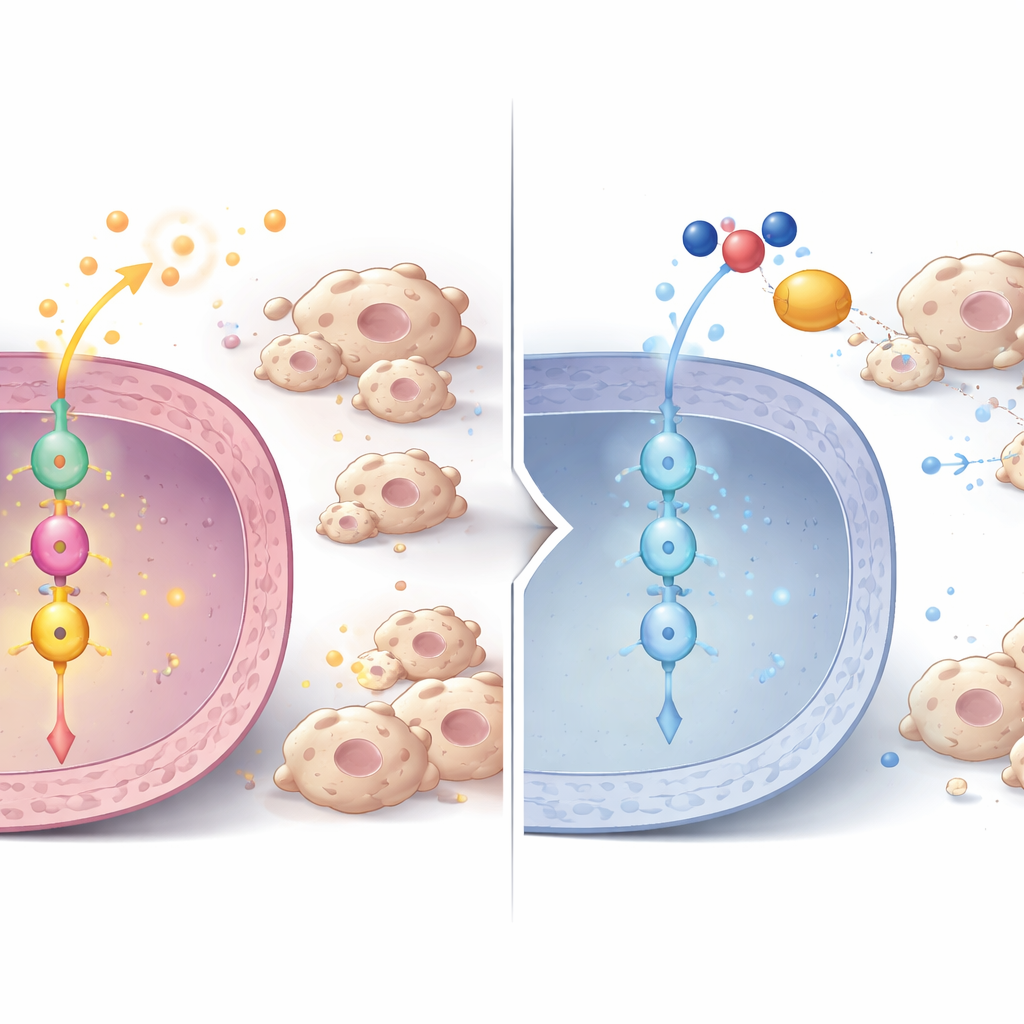
سلسلة إشارية من P3H1 إلى انقسام الخلايا والسيطرة المناعية
بتعمق أكبر، كشف الباحثون سلسلة إشارية داخل خلايا الورم. عندما انخفض P3H1، تراجعت مستويات بروتين آخر، كيناز بولو-لايك 1 (PLK1)، على مستوى البروتين والـRNA، في الخلايا وأورام الفئران وعينات المرضى. يعد PLK1 منظمًا رئيسيًّا لانقسام الخلايا ومعروفًا بفرْطه في النشاط في العديد من السرطانات. باستخدام فسفوبروتيوميك، أظهر الفريق أن نشاط PLK1 يعزز عادةً منظّمًا مركزيًا للسرطان يُدعى β-كاتينين عن طريق تعديله عند موقع محدد مطلوب لدخوله إلى نواة الخلية. في الخلايا الناقصة لـP3H1، انخفضت هذه العلامة المنشِّطة على β-كاتينين، وتناقص وجوده النووي، وتراجع تعبير جينات أهداف β-كاتينين. تشمل هذه الأهداف ليس فقط محفزات دورة الخلية مثل c-Myc وCyclin D1 التي تدفع الخلايا إلى الانقسام، بل أيضًا السيتوكينات نفسها التي تجذب البلاعم الداعمة للورم. إن إعادة تعبئة P3H1 أو PLK1 في الخلايا الخالية من P3H1 أعادت نشاط β-كاتينين وتكاثر خلايا السرطان وتجنيد البلاعم، مما يؤكد أن محور P3H1–PLK1–β-كاتينين هو محور تحكم مركزي.
جعل العلاج الكيميائي أكثر فاعلية
نظرًا لأن إشارة β-كاتينين والبلاعم الداعمة للورم متورطة في مقاومة الجيمسيتابين والأنظمة القياسية الأخرى، تساءل المؤلفون عما إذا كان حجب هذا المحور يمكن أن يحسن العلاج. جمعوا بين جيمسيتابين (ومجموعات معيارية أخرى) ومثبط PLK1 يدعى BI2536 في فئران حاملة لأورام بنكرياس بشرية. عند جرعة مختارة بعناية لتجنب سمية الأعضاء، أنتج المزيج أورامًا أصغر بكثير، وخلايا سرطانية أقل انقسامًا، وبلاعم مرتبطة بالأورام أقل من العلاج الكيميائي وحده. أظهرت العضويات البنكرياسية المستمدة من المرضى—أورام مصغرة نمت من عينات جراحية—نمطًا مشابهًا: أدت خفضـP3H1 إلى إبطاء نموها، وخفضت PLK1، وجعلتها أكثر عرضة للجيمسيتابين مع ناب-باكليتاكسيل، بينما عزز مثبط PLK1 الحساسية للعقاقير.
ماذا يعني هذا لعلاجات المستقبل
بعبارة بسيطة، يحدد هذا العمل ثلاث جزيئات—P3H1 وPLK1 وβ-كاتينين—تعمل معًا كدواسة تسريع لأورام البنكرياس، فتدفع كلاً من انقسام الخلية الجامح وتجند الخلايا المناعية التي تساعد السرطان بدلاً من محاربته. تعطيل هذا المحور يبطئ نمو الورم ويجعل العلاج الكيميائي الحالي أكثر فعالية في النماذج الفأرية والنماذج المستمدة من مرضى البشر. وعلى الرغم من أن أدوية تحجب P3H1 مباشرة غير متاحة بعد، فإن مثبطات PLK1 قيد التطوير بالفعل، مما يثير احتمال أنه في المستقبل قد يوفر الجمع بينها وبين العلاج الكيميائي التقليدي سيطرة أكثر ديمومة على المرض لمرضى سرطان البنكرياس.
الاستشهاد: Bai, P., Liu, C., Fu, C. et al. Targeting Prolyl 3-hydroxylase 1 inhibits pancreatic cancer progression and macrophage immunity. Nat Commun 17, 3913 (2026). https://doi.org/10.1038/s41467-026-70452-w
الكلمات المفتاحية: سرطان البنكرياس, البيئة الميكروية للأورام, البلاعم, إشارة β-كاتينين, العلاج الكيميائي الموجه