Clear Sky Science · ru
Обратный перенос водорода ускоряет электрокаталитическое восстановление нитратов до аммиака на Ru/WO3-x в кислотной среде
Чище удобрения из грязной воды
Аммиак — основа современных удобрений и перспективный способ хранения водородного топлива, но сегодня его производство опирается на вековой процесс Габера–Боша, который потребляет огромные объёмы энергии и выбрасывает большие количества углекислого газа. Одновременно многие отрасли сбрасывают кислые сточные воды с высоким содержанием нитратов, наносящие вред экосистемам. В этом исследовании рассматривается способ превратить такое загрязнение в ресурс: с помощью электричества напрямую превращать нитрат в кислотной воде в аммиак, избегая при этом образования бесполезного водорода и коррозии катализатора.
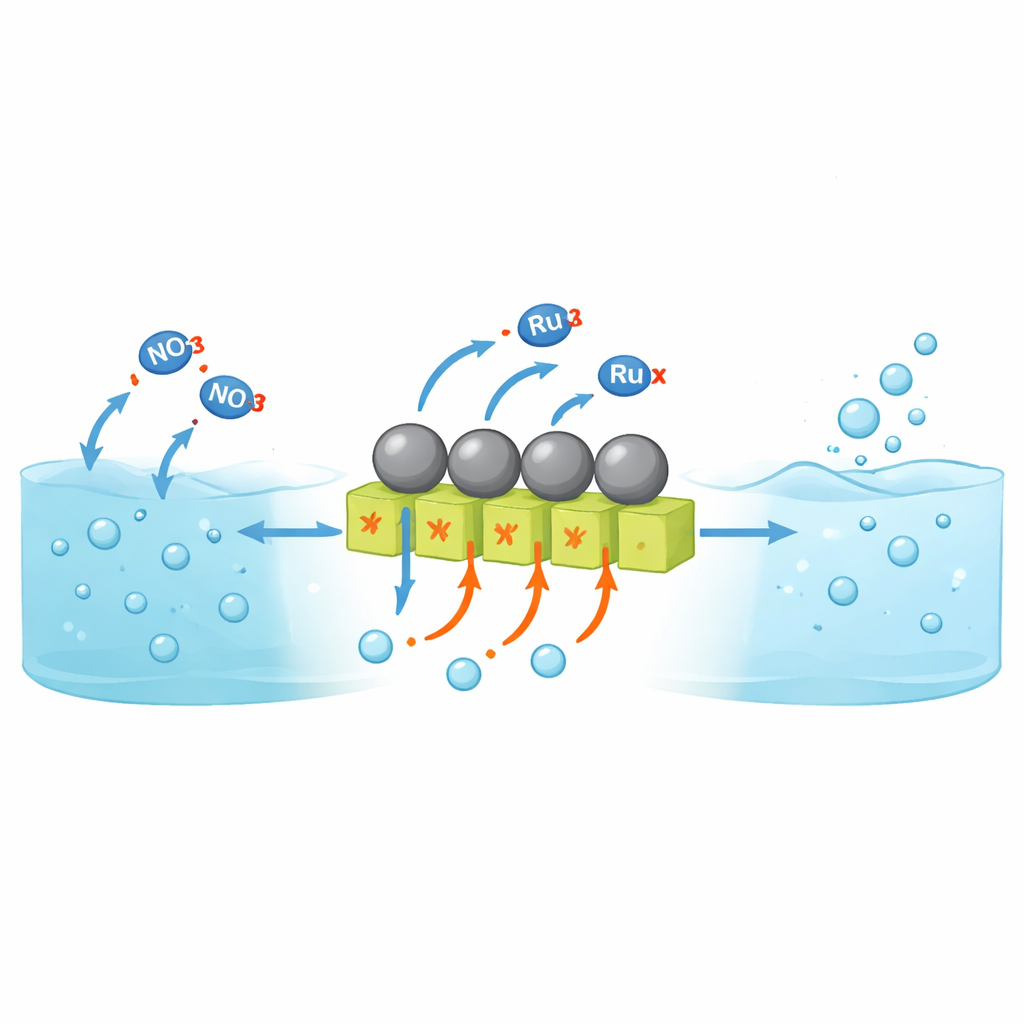
Почему превращать нитрат в аммиак сложно
Электрохимическое восстановление нитрата позволяет получать аммиак при комнатной температуре из воды и промышленных стоков вместо использования ископаемого топлива при высокой температуре и давлении. Однако большинство работ до сих пор посвящено нейтральным или щелочным растворам. В сильно кислой среде — ближе к реальным промышленным нитратным стокам — катализаторы склонны к коррозии, и побочная реакция берёт верх: протоны объединяются в молекулярный водород вместо того, чтобы участвовать в построении аммиака. Традиционно кислотоустойчивые металлы, такие как рутений, отлично связывают водород, что полезно для образования аммиака, но одновременно делает их очень активными для эволюции водорода. В результате лишь небольшая доля электрического тока идёт на синтез аммиака, особенно при высоких плотностях тока, необходимых для практических устройств.
Катализатор, который делит работу
Исследователи разработали композитный катализатор, который разделяет зоны обращения с водородом и нитратом, но при этом держит их в тесной близости для совместной работы. Они вырастили наностержни оксида вольфрама (WO3‑x) на титановой подложке и затем нанесли на их поверхность крошечные частицы рутения. Оксид вольфрама необычно хорошо поглощает протоны из кислого раствора и удерживает их внутри кристаллической решётки, но при этом плохо отдаёт их в виде молекулярного водорода. Детальная микроскопия и рентгеновские измерения показывают сильные электронные взаимодействия на границе между рутением и оксидом вольфрама, образующие множество контактных участков, где электронная структура рутения тонко меняется и в оксиде возникают вакансии кислорода. Эти изменения определяют, где накапливаются протоны и как они перемещаются.
Обратный перенос водорода в действии
В этой системе протоны сначала входят в решётку оксида вольфрама и запасаются вблизи поверхности катализатора. При приложенном напряжении они затем мигрируют от оксидной подложки обратно к частицам рутения — процесс, называемый обратным переносом водорода. Одновременно нитрат‑ионы из раствора оседают на рутении и поэтапно гидрируются через серию азот‑кислородных промежуточных звеньев, пока не образуется аммиак. Компьютерные моделирования показывают, что атомы рутения на интерфейсе, отдавшие часть электронной плотности вольфраму, предоставляют особенно благоприятные сайты для этих стадий присоединения водорода, снижая энергетические барьеры ключевых преобразований. Эксперименты с электрохимическими методами, in‑situ спектроскопией и изотопно меченым водородом подтверждают, что значительная доля протонов, хранящихся в оксиде, действительно перемещается к рутению и участвует в восстановлении нитратов вместо формирования газообразного водорода.
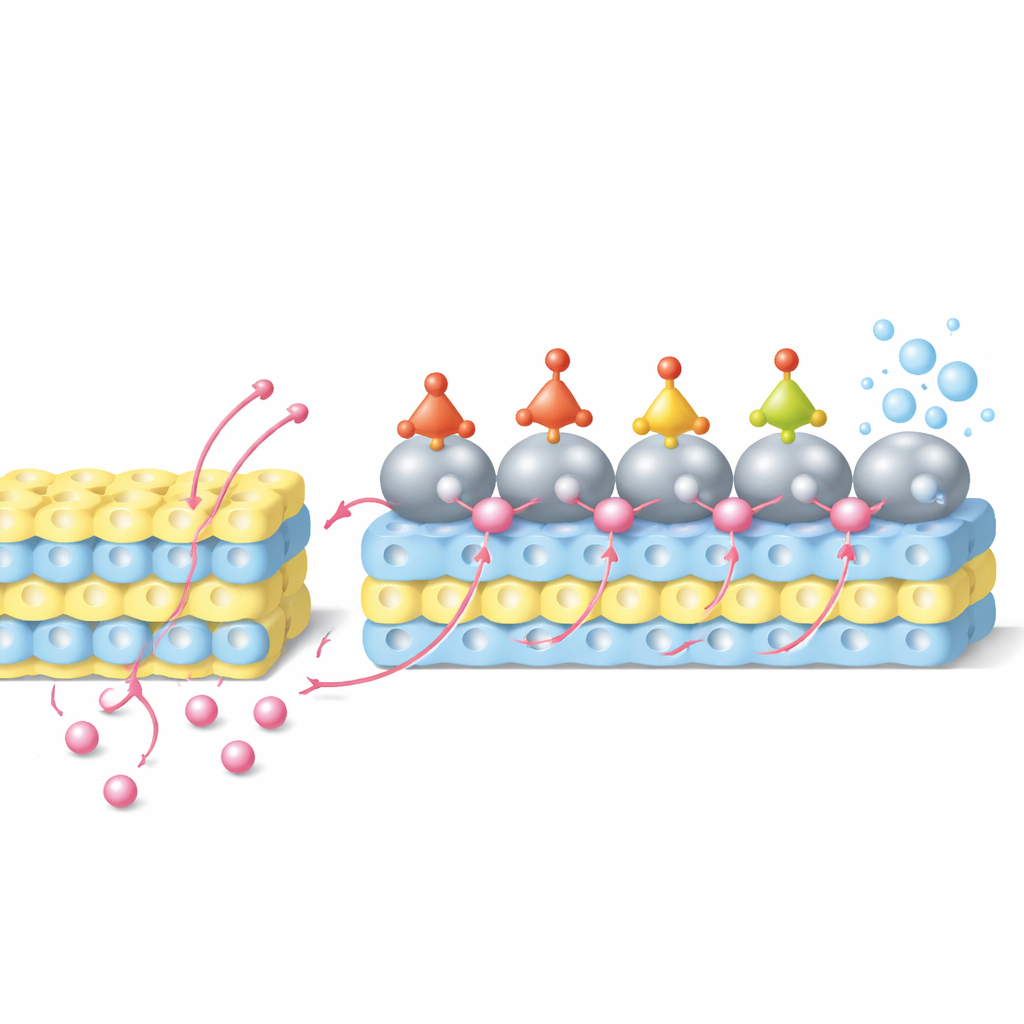
Рекордная производительность и работающее устройство
Поскольку подложка действует как быстрый резервуар и сеть доставки протонов, катализатор сохраняет сбалансированный и обильный запас водорода даже при очень высоких плотностях тока. В кислой нитратной среде электрод Ru/WO3‑x достигает плотности тока 500 миллиампер на квадратный сантиметр при почти нулевом приложенном напряжении, при этом примерно 94 процента электрического заряда превращаются в аммиак — показатели, превосходящие ранее описанные кислые системы для превращения нитратов в аммиак. Структура остаётся стабильной при длительной работе, и почти никаких нежелательных азотсодержащих побочных продуктов не обнаруживается. Чтобы продемонстрировать практическое применение, команда собрала «батаролайзер», в котором восстановление нитратов на этом катализаторе сочетается с окислением сульфидов на другом электрроде. Ячейка одновременно генерирует электрическую энергию и превращает нитрат и сульфидные загрязнения в полезные аммониевые и серосодержащие продукты.
Превращение отходов и электричества в ценность
Для неспециалиста главный вывод в том, что авторы нашли изящный способ, при котором один материал хранит и передаёт водород, а другой сосредоточен на преобразовании нитрата в аммиак. За счёт инженерии путей движения протонов — а не только за счёт создания более активного металла — они значительно подавляют образование бесполезного газообразного водорода и увеличивают выход аммиака в жёстких кислых условиях, близких к реальным промышленным стокам. Эта концепция разделения задач между подложкой и металлическим катализатором через контролируемый перенос водорода может быть применена ко многим другим электрохимическим преобразованиям, открывая пути к более чистому производству удобрений и устройствам, которые одновременно очищают сточные воды и поставляют полезные химикаты и энергию.
Цитирование: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Ключевые слова: синтез аммиака, нитратные сточные воды, электрокатализ, перенос водорода, катализатор на основе оксида вольфрама