Clear Sky Science · pt
O transbordamento reverso de hidrogênio acelera a redução eletrocatalítica de nitrato a amônia em Ru/WO3-x em meio ácido
Fertilizante mais limpo a partir de água poluída
A amônia é a espinha dorsal dos fertilizantes modernos e uma via promissora para armazenar hidrogênio combustível, mas sua produção hoje depende do processo Haber–Bosch centenário, que consome enormes quantidades de energia e emite grandes quantidades de dióxido de carbono. Ao mesmo tempo, muitas indústrias descartam águas residuais ácidas ricas em nitrato que podem prejudicar ecossistemas. Este estudo explora uma forma de transformar essa poluição em recurso: usar eletricidade para converter nitrato em água ácida diretamente em amônia, evitando ao mesmo tempo a produção desperdiçadora de gás hidrogênio e a corrosão do catalisador.
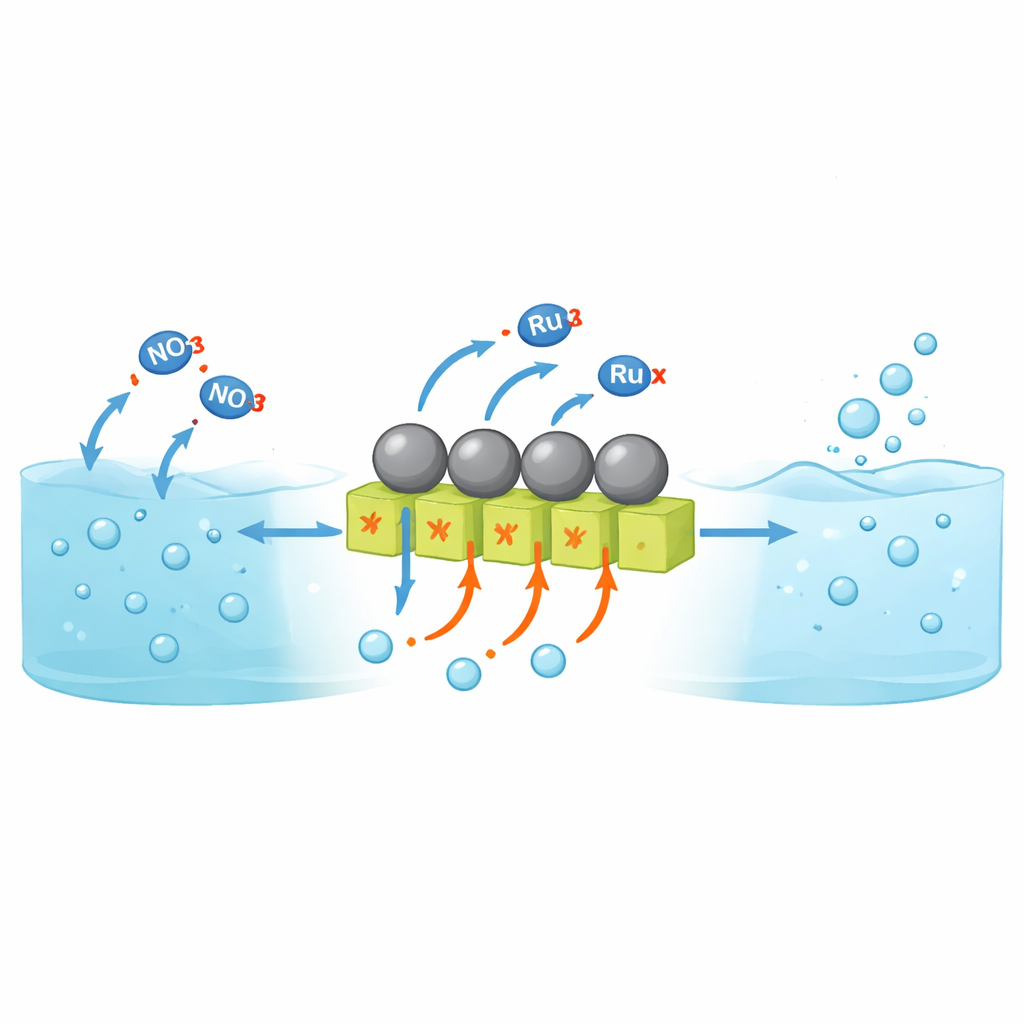
Por que transformar nitrato em amônia é difícil
A redução eletroquímica do nitrato permite produzir amônia à temperatura ambiente a partir de água e correntes de resíduos em vez de combustíveis fósseis em alta temperatura e pressão. No entanto, a maior parte das pesquisas até agora concentrou‑se em soluções neutras ou alcalinas. Em soluções fortemente ácidas — muito mais próximas dos efluentes industriais reais com nitrato — os materiais do catalisador tendem a corroer e uma reação concorrente domina: os prótons se combinam para formar gás hidrogênio em vez de contribuir para formar amônia. Metais convencionais resistentes à acidez, como o rutênio, ligam muito bem o hidrogênio, o que é bom para a formação de amônia, mas também os torna altamente ativos para a evolução de gás hidrogênio. Como resultado, muito pouca corrente elétrica se converte em amônia, especialmente nas densidades de corrente elevadas necessárias para dispositivos práticos.
Um catalisador que divide o trabalho
Os pesquisadores projetaram um catalisador composto que separa onde o hidrogênio e o nitrato são tratados, mantendo‑os suficientemente próximos para cooperação. Eles cresceram nanobastões de óxido de tungstênio (WO3‑x) sobre um suporte de titânio e então decoraram suas superfícies com pequenas partículas de rutênio. O óxido de tungstênio é incomumente bom em absorver prótons da solução ácida e mantê‑los dentro de sua estrutura cristalina, mas é ruim em liberá‑los como gás hidrogênio. Microscopia detalhada e medições por raios X mostram que surgem fortes interações eletrônicas na interface entre o rutênio e o óxido de tungstênio, criando muitos sítios de contato onde a estrutura eletrônica do rutênio é sutilmente alterada e vacâncias de oxigênio se formam no óxido. Essas mudanças ajudam a definir onde os prótons são armazenados e como eles se movem.
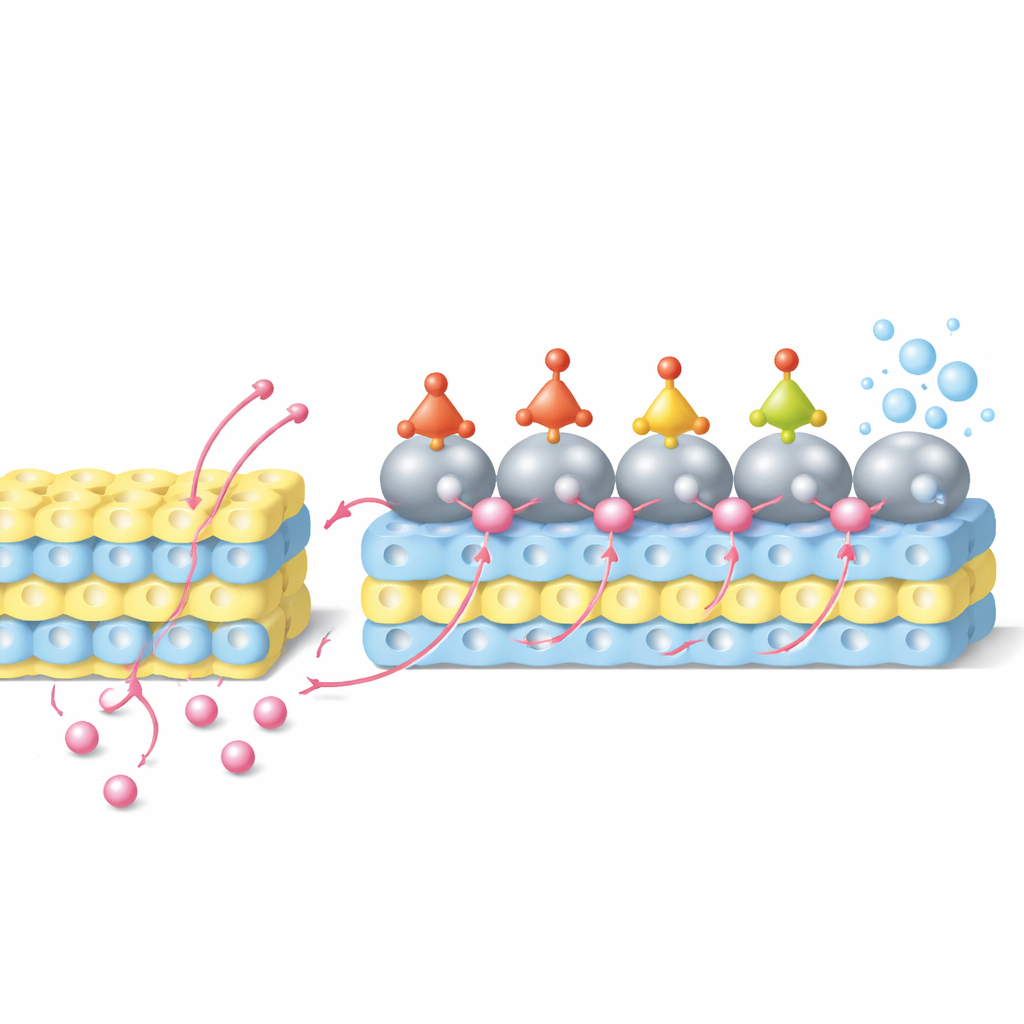
Transbordamento reverso de hidrogênio em ação
Nesse sistema, os prótons primeiro entram na grade do óxido de tungstênio e são armazenados próximos à superfície do catalisador. Sob tensão aplicada, eles então migram do suporte de óxido de volta em direção às partículas de rutênio — um processo denominado transbordamento reverso de hidrogênio. Ao mesmo tempo, íons nitrato da solução se adsorvem no rutênio e são hidrogenados passo a passo através de uma série de intermediários nitrogênio‑oxigênio até que a amônia seja formada. Simulações computacionais revelam que os átomos de rutênio na interface, que doaram parte da densidade eletrônica para o tungstênio, fornecem sítios especialmente favoráveis para essas etapas de adição de hidrogênio, reduzindo as barreiras de energia para transformações chave. Experimentos usando métodos eletroquímicos, espectroscopia in situ e hidrogênio marcado isotopicamente confirmam que uma fração significativa dos prótons armazenados no óxido de fato viaja para o rutênio e participa da redução do nitrato em vez de formar gás hidrogênio.
Desempenho recorde e um dispositivo funcional
Como o suporte atua como um reservatório rápido de prótons e uma rede de entrega, o catalisador mantém um suprimento de hidrogênio equilibrado e abundante mesmo em densidades de corrente muito altas. Em solução ácida de nitrato, o eletrodo Ru/WO3‑x alcança uma densidade de corrente de 500 miliamperes por centímetro quadrado a uma tensão aplicada quase nula, enquanto converte cerca de 94% da carga elétrica em amônia — valores que superam catalisadores previamente reportados para conversão de nitrato em amônia em meio ácido. A estrutura permanece estável durante operação prolongada, e quase nenhum subproduto indesejado de nitrogênio é detectado. Para demonstrar uso prático, a equipe construiu um “batteriolizador” que pareia a redução de nitrato neste catalisador com a oxidação de sulfeto em outro eletrodo. A célula gera simultaneamente energia elétrica e converte poluentes nitrato e sulfeto em produtos úteis à base de amônio e enxofre.
Transformando resíduo e eletricidade em valor
Para um público não especializado, a mensagem principal é que os autores descobriram uma maneira engenhosa de permitir que um material armazene e transporte hidrogênio enquanto outro se concentra em transformar nitrato em amônia. Ao projetar como os prótons se movem — em vez de simplesmente fabricar um metal mais ativo — eles suprimem amplamente a formação desperdiçadora de gás hidrogênio e aumentam a produção de amônia em condições ácidas severas que se assemelham a correntes de resíduos industriais reais. Esse conceito de dividir tarefas entre um suporte e um catalisador metálico por meio do transbordamento controlado de hidrogênio poderia ser aplicado a muitas outras reações eletroquímicas, abrindo caminhos para produção de fertilizantes mais limpa e para dispositivos que tanto tratam águas residuais quanto fornecem produtos químicos e energia úteis.
Citação: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Palavras-chave: síntese de amônia, água residual com nitrato, eletrocatálise, transbordamento de hidrogênio, catalisador de óxido de tungstênio