Clear Sky Science · it
L’inversione del spillover di idrogeno accelera la riduzione elettrocatalitica del nitrato ad ammoniaca su Ru/WO3-x in mezzi acidi
Fertilizzante più pulito dall’acqua inquinata
L’ammoniaca è la spina dorsale dei fertilizzanti moderni e una via promettente per immagazzinare idrogeno come combustibile, ma la sua produzione oggi si basa sul processo Haber–Bosch, vecchio di un secolo, che consuma enormi quantità di energia ed emette grandi quantità di anidride carbonica. Allo stesso tempo, molte industrie scaricano acque reflue acide ricche di nitrati che possono danneggiare gli ecosistemi. Questo studio esplora un modo per trasformare quell’inquinamento in una risorsa: usare elettricità per convertire i nitrati in acqua acida direttamente in ammoniaca, evitando al contempo la formazione inefficiente di idrogeno gassoso e la corrosione del catalizzatore.
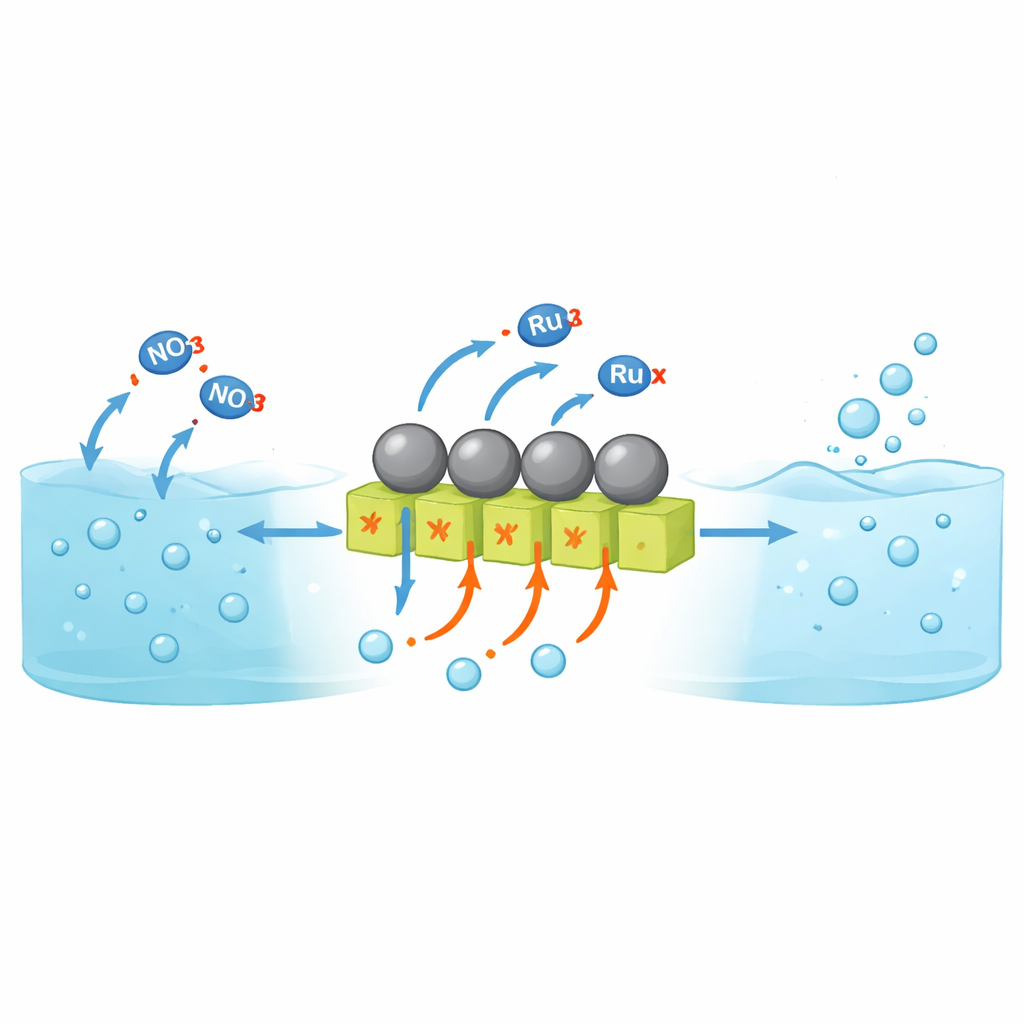
Perché convertire il nitrato in ammoniaca è difficile
La riduzione elettrochimica del nitrato permette di produrre ammoniaca a temperatura ambiente a partire dall’acqua e da flussi di rifiuto invece che da combustibili fossili a alta temperatura e pressione. Tuttavia, la maggior parte delle ricerche finora si è concentrata su soluzioni neutre o alcaline. In soluzioni fortemente acide—molto più vicine agli effluenti industriali reali—i materiali catalitici tendono a corrodersi e un’altra reazione prende il sopravvento: i protoni si combinano per formare idrogeno gassoso anziché contribuire alla formazione dell’ammoniaca. Metalli convenzionalmente resistenti agli acidi come il rutenio legano molto bene l’idrogeno, cosa utile per la formazione di ammoniaca ma che li rende anche molto attivi per l’evoluzione di idrogeno gassoso. Di conseguenza, pochissima della corrente elettrica viene convertita in ammoniaca, specialmente alle densità di corrente elevate necessarie per dispositivi pratici.
Un catalizzatore che condivide il lavoro
I ricercatori hanno progettato un catalizzatore composito che separa i luoghi in cui si gestiscono idrogeno e nitrato, pur mantenendoli abbastanza vicini da cooperare. Hanno fatto crescere nanorod di ossido di tungsteno (WO3‑x) su un supporto di titanio e poi hanno decorato le loro superfici con piccole particelle di rutenio. L’ossido di tungsteno è particolarmente efficace nell’assorbire protoni dalla soluzione acida e nel trattenerli nella sua struttura cristallina, pur essendo poco propenso a rilasciarli sotto forma di idrogeno gassoso. Microscopia dettagliata e misure ai raggi X mostrano che all’interfaccia tra rutenio e ossido di tungsteno emergono forti interazioni elettroniche, creando numerosi siti di contatto in cui la struttura elettronica del rutenio è sottilmente modificata e si formano vacanze di ossigeno nell’ossido. Questi cambiamenti aiutano a definire dove i protoni sono immagazzinati e come si muovono.
La prova dell’inversione del spillover di idrogeno
In questo sistema i protoni prima entrano nella reticolare dell’ossido di tungsteno e vengono immagazzinati vicino alla superficie del catalizzatore. Sotto applicazione di tensione, poi migrano dall’ossido di supporto verso le particelle di rutenio—un processo definito inversione dello spillover di idrogeno. Allo stesso tempo, gli ioni nitrato dalla soluzione si adsorbono sul rutenio e vengono idrogenati passo dopo passo attraverso una serie di intermedi azoto‑ossigeno fino a formare ammoniaca. Le simulazioni al calcolatore rivelano che gli atomi di rutenio all’interfaccia, che hanno donato parte della densità elettronica al tungsteno, forniscono siti particolarmente favorevoli per questi passi di aggiunta di idrogeno, abbassando le barriere energetiche per trasformazioni chiave. Esperimenti con metodi elettrochimici, spettroscopia in situ e idrogeno marcato con isotopi confermano che una frazione significativa dei protoni immagazzinati nell’ossido effettivamente viaggia verso il rutenio e partecipa alla riduzione del nitrato invece di formare idrogeno gassoso.
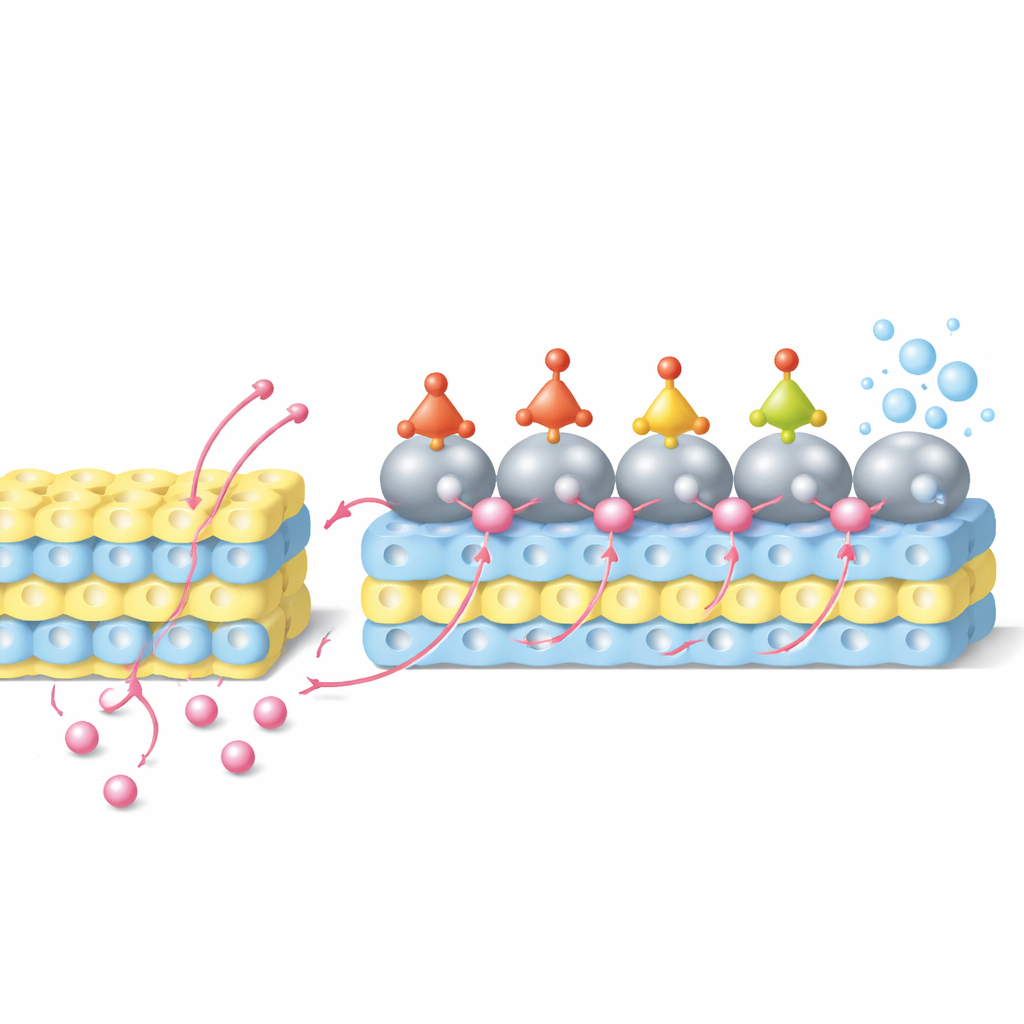
Prestazioni da record e un dispositivo funzionante
Poiché il supporto funge da rapido serbatoio e rete di consegna dei protoni, il catalizzatore mantiene una fornitura di idrogeno bilanciata e abbondante anche a densità di corrente molto elevate. In soluzione acida di nitrato, l’elettrodo Ru/WO3‑x raggiunge una densità di corrente di 500 milliampere per centimetro quadrato a una tensione applicata prossima allo zero, convertendo nel contempo circa il 94 percento della carica elettrica in ammoniaca—valori che superano i catalizzatori precedentemente riportati per la conversione acido nitrato→ammoniaca. La struttura rimane stabile durante lunghe operazioni e quasi nessun prodotto azotato indesiderato viene rilevato. Per dimostrare l’uso pratico, il team ha costruito un “batterolyzer” che abbina la riduzione del nitrato su questo catalizzatore con l’ossidazione del solfuro su un altro elettrodo. La cella genera contemporaneamente energia elettrica e converte i contaminanti nitrato e solfuro in prodotti utili a base di ammonio e zolfo.
Trasformare rifiuti ed elettricità in valore
Per un pubblico non specialista, il messaggio chiave è che gli autori hanno trovato un modo intelligente per lasciare che un materiale immagazzini e trasporti idrogeno mentre un altro si concentra sulla trasformazione del nitrato in ammoniaca. Ingegnerizzando il movimento dei protoni—piuttosto che limitarsi a rendere il metallo più attivo—sopprimono fortemente la formazione di idrogeno gassoso inutile e aumentano la produzione di ammoniaca in condizioni acide severe che somigliano ai flussi di rifiuto industriali reali. Questo concetto di condividere i compiti tra un supporto e un catalizzatore metallico tramite uno spillover controllato dell’idrogeno potrebbe essere applicato a molte altre reazioni elettrochimiche, aprendo strade a una produzione di fertilizzanti più pulita e a dispositivi che contemporaneamente depurano le acque reflue e forniscono prodotti chimici ed energia utili.
Citazione: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Parole chiave: sintesi dell’ammoniaca, acque reflue contenenti nitrato, elettrocatalisi, spillover dell’idrogeno, catalizzatore a base di ossido di tungsteno