Clear Sky Science · de
Umgekehrtes Wasserstoff‑Spillover beschleunigt die elektrochemische Nitratreduktion zu Ammoniak auf Ru/WO3-x in saurer Medien
Sauberer Dünger aus verschmutztem Wasser
Ammoniak ist das Rückgrat moderner Düngemittel und ein vielversprechender Träger für Wasserstoffkraftstoff. Seine heutige Herstellung beruht jedoch auf dem jahrhundertalten Haber‑Bosch‑Verfahren, das enorme Energiemengen verbraucht und große Mengen Kohlendioxid freisetzt. Gleichzeitig gelangen in vielen Industrien nitratreiches, saures Abwasser in die Umwelt, das Ökosysteme schädigen kann. Diese Studie untersucht einen Weg, diese Verschmutzung in eine Ressource zu verwandeln: mithilfe von Elektrizität Nitrat in saurem Wasser direkt in Ammoniak umzuwandeln, dabei die entstehende Abgabe von Wasserstoffgas zu vermeiden und Korrosion des Katalysators zu reduzieren.
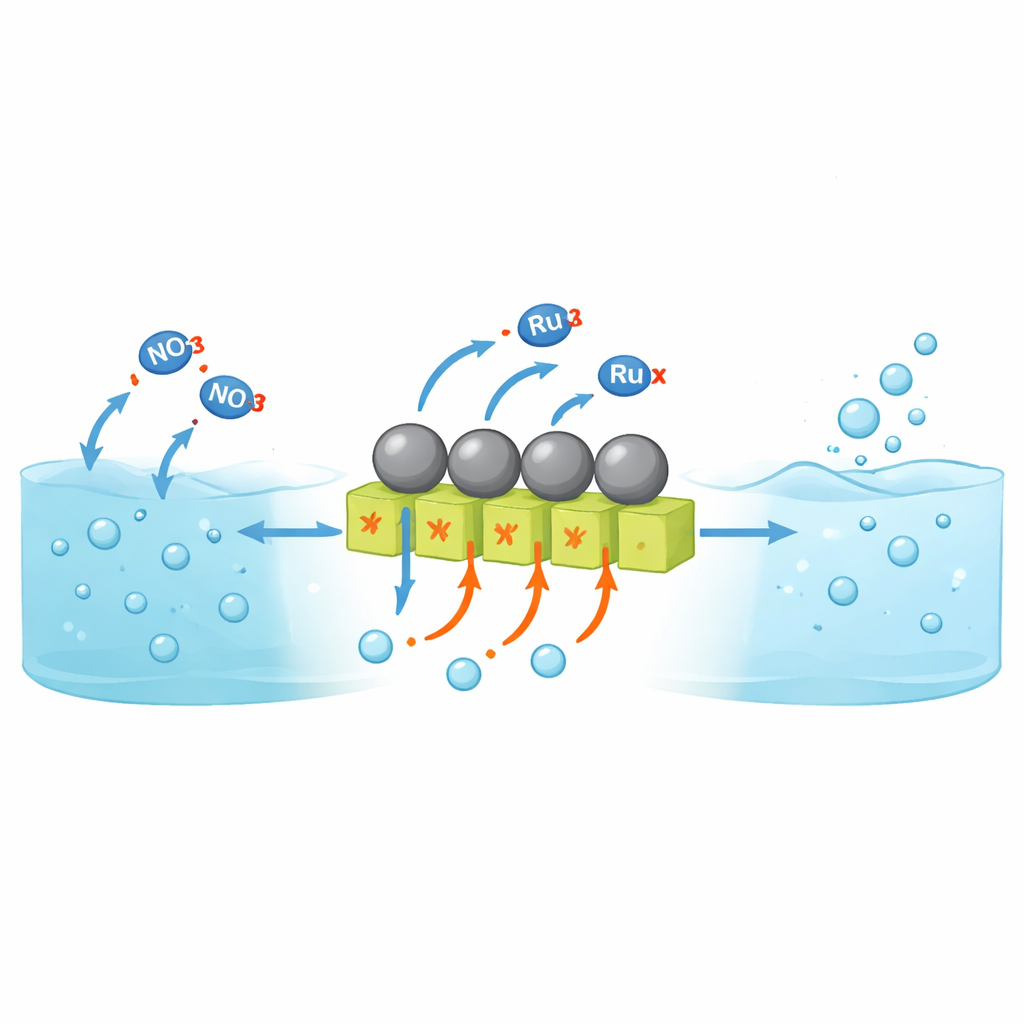
Warum die Umwandlung von Nitrat in Ammoniak schwierig ist
Die elektrochemische Reduktion von Nitrat ermöglicht die Herstellung von Ammoniak bei Raumtemperatur aus Wasser und Abwässern anstelle fossiler Brennstoffe unter hohen Temperaturen und Drücken. Bisher konzentrierte sich die Forschung jedoch überwiegend auf neutrale oder alkalische Lösungen. In stark sauren Lösungen — die den tatsächlichen industriellen Nitratabwässern näherkommen — neigen Katalysatormaterialien zur Korrosion, und eine Konkurrenzreaktion dominiert: Protonen verbinden sich zu Wasserstoffgas, anstatt zur Ammoniakbildung beizutragen. Konventionelle säureresistente Metalle wie Ruthenium binden Wasserstoff sehr stark, was zwar für die Ammoniaksynthese vorteilhaft ist, sie aber gleichzeitig hocheffizient für die Wasserstoffentwicklung macht. Folglich wird nur ein geringer Teil der elektrischen Ladung in Ammoniak umgesetzt, insbesondere bei den hohen Stromdichten, die für praktische Anwendungen nötig sind.
Ein Katalysator, der die Arbeit teilt
Die Forscher entwickelten einen Verbundkatalysator, der die Orte der Wasserstoff‑ und Nitratverarbeitung trennt, sie aber nahe genug zusammenhält, damit sie zusammenwirken können. Sie wuchsen Nanostäbchen aus Wolframat (WO3‑x) auf einer Titanunterlage und belegten deren Oberflächen anschließend mit winzigen Rutheniumpartikeln. Wolframat eignet sich ungewöhnlich gut dazu, Protonen aus saurer Lösung aufzunehmen und in seiner Kristallstruktur zu speichern, ist jedoch schlecht darin, diese als Wasserstoffgas freizusetzen. Detaillierte Mikroskopie und Röntgenmessungen zeigen, dass an der Schnittstelle zwischen Ruthenium und Wolframat starke elektronische Wechselwirkungen entstehen, die viele Kontaktstellen schaffen, an denen die elektronische Struktur des Rutheniums subtil verändert ist und Sauerstofffehlstellen im Oxid entstehen. Diese Änderungen beeinflussen, wo Protonen gespeichert werden und wie sie sich bewegen.
Umgekehrtes Wasserstoff‑Spillover in Aktion
In diesem System treten Protonen zunächst in das Wolframatgitter ein und werden in der Nähe der Katalysatoroberfläche gespeichert. Unter angelegter Spannung wandern sie dann vom Oxidträger zurück zu den Rutheniumpartikeln — ein Prozess, der als umgekehrtes Wasserstoff‑Spillover bezeichnet wird. Gleichzeitig treffen Nitrat‑Ionen aus der Lösung auf Ruthenium und werden schrittweise über eine Reihe von Stickstoff‑Sauerstoff‑Zwischenstufen hydriert, bis Ammoniak entsteht. Computersimulationen zeigen, dass Rutheniumatome an der Grenzfläche, die etwas Elektronendichte an Wolframat abgegeben haben, besonders günstige Stellen für diese Wasserstoffzufügungs‑Schritte bieten und damit die Energiebarrieren für wesentliche Umwandlungen senken. Experimente mit elektrochemischen Methoden, in‑situ Spektroskopie und isotopenmarkiertem Wasserstoff bestätigen, dass ein erheblicher Teil der im Oxid gespeicherten Protonen tatsächlich zu Ruthenium wandert und an der Nitratreduktion teilnimmt, statt zu Wasserstoffgas zu reagieren.
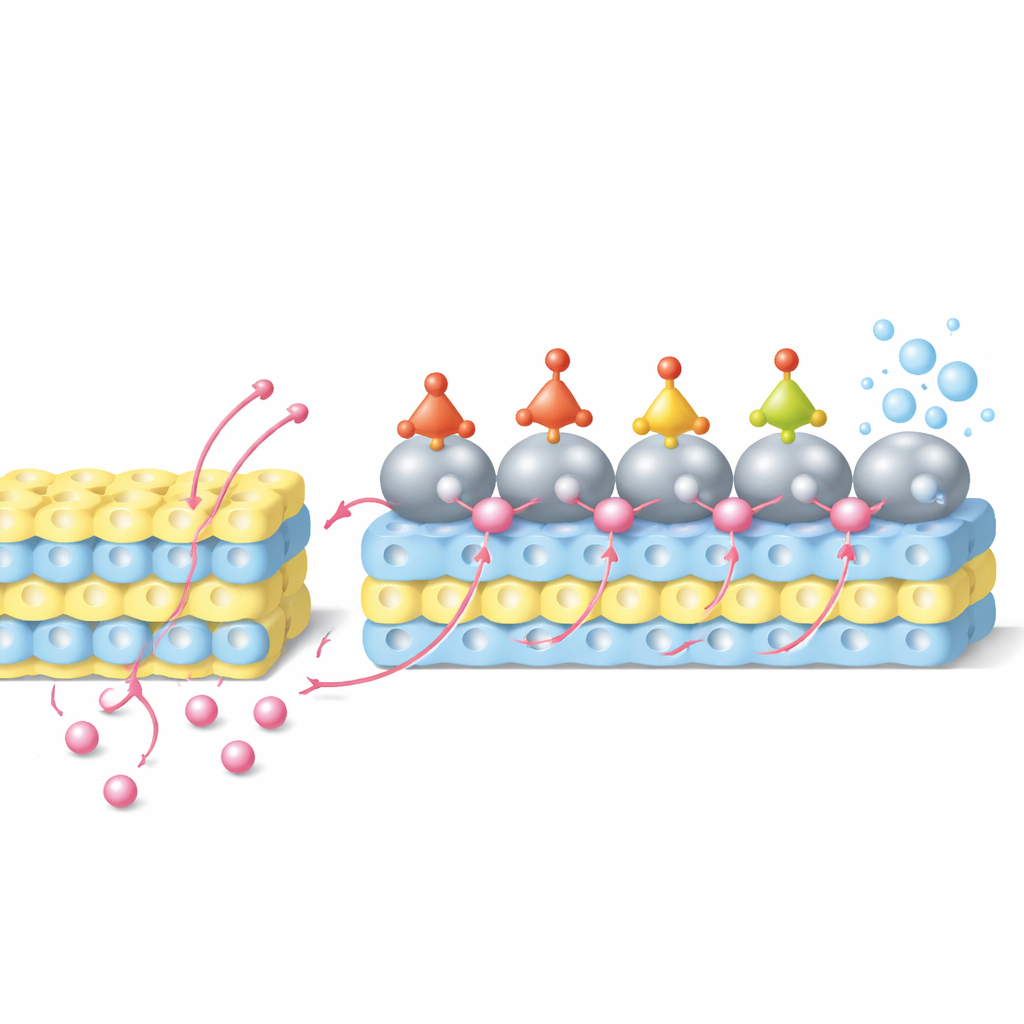
Rekordleistung und ein funktionierendes Gerät
Da der Träger als schneller Protonenspeicher und -liefernetz fungiert, hält der Katalysator auch bei sehr hohen Stromdichten eine ausgewogene und reichliche Wasserstoffversorgung aufrecht. In saurer Nitratlösung erreicht die Ru/WO3‑x‑Elektrode eine Stromdichte von 500 Milliampere pro Quadratzentimeter bei nahezu null angelegter Spannung und wandelt dabei etwa 94 Prozent der elektrischen Ladung in Ammoniak um — Werte, die zuvor berichtete saure Nitrat‑zu‑Ammoniak‑Katalysatoren übertreffen. Die Struktur bleibt über lange Betriebszeiten stabil, und nahezu keine unerwünschten Stickstoffnebenprodukte werden nachgewiesen. Um die praktische Anwendung zu demonstrieren, bauten die Forscher einen ‚Batterolyzer‘, der die Nitratreduktion an diesem Katalysator mit der Oxidation von Sulfid an einer anderen Elektrode koppelt. Die Zelle erzeugt gleichzeitig elektrische Leistung und verwandelt Nitrat‑ und Sulfid‑Verunreinigungen in nützliche Ammonium‑ und schwefelbasierte Produkte.
Abfall und Strom in Wert verwandeln
Für Nicht‑Spezialisten lautet die Kernbotschaft: Die Autoren haben einen eleganten Weg gefunden, ein Material als Speicher und Transporteur für Wasserstoff zu nutzen, während ein anderes Material sich auf die Umwandlung von Nitrat zu Ammoniak konzentriert. Indem sie die Bewegung der Protonen steuern — statt einfach nur ein reaktiveres Metall herzustellen — unterdrücken sie die verschwendende Bildung von Wasserstoffgas stark und steigern die Ammoniakausbeute unter den rauen sauren Bedingungen, die realen Industrieabwässern ähneln. Dieses Konzept, Aufgaben zwischen einem Träger und einem Metallkatalysator über kontrolliertes Wasserstoff‑Spillover zu teilen, könnte auf viele andere elektrochemische Reaktionen angewendet werden und Wege zu saubererer Düngerproduktion sowie zu Geräten öffnen, die Abwasser reinigen und dabei nützliche Chemikalien und Energie liefern.
Zitation: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Schlüsselwörter: Ammoniaksynthese, Nitratabwasser, Elektrokatalyse, Wasserstoff‑Spillover, Tungstenoxid‑Katalysator