Clear Sky Science · fr
La migration inverse d’hydrogène accélère la réduction électrocatalytique des nitrates en ammoniaque sur Ru/WO3-x en milieu acide
Un engrais plus propre à partir d’eaux polluées
L’ammoniac est la colonne vertébrale des engrais modernes et un vecteur prometteur pour stocker l’hydrogène, mais sa production actuelle repose sur le procédé centenaire Haber–Bosch, énergivore et fortement émetteur de dioxyde de carbone. Parallèlement, de nombreuses industries rejettent des eaux usées acides riches en nitrates qui peuvent endommager les écosystèmes. Cette étude examine une manière de transformer cette pollution en ressource : utiliser l’électricité pour convertir directement les nitrates en solution acide en ammoniac, tout en évitant la production inutile de gaz hydrogène et la corrosion du catalyseur.
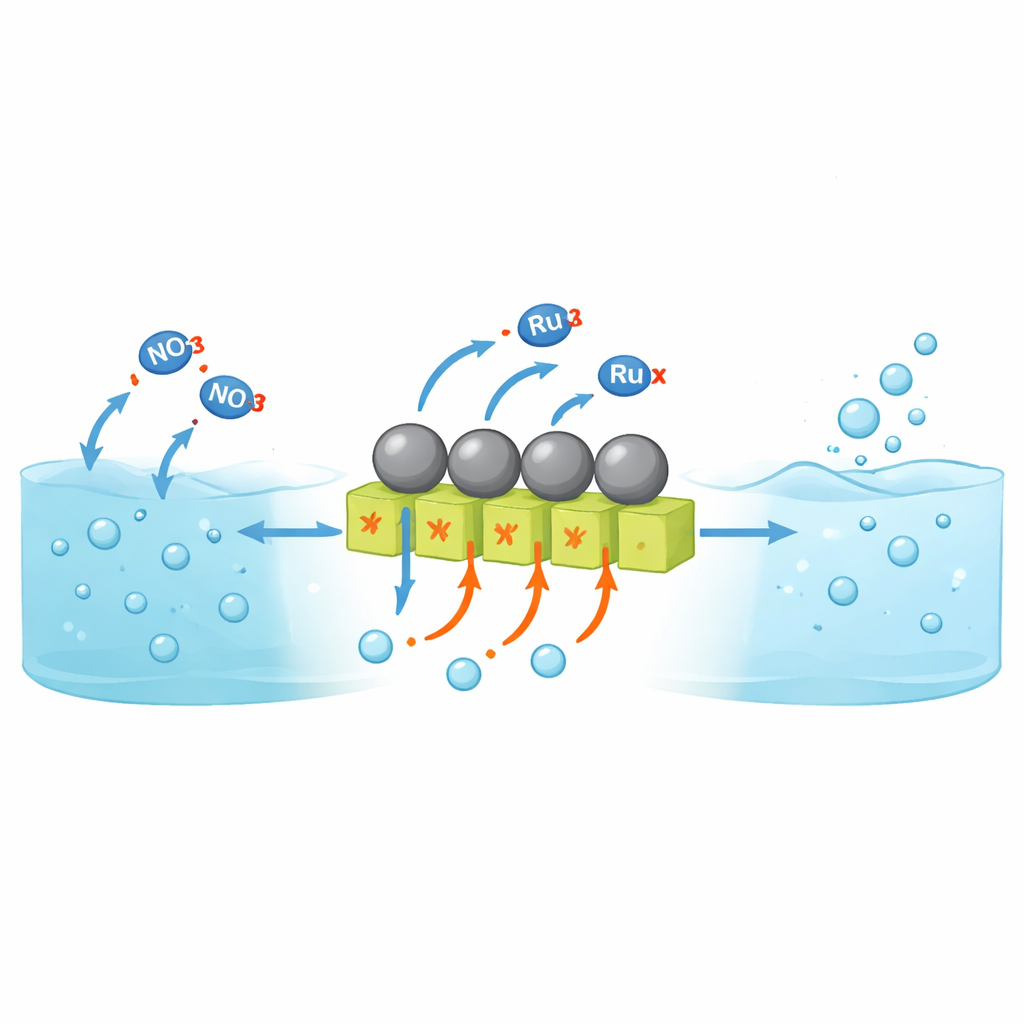
Pourquoi convertir les nitrates en ammoniac est difficile
La réduction électrochimique des nitrates permet de produire de l’ammoniac à température ambiante à partir d’eau et de flux de déchets plutôt que depuis des combustibles fossiles à haute température et pression. Cependant, la plupart des travaux se sont jusqu’à présent concentrés sur des solutions neutres ou alcalines. En solutions fortement acides — beaucoup plus proches des effluents industriels nitrés réels — les matériaux catalytiques ont tendance à corroder et une autre réaction prédomine : les protons se combinent pour former du gaz hydrogène au lieu de contribuer à la formation d’ammoniac. Les métaux résistants en milieu acide comme le ruthénium lient très bien l’hydrogène, ce qui favorise la formation d’ammoniac mais les rend aussi très actifs pour l’évolution de l’hydrogène. En conséquence, une très faible fraction du courant électrique sert réellement à produire de l’ammoniac, surtout aux densités de courant élevées nécessaires pour des dispositifs pratiques.
Un catalyseur qui partage le travail
Les chercheurs ont conçu un catalyseur composite qui sépare les lieux de traitement de l’hydrogène et des nitrates, tout en les maintenant assez proches pour coopérer. Ils ont fait croître des nanobâtonnets d’oxyde de tungstène (WO3‑x) sur un support en titane, puis ont décoré leurs surfaces de nanoparticules de ruthénium. L’oxyde de tungstène est particulièrement bon pour absorber les protons depuis une solution acide et les retenir dans sa structure cristalline, mais il libère difficilement ces protons sous forme de gaz hydrogène. La microscopie détaillée et les mesures par rayons X montrent que de fortes interactions électroniques apparaissent à l’interface entre le ruthénium et l’oxyde de tungstène, créant de nombreux sites de contact où la structure électronique du ruthénium est subtilement modifiée et où des lacunes en oxygène se forment dans l’oxyde. Ces changements contribuent à définir où les protons sont stockés et comment ils se déplacent.
La migration inverse d’hydrogène en action
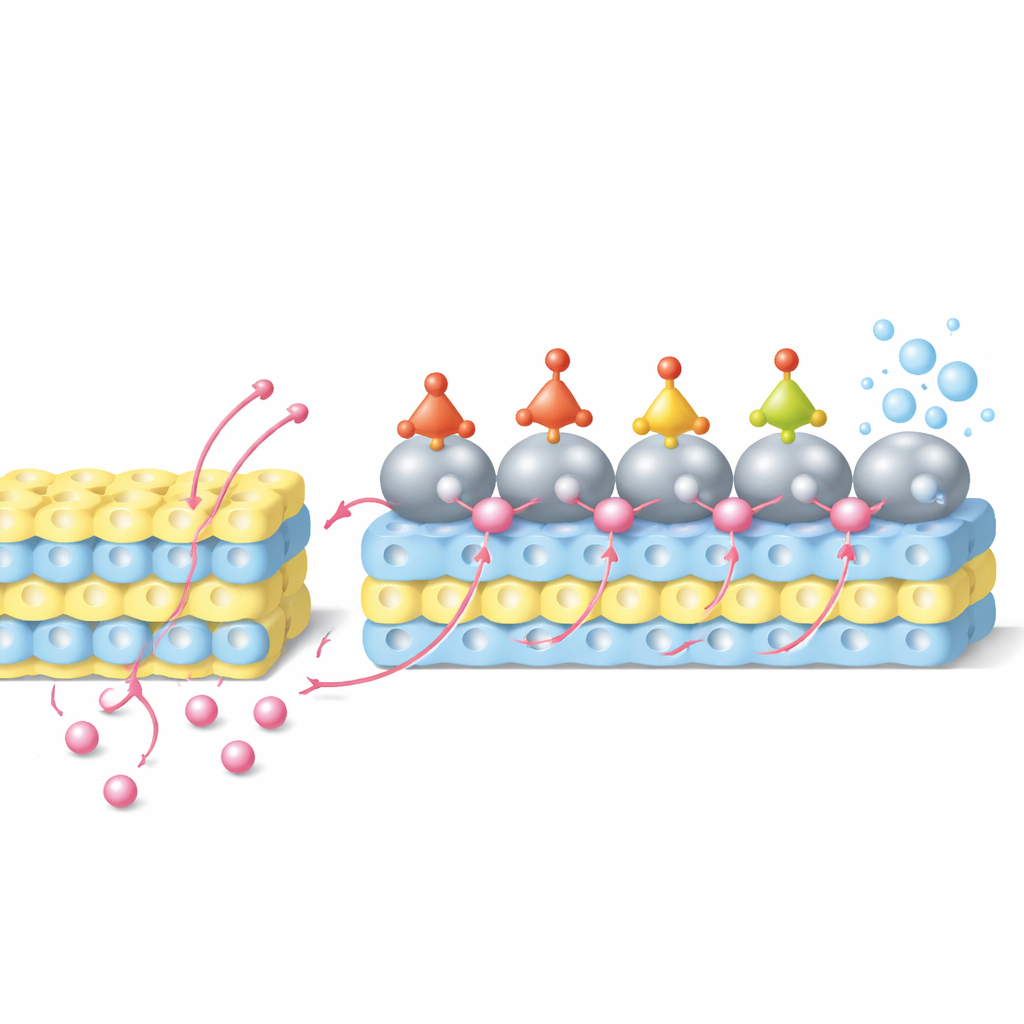
Dans ce système, les protons pénètrent d’abord dans le réseau de l’oxyde de tungstène et sont stockés près de la surface du catalyseur. Sous l’effet d’une tension appliquée, ils migrent ensuite depuis le support oxydique vers les particules de ruthénium — un processus appelé migration inverse d’hydrogène. Simultanément, les ions nitrate en solution se fixent sur le ruthénium et sont hydrogénés pas à pas à travers une série d’intermédiaires oxygénés de l’azote jusqu’à la formation d’ammoniac. Des simulations informatiques montrent que les atomes de ruthénium à l’interface, ayant cédé une partie de leur densité électronique au tungstène, offrent des sites particulièrement favorables pour ces étapes d’ajout d’hydrogène, abaissant les barrières énergétiques des transformations clés. Des expériences électrochimiques, des spectroscopies in situ et des essais avec hydrogène marqué isotopiquement confirment qu’une fraction significative des protons stockés dans l’oxyde migre effectivement vers le ruthénium et participe à la réduction des nitrates au lieu de former du gaz hydrogène.
Performance record et dispositif fonctionnel
Parce que le support sert de réservoir et de réseau de distribution rapide de protons, le catalyseur maintient un apport en hydrogène équilibré et abondant même à des densités de courant très élevées. En solution acide contenant des nitrates, l’électrode Ru/WO3‑x atteint une densité de courant de 500 milliampères par centimètre carré à une tension appliquée proche de zéro, tout en convertissant environ 94 % de la charge électrique en ammoniac — des performances supérieures aux catalyseurs acides précédemment rapportés pour la conversion nitrate→ammoniac. La structure reste stable sur de longues durées de fonctionnement et quasiment aucun sous‑produit azoté indésirable n’est détecté. Pour démontrer l’utilité pratique, l’équipe a construit un « batterolyseur » associant la réduction des nitrates sur ce catalyseur à l’oxydation de sulfure sur une autre électrode. La cellule génère simultanément de l’énergie électrique et convertit les polluants nitrate et sulfure en produits utiles à base d’ammonium et de soufre.
Transformer déchets et électricité en valeur
Pour un non‑spécialiste, l’idée clé est que les auteurs ont trouvé une manière ingénieuse de laisser un matériau stocker et transporter l’hydrogène tandis qu’un autre se concentre sur la transformation des nitrates en ammoniac. En maîtrisant le déplacement des protons — plutôt qu’en se contentant de rendre un métal plus actif — ils suppriment largement la formation inutile de gaz hydrogène et augmentent la production d’ammoniac dans des conditions acides agressives proches des réels effluents industriels. Ce concept de partage des tâches entre un support et un catalyseur métallique via une migration contrôlée de l’hydrogène pourrait s’appliquer à de nombreuses autres réactions électrochimiques, ouvrant des voies vers une production d’engrais plus propre et des dispositifs qui à la fois épurent les eaux usées et fournissent des produits chimiques et de l’énergie utiles.
Citation: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Mots-clés: synthèse de l’ammoniac, eaux usées riches en nitrates, électrocatalyse, migration d’hydrogène, catalyseur à base d’oxyde de tungstène