Clear Sky Science · ar
التسرّب العكسي للهيدروجين يسرّع الاختزال الكهروتحفيزي لنترات الأمونيا على Ru/WO3-x في وسط حمضي
أسمدة أنظف من مياه ملوثة
الأمونيا تشكّل العمود الفقري للأسمدة الحديثة وتمثل وسيلة واعدة لتخزين وقود الهيدروجين، لكن إنتاجها اليوم يعتمد على عملية هابر–بوش القديمة التي تستهلك كميات هائلة من الطاقة وتطلق كميات كبيرة من ثاني أكسيد الكربون. وفي الوقت نفسه، تتخلص كثير من الصناعات من مياه صرف حمضية غنية بالنترات يمكن أن تضر الأنظمة البيئية. تدرس هذه الدراسة طريقة لتحويل تلك الملوّثات إلى مورد: استخدام الكهرباء لتحويل النترات في الماء الحمضي مباشرة إلى أمونيا، مع تجنّب إنتاج غاز الهيدروجين المهدِر وتآكل المحفز.
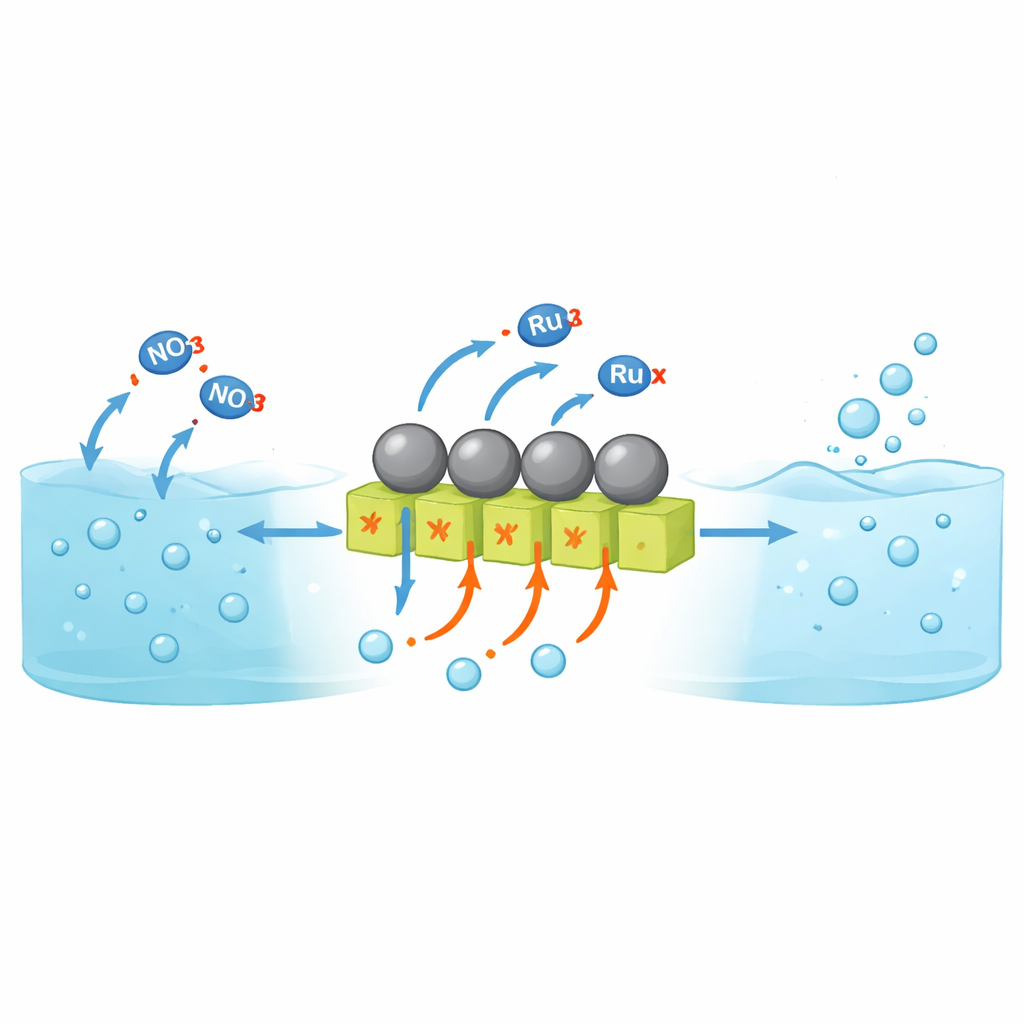
لماذا تحويل النترات إلى أمونيا صعب
يتيح الاختزال الكهروكيميائي للنترات إنتاج الأمونيا في درجة حرارة الغرفة من الماء ومجاري النفايات بدلاً من الاعتماد على الوقود الأحفوري ودرجات الحرارة والضغوط العالية. مع ذلك، ركزت معظم الأبحاث حتى الآن على محاليل محايدة أو قلوية. في المحاليل الحمضية الشديدة — الأقرب إلى مياه صرف صناعية حقيقية — تميل مواد المحفز إلى التآكل وتسيطر تفاعل آخر: تتحد البروتونات لتكوّن غاز الهيدروجين بدل أن تساهم في بناء الأمونيا. المعادن المقاومة للحمض التقليدية مثل الروثينيوم ممتازة في ربط الهيدروجين، وهو أمر مفيد لتكوين الأمونيا لكنه يجعلها نشطة جداً لتطور غاز الهيدروجين. نتيجة لذلك، يتحوّل جزء ضئيل فقط من التيار الكهربائي إلى أمونيا، لا سيما عند كثافات التيار العالية المطلوبة للأجهزة العملية.
محفز يقسّم العمل
صمّم الباحثون محفزاً مُركباً يفصل أماكن التعامل مع الهيدروجين والنترات، مع إبقائهما على مقربة كافية للتعاون. نما لديهم أعمدة نانوية من أكسيد التنجستن (WO3‑x) على دعم من التيتانيوم ثم زُيّنت أسطحها بجسيمات صغيرة من الروثينيوم. يتميز أكسيد التنجستن بقدرته الفريدة على امتصاص البروتونات من المحلول الحمضي واحتفاظها داخل بنيته البلورية، ومع ذلك فإنه ضعيف في تحريرها كغاز هيدروجين. تُظهر الميكروسكوبات التفصيلية وقياسات الأشعة السينية أن تفاعلات إلكترونية قوية تنشأ عند الواجهة بين الروثينيوم وأكسيد التنجستن، مما يخلق مواقع تلامس عديدة يتغيّر عندها البنية الإلكترونية للروثينيوم بشكل طفيف وتتشكل شواغر أكسجينية في الأكاسيد. تساعد هذه التغيرات في تحديد أماكن تخزين البروتونات وكيفية حركتها.
تسرّب الهيدروجين العكسي قيد العمل
في هذا النظام تدخل البروتونات أولاً شبكة أكسيد التنجستن وتخزن قرب سطح المحفز. تحت تأثير جهد كهربائي مطبّق، تنتقل لاحقاً من دعامة الأكسيد عائدةً نحو جسيمات الروثينيوم — عملية تُسمى تسرّب الهيدروجين العكسي. في الوقت نفسه، تحط أيونات النترات من المحلول على الروثينيوم وتخضع لهدرجة تدريجية عبر سلسلة من الوسائط النيتروجينية-الأكسجينية حتى تتكون الأمونيا. تكشف المحاكاة الحاسوبية أن ذرات الروثينيوم عند الواجهة، والتي تبرعت ببعض كثافة إلكترونية للتنجستن، توفر مواقع ملائمة بشكل خاص لخطوات إضافة الهيدروجين هذه، مما يخفض حواجز الطاقة للتحولات الأساسية. تؤكد التجارب باستخدام طرق كهروكيميائية، وطيفية في الموقع، وهيدروجين موسوم بالنظائر أن جزءاً كبيراً من البروتونات المخزنة في الأكسيد بالفعل ينتقل إلى الروثينيوم ويشارك في اختزال النترات بدل أن يشكل غاز الهيدروجين.
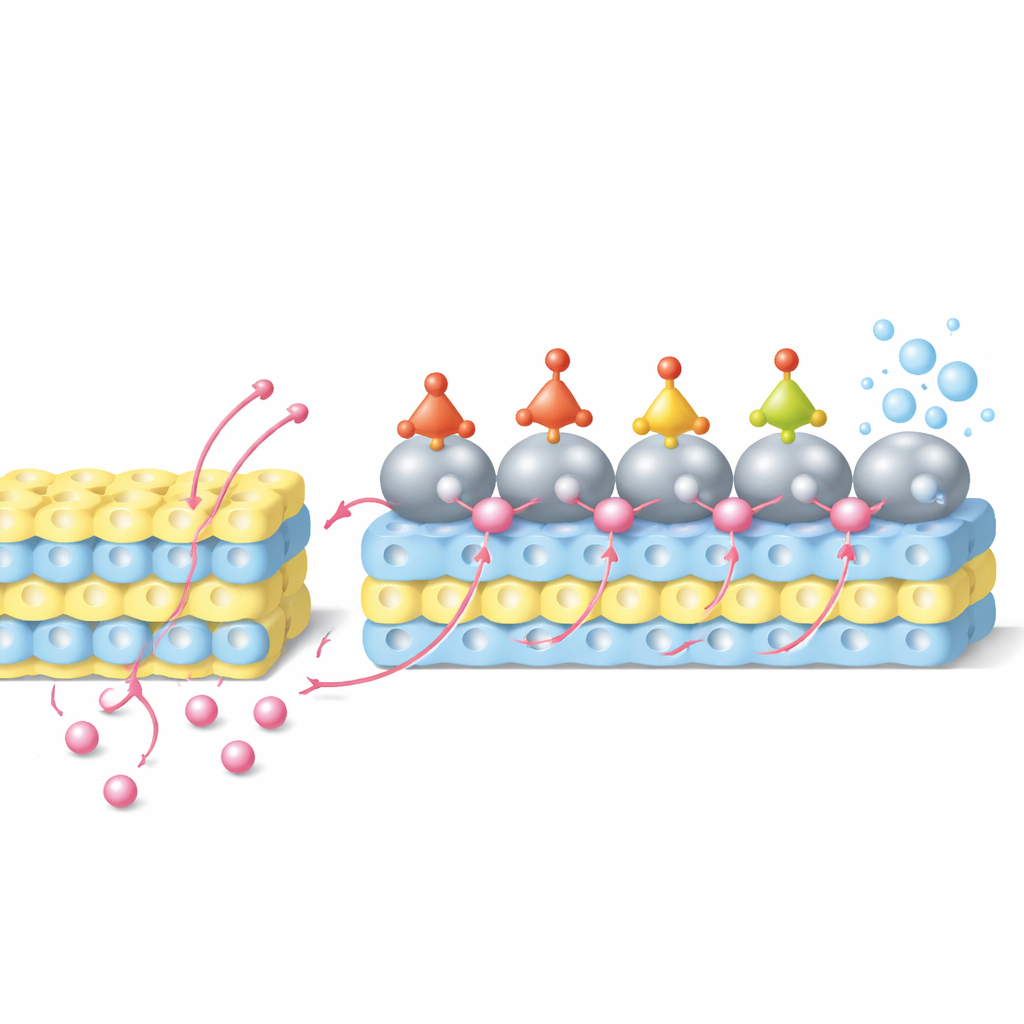
أداء قياسي وجهاز عملي
لأن الدعامة تعمل كمستودع وشبكة توصيل سريعة للبروتونات، يحافظ المحفز على إمداد متوازن ووفير من الهيدروجين حتى عند كثافات تيار عالية جداً. في محلول نترات حمضي، يحقّق قطب Ru/WO3‑x كثافة تيار تبلغ 500 ملي أمبير لكل سنتيمتر مربع عند جهد مطبّق قريب من الصفر، مع تحويل نحو 94 بالمئة من الشحنة الكهربائية إلى أمونيا — وهي قيم تتفوق على المحفزات المبلّغة سابقاً لتحويل النترات إلى أمونيا في وسط حمضي. تبقى البنية مستقرة على مدى تشغيل طويل، ولا تُكشف تقريباً أي نواتج نيتروجينية غير مرغوب فيها. ولإظهار استخدام عملي، بنى الفريق "بطارية‑محلّل" (batterolyzer) يزاوج اختزال النترات على هذا المحفز مع أكسدة الكبريتيد على قطب آخر. تولد الخلية طاقة كهربائية في الوقت نفسه التي تحول فيه النترات والكبريتيد الملوّثين إلى منتجات أمونيوم ومشتقات كبريت مفيدة.
تحويل النفايات والكهرباء إلى قيمة
بالنسبة للقارئ غير المتخصص، الرسالة الأساسية هي أن الباحثين وجدوا طريقة ذكية تسمح لمادة واحدة بتخزين ونقل الهيدروجين بينما تركز مادة أخرى على تحويل النترات إلى أمونيا. من خلال هندسة حركة البروتونات — بدلاً من مجرد صنع معدن أكثر نشاطاً — قلّلوا كثيراً من تكوّن غاز الهيدروجين المهدِر وزادوا إنتاج الأمونيا في ظروف حمضية قاسية تشبه مجاري النفايات الصناعية الحقيقية. يمكن تطبيق مفهوم تقسيم المهام بين دعامة ومحفز معدني عبر تسرّب الهيدروجين المتحكّم به على العديد من التفاعلات الكهروكيميائية الأخرى، مما يفتح طرقاً لإنتاج أسمدة أنظف ولأجهزة تنظف مياه الصرف وتنتج مواد مفيدة وطاقة.
الاستشهاد: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
الكلمات المفتاحية: تصنيع الأمونيا, مياه مصرفية غنية بالنترات, التحفيز الكهربائي, تسرّب الهيدروجين, محفز أكسيد التنجستن