Clear Sky Science · es
El derrame de hidrógeno inverso acelera la reducción electrocatalítica de nitrato a amoníaco en Ru/WO3-x en medios ácidos
Fertilizante más limpio a partir de aguas sucias
El amoníaco es la columna vertebral de los fertilizantes modernos y una vía prometedora para almacenar hidrógeno como combustible, pero su producción actual depende del proceso Haber–Bosch centenario, que consume grandes cantidades de energía y emite enormes cantidades de dióxido de carbono. Al mismo tiempo, muchas industrias vierten aguas residuales ácidas ricas en nitratos que pueden dañar los ecosistemas. Este estudio explora una forma de convertir esa contaminación en un recurso: usar electricidad para convertir directamente el nitrato en agua ácida en amoníaco, evitando la producción desperdiciada de gas hidrógeno y la corrosión del catalizador.
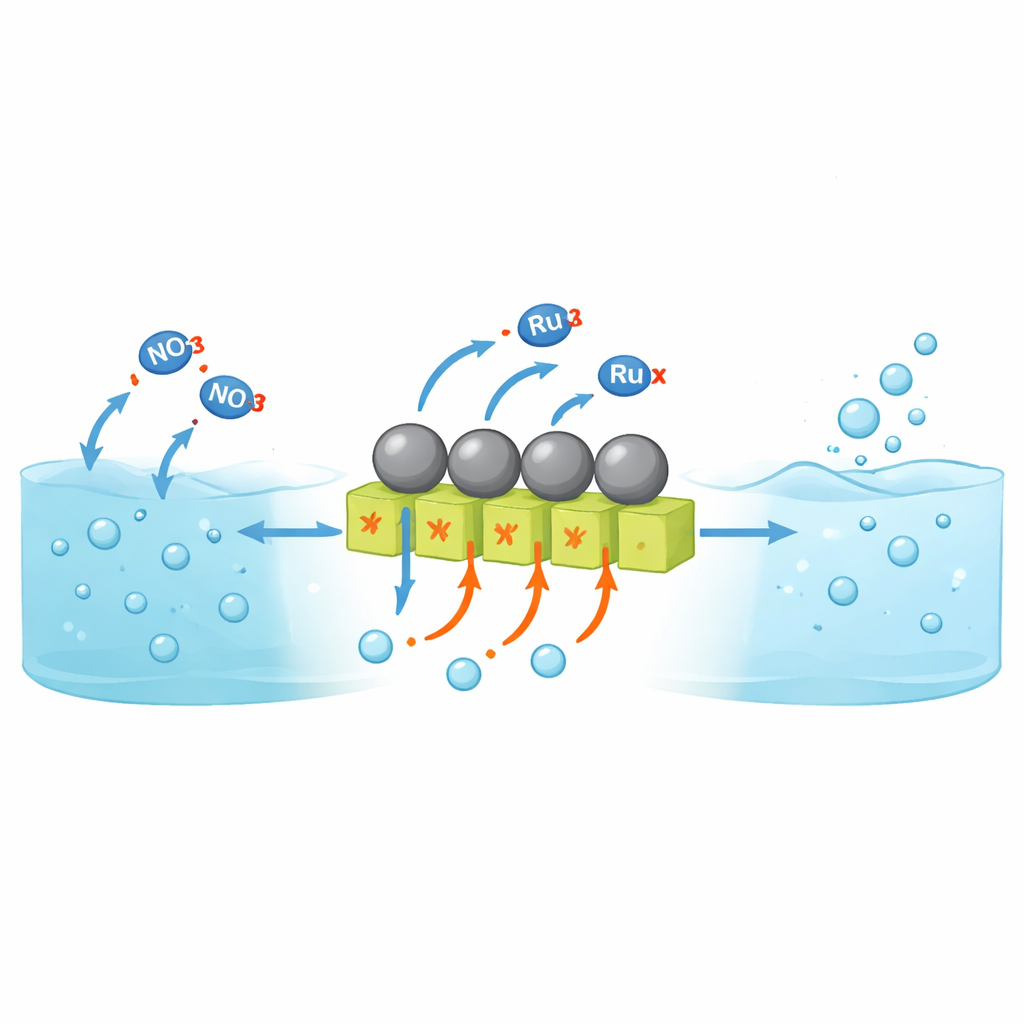
Por qué es difícil convertir nitrato en amoníaco
La reducción electroquímica del nitrato permite fabricar amoníaco a temperatura ambiente a partir de agua y corrientes de desecho en lugar de a partir de combustibles fósiles a alta temperatura y presión. Sin embargo, la mayoría de la investigación hasta ahora se ha centrado en soluciones neutras o alcalinas. En soluciones fuertemente ácidas —mucho más cercanas a efluentes industriales reales con nitrato— los materiales catalíticos tienden a corroerse y surge otra reacción dominante: los protones se combinan para formar gas hidrógeno en vez de ayudar a construir amoníaco. Metales convencionales resistentes al ácido, como el rutenio, son excelentes para adsorber hidrógeno, lo cual favorece la formación de amoníaco pero también los hace muy activos para la evolución de hidrógeno. Como resultado, muy poca corriente eléctrica termina produciendo amoníaco, especialmente a las densidades de corriente altas necesarias para dispositivos prácticos.
Un catalizador que reparte el trabajo
Los investigadores diseñaron un catalizador compuesto que separa dónde se manejan el hidrógeno y el nitrato, manteniéndolos lo bastante cerca para cooperar. Hicieron crecer nanobarras de óxido de tungsteno (WO3‑x) sobre un soporte de titanio y luego decoraron sus superficies con pequeñas partículas de rutenio. El óxido de tungsteno es excepcionalmente bueno para absorber protones desde la solución ácida y retenerlos dentro de su estructura cristalina, pero es pobre liberándolos como gas hidrógeno. Microscopía detallada y mediciones por rayos X muestran que surgen interacciones electrónicas fuertes en la interfaz entre rutenio y óxido de tungsteno, creando muchos sitios de contacto donde la estructura electrónica del rutenio se altera sutilmente y se forman vacantes de oxígeno en el óxido. Estos cambios ayudan a definir dónde se almacenan los protones y cómo se mueven.
Derrame de hidrógeno inverso en acción
En este sistema, los protones primero entran en la red del óxido de tungsteno y se almacenan cerca de la superficie del catalizador. Bajo una tensión aplicada, luego migran desde el soporte de óxido de vuelta hacia las partículas de rutenio: un proceso denominado derrame de hidrógeno inverso. Al mismo tiempo, los iones nitrato de la solución se adsorben sobre el rutenio y se hidrogenan por etapas a través de una serie de intermedios oxigenados del nitrógeno hasta formarse amoníaco. Simulaciones por ordenador revelan que los átomos de rutenio en la interfaz, que han donado parte de su densidad electrónica al tungsteno, proporcionan sitios especialmente favorables para estos pasos de adición de hidrógeno, reduciendo las barreras energéticas para transformaciones clave. Experimentos con métodos electroquímicos, espectroscopía in situ y mediciones con hidrógeno isotópicamente marcado confirman que una fracción significativa de los protones almacenados en el óxido efectivamente viaja al rutenio y participa en la reducción de nitrato en lugar de formar gas hidrógeno.
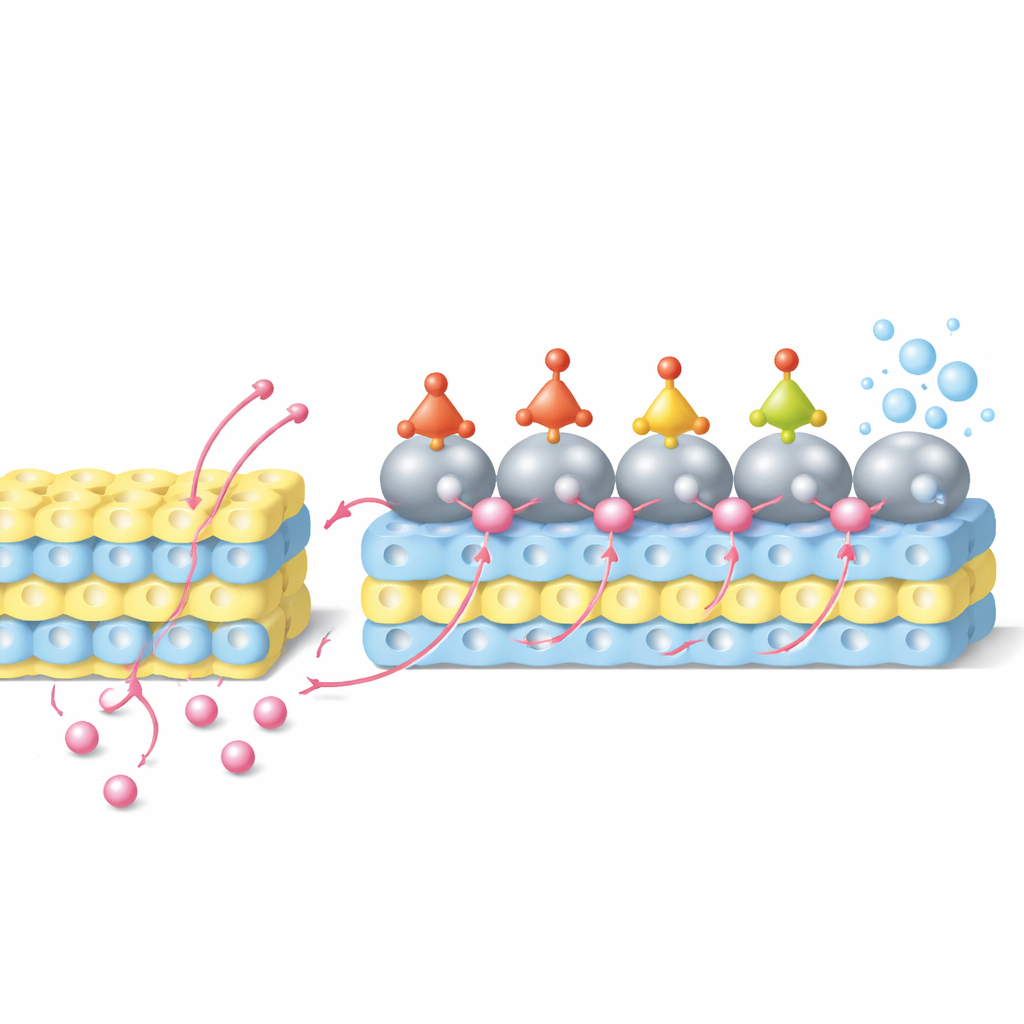
Rendimiento récord y un dispositivo operativo
Porque el soporte actúa como un reservorio y una red de suministro de protones rápida, el catalizador mantiene un suministro de hidrógeno equilibrado y abundante incluso a densidades de corriente muy altas. En solución ácida con nitrato, el electrodo Ru/WO3‑x alcanza una densidad de corriente de 500 miliamperios por centímetro cuadrado a un voltaje aplicado cercano a cero, mientras convierte alrededor del 94 por ciento de la carga eléctrica en amoníaco, valores que superan a los de catalizadores previos reportados para la conversión de nitrato a amoníaco en ácido. La estructura permanece estable durante operaciones prolongadas y casi no se detectan subproductos indeseados de nitrógeno. Para demostrar un uso práctico, el equipo construyó un “batteriolizador” que empareja la reducción de nitrato en este catalizador con la oxidación de sulfuro en otro electrodo. La celda genera simultáneamente energía eléctrica y convierte los contaminantes nitrato y sulfuro en productos útiles a base de amonio y azufre.
Convertir residuos y electricidad en valor
Para un lector no especializado, el mensaje clave es que los autores han hallado una forma ingeniosa de permitir que un material almacene y transporte hidrógeno mientras otro se concentra en transformar nitrato en amoníaco. Al diseñar cómo se mueven los protones —en vez de simplemente hacer un metal más activo— suprimen en gran medida la formación de gas hidrógeno desperdiciado y aumentan la producción de amoníaco en condiciones ácidas duras que se asemejan a corrientes de residuos industriales reales. Este concepto de repartir tareas entre un soporte y un catalizador metálico mediante un derrame de hidrógeno controlado podría aplicarse a muchas otras reacciones electroquímicas, abriendo vías hacia una producción de fertilizantes más limpia y hacia dispositivos que, a la vez, limpien aguas residuales y suministren productos químicos y energía útiles.
Cita: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Palabras clave: síntesis de amoníaco, aguas residuales con nitrato, electrocatalisis, derrame de hidrógeno, catalizador de óxido de tungsteno