Clear Sky Science · pl
Odwrotny rozlew wodoru przyspiesza elektrokatalityczną redukcję azotanów do amoniaku na Ru/WO3-x w środowisku kwaśnym
Czystszy nawóz z brudnej wody
Amoniak jest podstawą współczesnych nawozów i obiecującym nośnikiem wodoru, jednak jego produkcja wciąż opiera się na stulecznej metodzie Habera–Boscha, która zużywa ogromne ilości energii i emituje duże ilości dwutlenku węgla. Jednocześnie wiele gałęzi przemysłu odprowadza kwaśne ścieki bogate w azotany, które mogą szkodzić ekosystemom. W tym badaniu zbadano sposób zamiany tego zanieczyszczenia w zasób: wykorzystanie energii elektrycznej do bezpośredniej konwersji azotanów w kwaśnej wodzie na amoniak, przy jednoczesnym unikaniu marnotrawnej produkcji wodoru gazowego i korozji katalizatora.
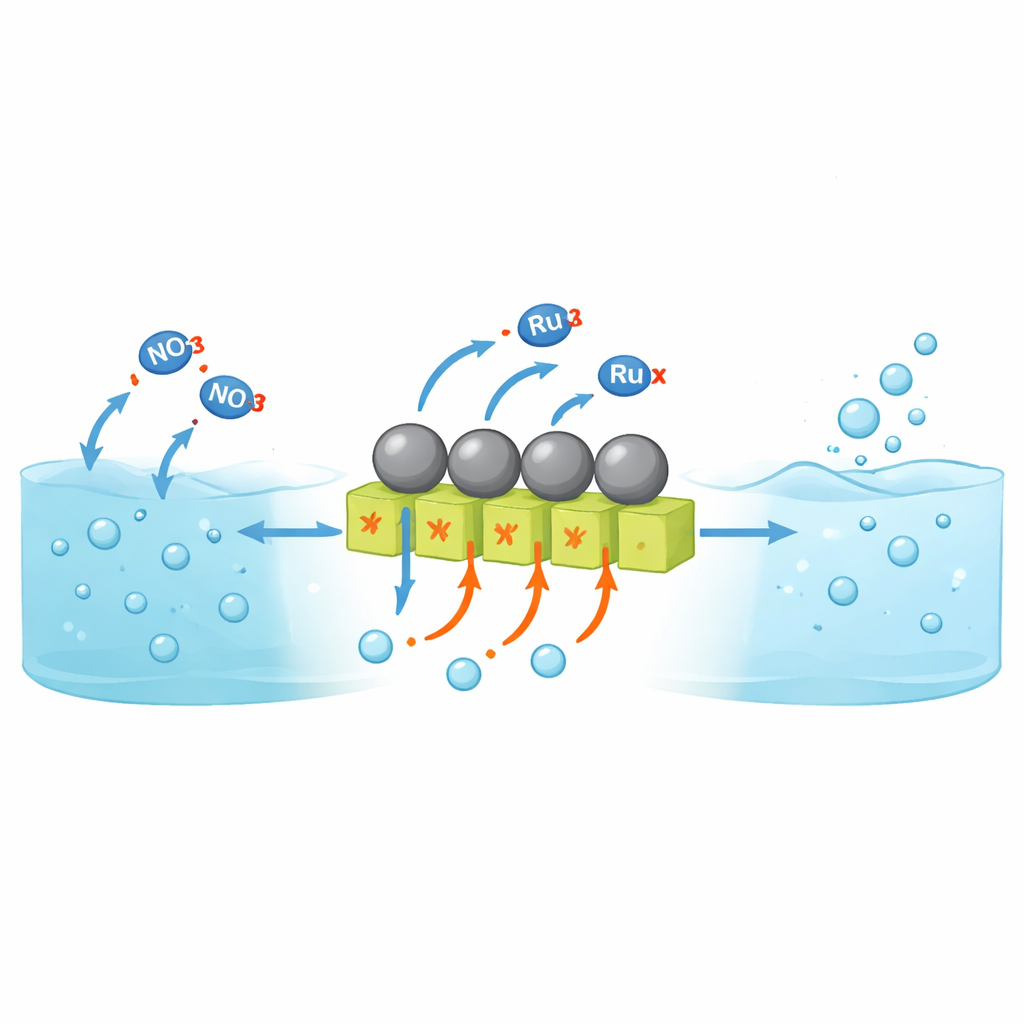
Dlaczego przemiana azotanów w amoniak jest trudna
Elektrochemiczna redukcja azotanów pozwala wytwarzać amoniak w temperaturze pokojowej z wody i strumieni odpadów zamiast z paliw kopalnych w wysokiej temperaturze i pod wysokim ciśnieniem. Jednak większość badań dotyczyła dotąd roztworów obojętnych lub zasadowych. W silnie kwaśnych roztworach — znacznie bliższych rzeczywistym przemysłowym ściekom azotanowym — materiały katalityczne mają tendencję do korodowania, a przyspieszona zostaje inna reakcja: protony łączą się, tworząc wodór gazowy, zamiast uczestniczyć w budowie amoniaku. Konwencjonalne metale odporne na działanie kwasów, takie jak ruten, doskonale wiążą wodór, co sprzyja tworzeniu amoniaku, ale jednocześnie czyni je bardzo aktywnymi w ewolucji wodoru gazowego. W efekcie bardzo niewielka część przepływu prądu przekształca się w amoniak, zwłaszcza przy gęstościach prądu potrzebnych w praktycznych urządzeniach.
Katalizator, który dzieli zadania
Naukowcy zaprojektowali kompozytowy katalizator, który rozdziela miejsca, gdzie obsługiwany jest wodór i azotany, jednocześnie utrzymując je wystarczająco blisko, by mogły współpracować. Na podłożu tytanowym wyhodowali nanorurki tlenku wolframu (WO3‑x), a następnie ozdobili ich powierzchnie drobnymi cząstkami rutenu. Tlenek wolframu jest niezwykle dobry w pochłanianiu protonów z kwaśnego roztworu i przechowywaniu ich w swojej strukturze krystalicznej, ale słabo uwalnia je jako wodór gazowy. Szczegółowa mikroskopia i pomiary rentgenowskie wykazują silne interakcje elektroniczne na granicy między rutenem a tlenkiem wolframu, tworząc liczne miejsca kontaktu, w których struktura elektronowa rutenu ulega subtelnym zmianom, a w tlenku pojawiają się wakancje tlenowe. Zmiany te pomagają określić, gdzie przechowywane są protony i jak się poruszają.
Odwrotny rozlew wodoru w praktyce
W tym systemie protony najpierw wchodzą w sieć tlenku wolframu i są przechowywane blisko powierzchni katalizatora. Pod przyłożonym napięciem przemieszczają się następnie z podłoża tlenkowego z powrotem w kierunku cząstek rutenu — proces określany jako odwrotny rozlew wodoru. Równocześnie jony azotanowe z roztworu adsorbują się na rutenie i są stopniowo uwodorniane przez serię pośrednich związków azotowo-tlenowych, aż do powstania amoniaku. Symulacje komputerowe wykazują, że atomy rutenu na granicy, które przekazały część gęstości elektronowej do wolframu, zapewniają szczególnie sprzyjające miejsca dla etapów dodawania wodoru, obniżając bariery energetyczne kluczowych przekształceń. Eksperymenty z użyciem metod elektrochemicznych, spektroskopii in situ oraz znakowanego izotopowo wodoru potwierdzają, że znacząca część protonów przechowywanych w tlenku faktycznie przemieszcza się do rutenu i uczestniczy w redukcji azotanów zamiast tworzyć gazowy wodór.
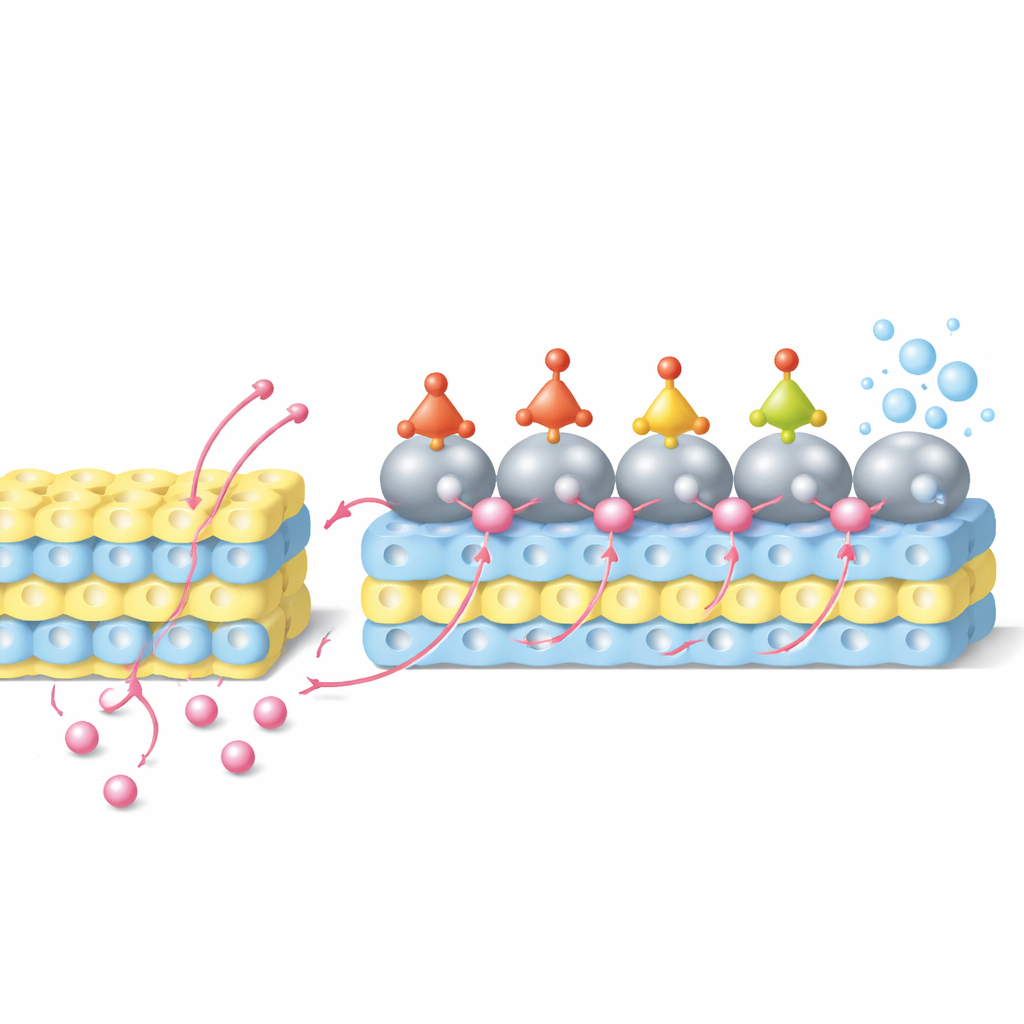
Rekordowa wydajność i działające urządzenie
Dzięki temu, że podłoże działa jako szybki rezerwuar protonów i sieć dostarczająca je do miejsc reakcji, katalizator utrzymuje zrównoważone i obfite zaopatrzenie w wodór nawet przy bardzo wysokich gęstościach prądu. W kwaśnym roztworze azotanowym elektroda Ru/WO3‑x osiąga gęstość prądu 500 miliamperów na centymetr kwadratowy przy niemal zerowym przyłożonym napięciu, jednocześnie przekształcając około 94 procent ładunku elektrycznego w amoniak — wartości przewyższające wcześniej zgłaszane katalizatory do konwersji azotanów na amoniak w warunkach kwaśnych. Struktura pozostaje stabilna podczas długotrwałej pracy, a niemal żadne niepożądane azotowe produkty uboczne nie są wykrywane. Aby wykazać praktyczne zastosowanie, zespół zbudował „batterolyzer”, w którym redukcję azotanów na tym katalizatorze sparowano z utlenianiem siarczków na drugiej elektrodzie. Ogniwo jednocześnie generuje energię elektryczną i przekształca zanieczyszczenia azotanowe i siarczkowe w użyteczne produkty ammoniowe i siarkowe.
Zmiana odpadów i energii w wartość
Dla osoby nietechnicznej kluczowy wniosek jest taki, że autorzy znaleźli sprytny sposób, by jeden materiał przechowywał i transportował wodór, podczas gdy drugi skupia się na przekształcaniu azotanów w amoniak. Poprzez inżynierię ruchu protonów — zamiast jedynie tworzenia bardziej aktywnego metalu — znacznie ograniczyli marnotrawną produkcję wodoru gazowego i zwiększyli wydajność produkcji amoniaku w surowych, kwaśnych warunkach przypominających rzeczywiste strumienie przemysłowych ścieków azotanowych. Ten pomysł dzielenia zadań między podłoże a metaliczny katalizator poprzez kontrolowany rozlew wodoru może zostać zastosowany w wielu innych reakcjach elektrochemicznych, otwierając drogi do czystszej produkcji nawozów oraz do urządzeń, które jednocześnie oczyszczają ścieki i dostarczają użyteczne chemikalia i energię.
Cytowanie: Zhu, W., Lin, YC., Cong, J. et al. Reverse hydrogen spillover accelerates electrocatalytic nitrate reduction to ammonia on Ru/WO3-x in acidic media. Nat Commun 17, 2830 (2026). https://doi.org/10.1038/s41467-026-69335-x
Słowa kluczowe: synteza amoniaku, ścieki z azotanami, elektrokataliza, rozlew wodoru, katalizator tlenku wolframu