Clear Sky Science · pl
Kompresowanie zbiorowej wiedzy ESM do pojedynczego modelu języka białek
Dlaczego ważne jest sprowadzenie wielu modeli białek do jednego
Każdy człowiek nosi miliony drobnych różnic w DNA, z których wiele zmienia pojedyncze cegiełki w białkach. Większość takich zmian jest nieszkodliwa, ale niektóre mogą prowadzić do chorób. Lekarze i badacze potrzebują szybkiego i dokładnego sposobu, by powiedzieć, które zmiany są groźne, używając jedynie sekwencji białkowej. Ten artykuł opisuje nową strategię, która zbiera zbiorową wiedzę wielu istniejących „modeli języka” białek i kompresuje ją do jednego, wydajnego systemu, który dorównuje lub przewyższa obecne najlepsze narzędzia do oceny wpływu zmian genetycznych.
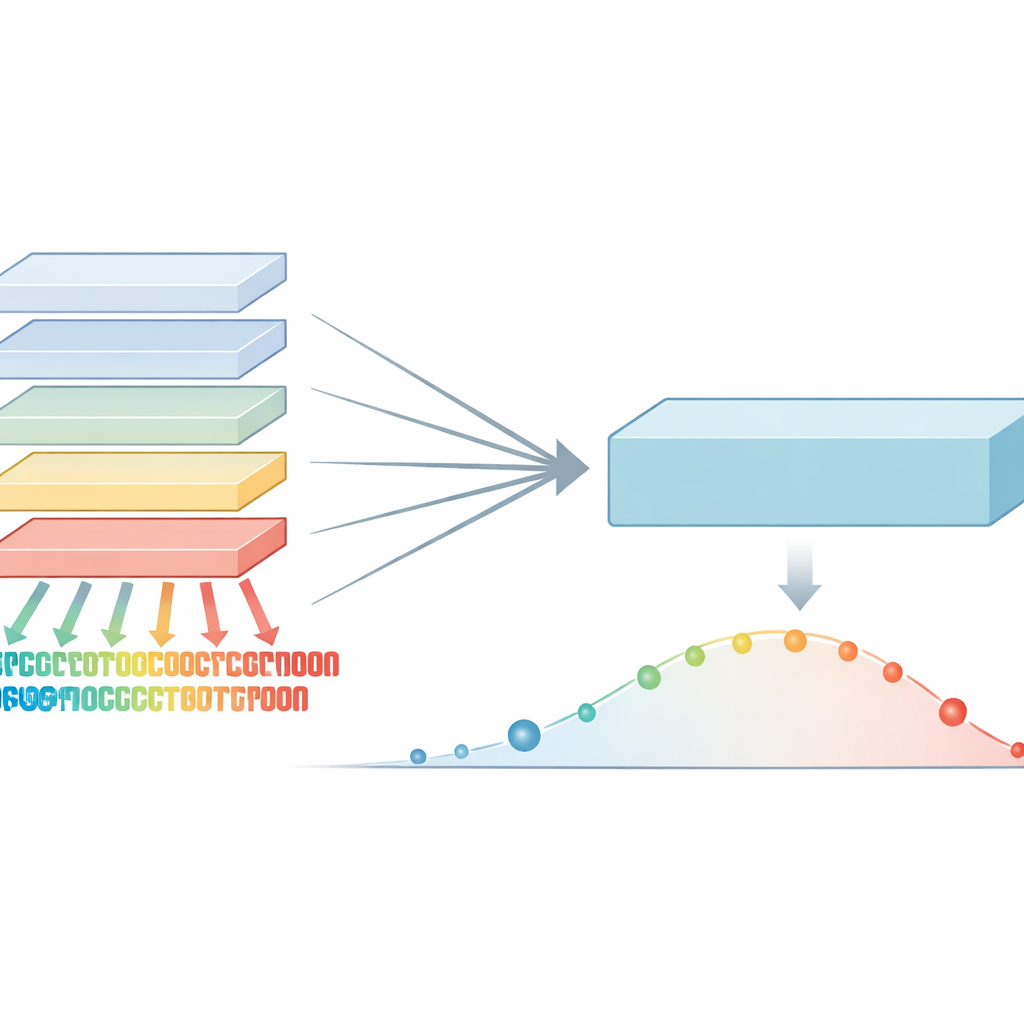
Od czytania zdań do czytania białek
Modele języka białek zapożyczają pomysły z technologii stojącej za nowoczesnymi systemami tłumaczenia i rozmów. Zamiast uczyć się słów w zdaniu, uczą się wzorców w ciągach aminokwasów — „liter” sekwencji białkowych. Trenując na setkach milionów naturalnych białek, modele te wychwytują sygnały o tym, które pozycje są silnie konserwowane, a które tolerują zmiany. Te wzorce można następnie wykorzystać do punktowania wariantów genetycznych: jeśli zmiana narusza wzorzec, który ewolucja mocno chroni, jest bardziej prawdopodobne, że będzie szkodliwa. Do tej pory najsilniejsze metody łączyły te modele z dodatkowymi informacjami, takimi jak struktura 3D czy drzewa ewolucyjne rodzin białek, co czyniło je potężnymi, ale też złożonymi i czasami trudnymi do szerokiego zastosowania.
Pozwalając modelom uczyć się nawzajem
Autorzy zauważyli, że różne modele języka białek, nawet jeśli zbudowane na podobnych danych, mają odrębne mocne strony i słabe punkty. Jeden model może być szczególnie dobry w wykrywaniu wrażliwych regionów w jednej rodzinie białek, podczas gdy inny sprawdza się lepiej gdzie indziej. Zamiast uśredniać ich opinie, zespół wprowadził regułę „maksymalnej pewności”: dla każdej możliwej zmiany białkowej przeglądają całą rodzinę modeli i zachowują ten, który jest najbardziej przekonany, że zmiana jest szkodliwa. Ten krok generuje wzbogacony zestaw ocen, który wychwytuje najsilniejsze ewolucyjne sygnały ostrzegawcze z dowolnego modelu w grupie, zamiast je rozmywać.
Skondensowanie wielu głosów w jednym
Pracując z tym wzbogaconym sygnałem, badacze zaprojektowali proces treningowy, który nazywają ko‑destylacją. W nim wszystkie oryginalne modele wielokrotnie ćwiczą dopasowywanie się do najsilniejszego zbiorowego sygnału, zamieniając się rolami „ucznia” i „nauczyciela” w zależności od tego, gdzie każdy z nich ma największą pewność. W początkowych rundach reguła maksymalnej pewności pomaga wyróżnić subtelne, ale istotne wzorce, które niektóre modele przeoczyły. W późniejszych rundach łagodniejsze uśrednienie pomaga modelom dojść do porozumienia i wygładzić szum. W kilku cyklach jeden duży model stopniowo absorbuje prawie wszystkie użyteczne informacje, które wcześniej były rozproszone po całym zespole. Ten końcowy model, nazwany VESM‑3B, jest potem używany do trenowania mniejszych wersji, które działają wystarczająco szybko na dużych zbiorach genetycznych, zachowując przy tym większość dokładności.
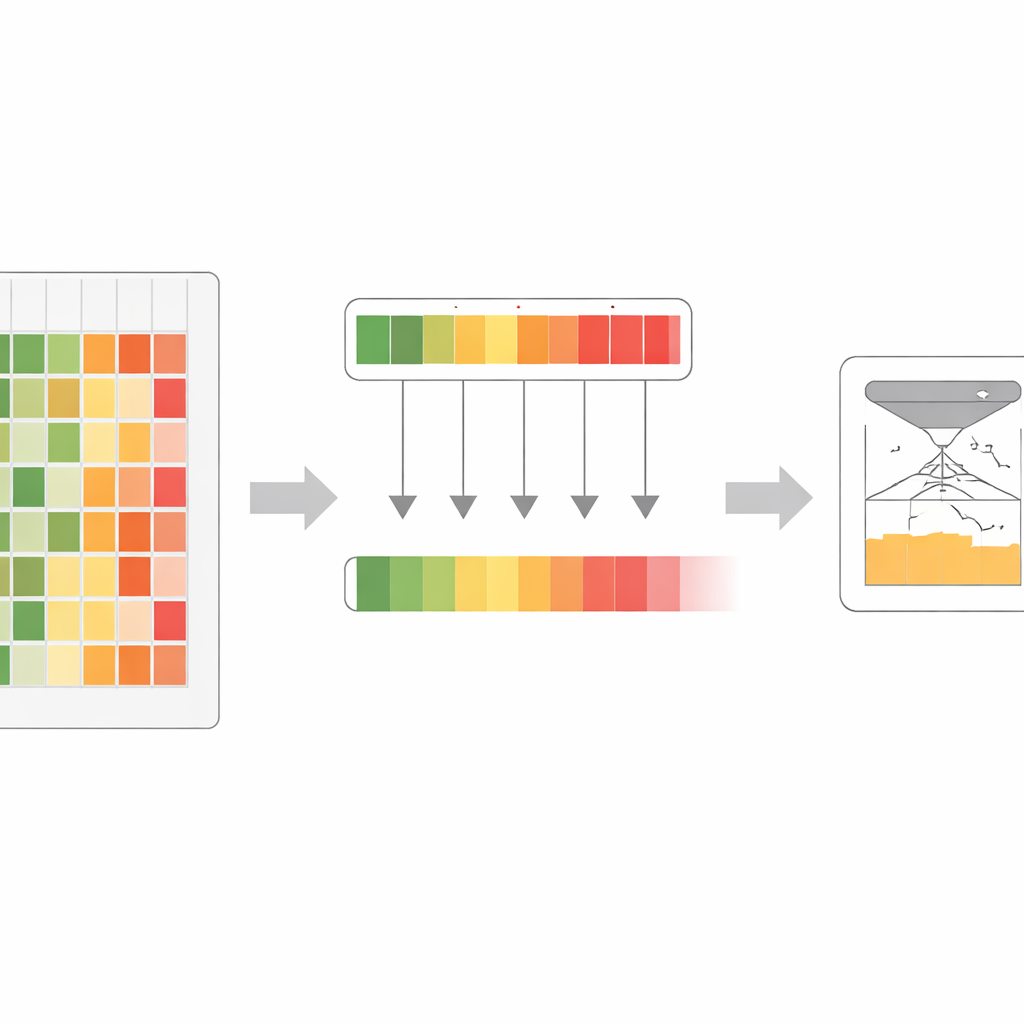
Pokonanie złożonych systemów za pomocą samych sekwencji
Mimo że jako wejście użyto wyłącznie surowych sekwencji białek, modele VESM dorównują lub przewyższają zaawansowanych konkurentów, którzy również polegają na strukturach 3D, ręcznie tworzonych historiach ewolucyjnych czy danych z populacji ludzkich. Na klinicznych benchmarkach pochodzących z bazy ClinVar wariantów chorobowych główny model VESM przewyższa wiele powszechnie używanych narzędzi, a nawet nieznacznie wyprzedza AlphaMissense — niedawny, szeroko omawiany system łączący dane strukturalne i populacyjne. Co kluczowe, wydajność VESM utrzymuje się również dla bardzo rzadkich wariantów — tych, które klinicyści mają najtrudniej interpretować. Modele sprawdzają się także na pomiarach laboratoryjnych testujących, jak mutacje wpływają na wydolność białka, jego stabilność i wiązanie, oraz potrafią śledzić wielkość i kierunek efektów wariantów na rzeczywiste cechy kliniczne w dużych zbiorach biobankowych.
Co to oznacza dla genetyki i medycyny
Poprzez staranne łączenie i ulepszanie mocnych stron wielu modeli sekwencyjnych ta praca pokazuje, że same surowe sekwencje białkowe mogą zawierać wystarczający sygnał do przewidywania wpływu zmian genetycznych na poziomie najnowocześniejszych metod. Efektem jest rodzina narzędzi, które są prostsze we wdrożeniu niż systemy ciężkie od danych strukturalnych czy wymagające dużych zasobów, a jednocześnie pozostają wysoce dokładne w odniesieniu do białek pochodzących od ludzi, drobnoustrojów i wirusów. Dla klinicystów i badaczy oznacza to szybszą i bardziej niezawodną selekcję wariantów DNA, jaśniejszą ocenę tego, jak silnie zmiana może wpływać na cechy związane z chorobą, oraz praktyczny sposób wdrożenia potężnych modeli predykcyjnych w codziennych przepływach pracy w genetyce i projektowaniu białek.
Cytowanie: Dinh, T., Jang, SK., Zaitlen, N. et al. Compressing the collective knowledge of ESM into a single protein language model. Nat Methods 23, 772–784 (2026). https://doi.org/10.1038/s41592-026-03050-9
Słowa kluczowe: modele języka białek, predykcja efektów wariantów, warianty genetyczne, sygnały ewolucyjne, genomika kliniczna