Clear Sky Science · nl
In-silico identificatie van genetische varianten geassocieerd met chronische lymfatische leukemie voor diagnostische en therapeutische toepassingen
Waarom het volgen van kanker in ons DNA ertoe doet
Chronische lymfatische leukemie (CLL) is de meest voorkomende leukemie bij volwassenen, maar blijft voor veel patiënten ongeneeslijk. Families van mensen met CLL lopen een aanzienlijk hoger risico, wat erop wijst dat erfelijke DNA-veranderingen de basis voor de ziekte mede vormen. Deze studie stelt een praktische vraag: kunnen we grootschalige genetische gegevens en computeranalyses gebruiken om de belangrijkste kwetsbare plekken in ons DNA te identificeren die CLL aandrijven — en deze vervolgens koppelen aan bestaande of veelbelovende geneesmiddelen? De antwoorden kunnen vroege diagnose verbeteren en wijzen op preciezere behandelingen met minder trial-and-error.
Over duizenden genomen heen kijken
De onderzoekers begonnen met het verzamelen van samenvattende resultaten van drie grote genome-wide associatiestudies, die het DNA van vele mensen met en zonder CLL scannen om kleine verschillen te vinden die samenhangen met het ziekte‑risico. Door deze datasets zorgvuldig schoon te maken en samen te voegen, allemaal gebaseerd op hetzelfde menselijke referentiegenoom, verhoogden ze de statistische kracht om subtiele genetische signalen op te sporen. Met een meta-analysemethode die studies weegt op basis van de precisie van hun schattingen, identificeerden ze 2.357 DNA-posities, zogenaamde enkelvoudige nucleotidepolymorfismen (SNP’s), die sterk geassocieerd waren met CLL. Deze signalen clusteren in 40 genomische regio’s, waaronder 11 gebieden die eerder niet aan de ziekte waren gekoppeld.
Van DNA-markers naar sleutelsignaalgenen
De meeste risicomarkers lagen tussen genen of in niet-coderende delen van genen, waar hun effecten niet direct zichtbaar zijn. Om ze te interpreteren gebruikte het team bioinformatische gereedschappen die elk marker koppelen aan nabijgelegen genen of aan genen waarvan de activiteit in bloedcellen verandert wanneer die marker aanwezig is. Deze toewijzing leverde 60 genen op die zich in of nabij de risicoregions bevinden. De onderzoekers vroegen vervolgens welke van deze genen centrale posities innemen in het netwerk van eiwit‑eiwitinteracties binnen cellen. Een netwerkanalyse belichtte zeven genen — TERT, BCL2, BCL2L11, CFLAR, CASP8, LEF1 en FAS — als knooppunten die veel paden verbinden. Onafhankelijke ziekte‑databanken ondersteunden sterke verbanden tussen deze genen en CLL, evenals andere bloedkankers en immuunaandoeningen.
Hoe verstoorde celdood leukemie voedt
Bij het bekijken van de functies van deze zeven genen kwam een duidelijk thema naar voren: de meeste regelen of cellen overleven of afsterven. Verschillende, waaronder BCL2 en BCL2L11, behoren tot een familie die overlevingssignalen in evenwicht brengt met zelfvernietigingssignalen in de energiecentrales van de cel, de mitochondriën. Andere — FAS, CFLAR en CASP8 — sturen een parallelle “doodreceptor”route aan aan het celoppervlak. In CLL kantelt dit mechanisme richting overleving: pro‑overlevingsproteïnen zijn overactief, terwijl pro‑doodpartners geblokkeerd of verminderd zijn. Het resterende sleutelgen, LEF1, zit in een groeipad dat leukemiecellen helpt door te gaan met delen. Toen de onderzoekers verrijkingsanalyses uitvoerden, waren de belangrijkste biologische thema’s celdood, kankerpaden en immuunsignalering, wat het idee versterkt dat erfelijke varianten deze regelsystemen aanduwen richting levensvatbare, abnormale B‑cellen.
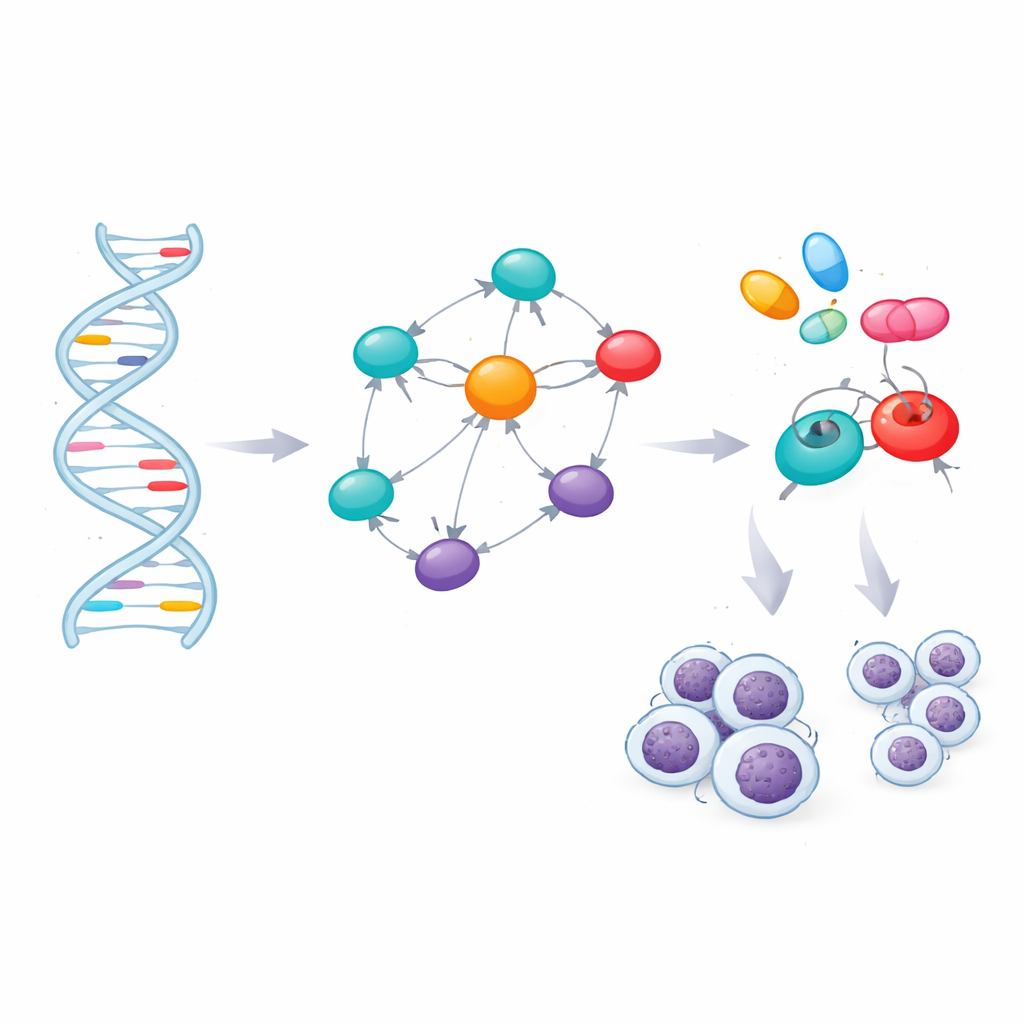
Genen koppelen aan geneesmiddelen
Het identificeren van cruciale genen opent de deur naar gerichte therapie, maar alleen als die genen door geneesmiddelen te beïnvloeden zijn. Het team evalueerde de driedimensionale structuren van de zeven eiwitten en vond veelbelovende holtes waar kleine moleculen aan kunnen binden. Ze doorzochten vervolgens een bibliotheek van 166 bestaande of experimentele verbindingen die verbonden zijn met CLL of aanverwante aandoeningen en gebruikten moleculaire docking‑simulaties om te zien welke geneesmiddelen het beste in de sleutelproteïnen of hun belangrijkste regelaars pasten. Na het rangschikken van deze virtuele interacties filtreerden ze de topkandidaten met behulp van gangbare regels voor “drug‑likeness” en computermodellen die voorspellen hoe goed een verbinding geabsorbeerd, verdeeld, gemetaboliseerd en uitgescheiden wordt en hoe toxisch het kan zijn. Deze conservatieve selectie liet vier sterke kanshebbers over: de reeds goedgekeurde kankergeneesmiddelen ibrutinib, selinexor, imatinib en avapritinib.
Wat dit voor patiënten kan betekenen
Voor mensen die met CLL leven verandert dit werk nog niet direct de dagelijkse zorg, maar het helpt de verbindingen te leggen tussen erfelijk risico, de interne bedrading van leukemiecellen en de geneesmiddelen die dat netwerk het beste kunnen ontregelen. Twee van de uitgelichte geneesmiddelen, ibrutinib en selinexor, worden al in CLL gebruikt en werken op manieren die passen bij het genetische beeld dat hier is onthuld, met name door het evenwicht terug te keren naar celdood van kankercellen. De studie suggereert ook dat imatinib en avapritinib, momenteel gebruikt bij andere kankers, nader onderzoek in CLL verdienen. Breder gezien toont de aanpak hoe het delven in bestaande genetische data met krachtige computationele tools sleutelziegens en potentiële therapieën kan onthullen, en zo toekomstige laboratoriumexperimenten en klinische studies kan richten op de meest veelbelovende doelwitten.
Bronvermelding: Islam, M.S., Mollah, M.H., Ahsan, M.A. et al. In-silico identification of genetic variants associated with chronic lymphocytic leukemia for diagnostic and therapeutic applications. Sci Rep 16, 14545 (2026). https://doi.org/10.1038/s41598-026-45456-7
Trefwoorden: chronische lymfatische leukemie, genetische risicovarianten, apoptosepaden, hergebruik van geneesmiddelen, gerichte kankertherapie