Clear Sky Science · es
Identificación in silico de variantes genéticas asociadas con la leucemia linfocítica crónica para aplicaciones diagnósticas y terapéuticas
Por qué importa rastrear el cáncer en nuestros genes
La leucemia linfocítica crónica (LLC) es la leucemia adulta más frecuente, pero sigue siendo incurable para muchos pacientes. Las familias de personas con LLC presentan un riesgo marcadamente mayor, lo que sugiere que cambios heredados en el ADN contribuyen a crear el terreno para la enfermedad. Este estudio plantea una pregunta práctica: ¿podemos usar datos genéticos a gran escala y análisis computacionales para señalar los puntos débiles clave en nuestro ADN que impulsan la LLC—y luego relacionarlos con fármacos existentes o prometedores? Las respuestas podrían mejorar el diagnóstico temprano y orientar tratamientos más precisos, con menos prueba y error.
Analizando miles de genomas
Los investigadores empezaron recopilando resultados resumen de tres grandes estudios de asociación del genoma completo, que examinan el ADN de muchas personas con y sin LLC para encontrar pequeñas diferencias vinculadas al riesgo de la enfermedad. Al limpiar y fusionar cuidadosamente estos conjuntos de datos, todos basados en la misma referencia genómica humana, aumentaron la potencia estadística para detectar señales genéticas sutiles. Empleando un método de metaanálisis que pondera los estudios según la precisión de sus estimaciones, identificaron 2.357 posiciones en el ADN, llamadas polimorfismos de un solo nucleótido, que se asociaban fuertemente con la LLC. Estas señales se agruparon en 40 tramos del genoma, incluidos 11 regiones que no se habían relacionado antes con la enfermedad.
De marcadores de ADN a genes reguladores clave
La mayoría de los marcadores de riesgo se ubicaron entre genes o en partes no codificantes de los genes, donde sus efectos no son obvios. Para interpretarlos, el equipo usó herramientas de bioinformática que vinculan cada marcador con genes cercanos o con genes cuya actividad en células sanguíneas cambia cuando ese marcador está presente. Este mapeo produjo 60 genes que se sitúan dentro o cerca de las regiones de riesgo. Los científicos preguntaron entonces cuáles de estos genes ocupan posiciones centrales en la red de contactos proteína–proteína dentro de las células. Un análisis de redes destacó siete genes—TERT, BCL2, BCL2L11, CFLAR, CASP8, LEF1 y FAS—como nodos que conectan muchas vías. Bases de datos independientes de enfermedades respaldaron fuertes vínculos entre estos genes y la LLC, así como con otros cánceres hematológicos y trastornos inmunitarios.
Cómo la alteración de la muerte celular alimenta la leucemia
Al examinar la función de estos siete genes, surgió un tema claro: la mayoría controlan si las células viven o mueren. Varios, incluidos BCL2 y BCL2L11, pertenecen a una familia que equilibra las señales de supervivencia con las de autodestrucción en las centrales energéticas de la célula, las mitocondrias. Otros—FAS, CFLAR y CASP8—gobiernan una ruta alternativa de “receptores de la muerte” en la superficie celular. En la LLC, esta maquinaria se inclina hacia la supervivencia: las proteínas pro-supervivencia están sobreactivas, mientras que las contrapartes pro-muerte están bloqueadas o reducidas. El gen clave restante, LEF1, forma parte de una vía de crecimiento que ayuda a las células leucémicas a seguir dividiéndose. Cuando los investigadores realizaron análisis de enriquecimiento, los temas biológicos principales fueron la muerte celular, las vías del cáncer y la señalización inmune, lo que refuerza la idea de que las variantes heredadas empujan estos sistemas de control hacia linfocitos B anormales y de larga vida.
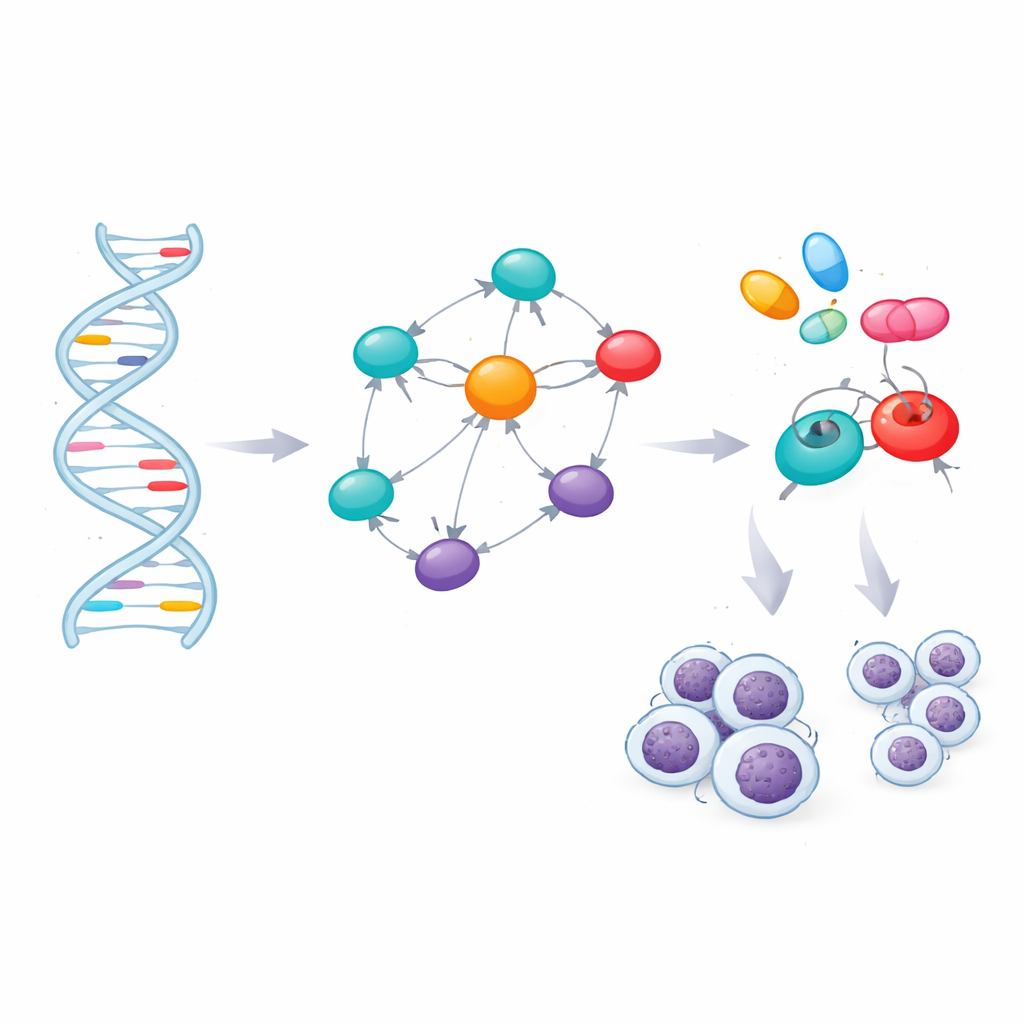
Relacionando genes con medicamentos
Identificar genes cruciales abre la puerta a la terapia dirigida, pero solo si esos genes pueden ser modulados por fármacos. El equipo evaluó las estructuras tridimensionales de las siete proteínas y encontró cavidades prometedoras donde podrían unirse pequeñas moléculas. Luego revisaron una biblioteca de 166 compuestos existentes o experimentales vinculados a la LLC o a condiciones relacionadas y usaron simulaciones de acoplamiento molecular para ver qué fármacos encajaban mejor en las proteínas clave o en sus principales reguladores. Tras clasificar estas interacciones virtuales, filtraron los mejores candidatos mediante reglas estándar de “características de fármaco” y por modelos computacionales que predicen la absorción, distribución, metabolismo, excreción y toxicidad de un compuesto. Este cribado conservador dejó cuatro candidatos sólidos: los fármacos oncológicos ya aprobados ibrutinib, selinexor, imatinib y avapritinib.
Qué podría significar esto para los pacientes
Para las personas con LLC, este trabajo aún no cambia la atención cotidiana, pero ayuda a conectar los puntos entre el riesgo heredado, el cableado interno de las células leucémicas y los medicamentos que podrían interrumpir mejor ese cableado. Dos de los fármacos destacados, ibrutinib y selinexor, ya se usan en LLC y actúan de formas coherentes con el panorama genético revelado aquí, especialmente al inclinar la balanza de nuevo hacia la muerte de células cancerosas. El estudio también sugiere que imatinib y avapritinib, empleados actualmente en otros cánceres, podrían merecer pruebas más cercanas en LLC. Más en general, el enfoque muestra cómo explotar datos genéticos existentes con potentes herramientas computacionales puede revelar genes clave de la enfermedad y reducir el campo de terapias potenciales, orientando futuros experimentos de laboratorio y ensayos clínicos hacia los objetivos más prometedores.
Cita: Islam, M.S., Mollah, M.H., Ahsan, M.A. et al. In-silico identification of genetic variants associated with chronic lymphocytic leukemia for diagnostic and therapeutic applications. Sci Rep 16, 14545 (2026). https://doi.org/10.1038/s41598-026-45456-7
Palabras clave: leucemia linfocítica crónica, variantes genéticas de riesgo, vías de apoptosis, reutilización de fármacos, terapia dirigida contra el cáncer