Clear Sky Science · zh
基于糖链的生物降解剂靶向细胞因子免疫轴
关闭失控的炎症反应
从类风湿性关节炎到某些癌症,许多难治疾病都由一类小型信使蛋白——细胞因子——持续激活免疫系统而加剧。现有药物大多试图阻断这些信号分子,但在病情严重时,单纯中和可能无法应对过量的信号。本研究探讨了一种不同的设想:与其仅仅削弱信号,能否通过将这些有害分子送入体内细胞的“回收中心”进行破坏,从血液中物理性地移除它们?
移除问题分子的全新途径
研究者聚焦于强效炎性细胞因子白细胞介素‑6(IL‑6)及其可溶性受体,这两者共同驱动多种慢性与急性免疫疾病。团队没有去设计另一种阻断抗体,而是构建“生物降解剂”(BioDegs)。这些基于蛋白的工具(如抗体或小型抗体片段)先结合IL‑6或其受体,然后搭乘运送通路前往肝脏。在肝脏中,它们通过一个基于糖的“把手”与肝细胞表面的天然受体结合,将细胞因子一并拉入细胞的废物处理系统进行分解。
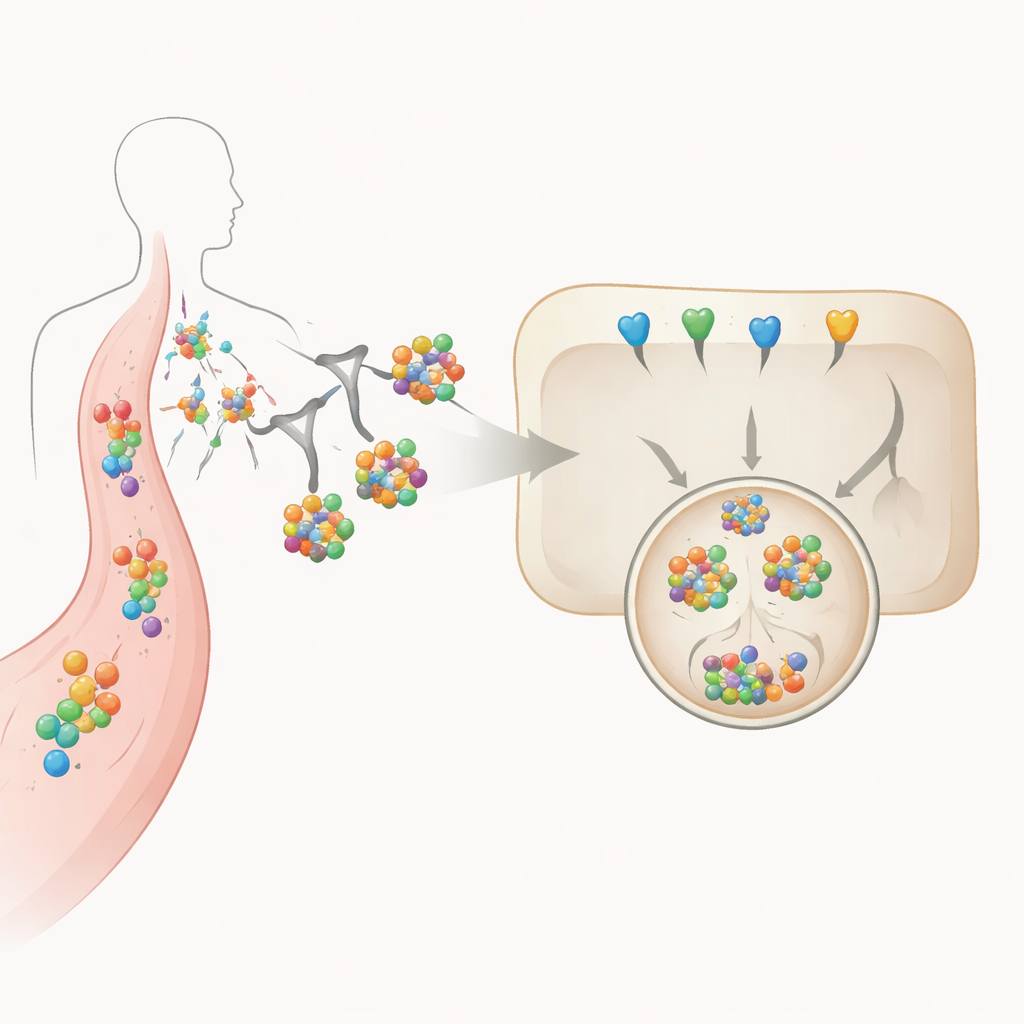
用糖作精确递送标签
该方法的核心是一种附着在降解剂蛋白上的三叉糖结构。这种糖被一种主要存在于肝细胞上的偶氨基糖蛋白受体(asialoglycoprotein receptor)特异识别。当带糖标签的降解剂在血液中结合IL‑6或其受体时,整个复合物会被牵引到肝细胞表面,被吞噬并通过细胞内不同区室运输到溶酶体——一个充满消化酶的酸性囊泡。作者系统地改变了糖基数量以及承载糖基的蛋白“骨架”类型,测定这些设计选择如何影响稳定性、结合力、细胞摄取以及在类肝细胞培养体系中IL‑6的实际降解情况。
测试不同的生物降解剂构型
团队比较了几种格式:已有针对IL‑6或其受体的全尺寸治疗性抗体、一种结合IL‑6的骆驼科单域抗体片段(称为VHH),以及被改造为诱饵的可溶性IL‑6受体。所有这些都以不同程度化学修饰上三叉糖。在天然携带相关糖受体的肝癌细胞培养物中,带糖标签的抗体和VHH能够成功将IL‑6或其受体拖入细胞并引向溶酶体。附着的糖基越多(在一定范围内),复合物被内吞的效率越高,约一天内培养基中IL‑6的含量下降越明显。值得注意的是,尽管VHH基降解剂可附着的糖位点较少,但由于其紧凑的形状更易形成有利于摄取的复合体,因此在内化和清除IL‑6方面表现尤其出色。
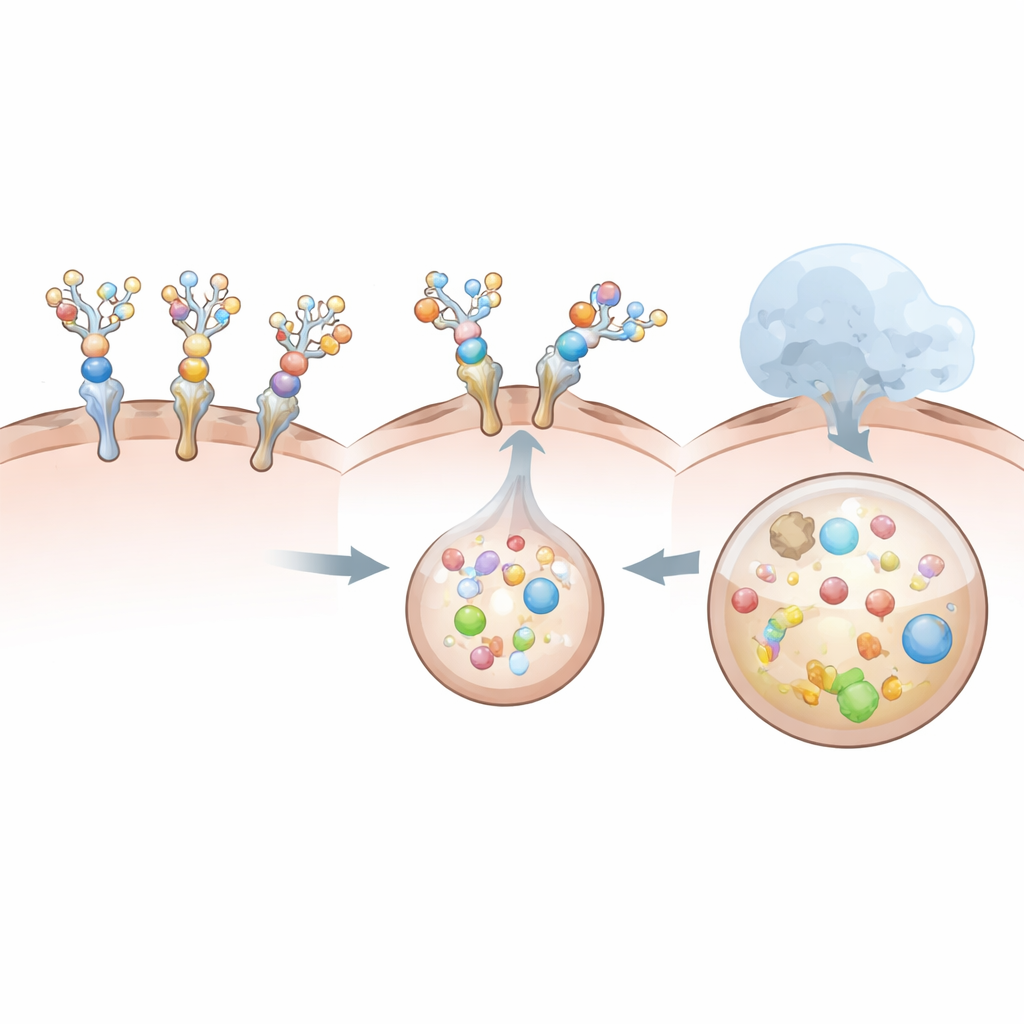
为何某些设计优于其他设计
并非所有降解剂的表现都相同。基于可溶性受体的设计虽然能被肝细胞摄取,但作为IL‑6的“护送者”表现不佳。其与IL‑6的天然相互作用相对较弱且持续时间短,而大量糖修饰进一步削弱了这种结合。因此,这种诱饵受体往往单独被内化,而大多数IL‑6仍留在细胞外,几乎未受影响。相比之下,抗体和VHH降解剂即便在糖基附件后仍能与IL‑6保持极强的结合力,同时与肝受体的相互作用也足以确保细胞因子与降解剂一同被内化。这些比较表明,单纯结合目标并不足够:降解剂、其靶标与肝受体之间的整体几何形状、尺寸与协同性,都会影响复合物是否能够被高效吞噬并破坏。
展望更聪明的炎症控制策略
对非专业读者而言,核心信息是:未来有望不仅阻断像IL‑6这样的炎性信号,还能通过将它们重新定向到肝脏的天然清除机制,有选择性地“吸净”血液循环中的这些分子。本研究为设计此类基于糖链的降解剂提供了实用路线图,展示了哪些分子特征能提升其效能、哪些则效果欠佳。长期来看,优化这些设计或可开发出在严重关节炎、细胞因子风暴或某些癌症等疾病中更彻底清除致病细胞因子的药物,同时借助肝脏作为安全的定点清理中心以减少对健康组织的影响。
引用: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
关键词: 靶向蛋白降解, 白细胞介素‑6, 溶酶体运输, 细胞外降解剂, 免疫疗法