Clear Sky Science · fr
Dégradeurs biologiques à base de glycanes ciblant l’axe immunitaire des cytokines
Éteindre l’inflammation incontrôlée
De nombreuses maladies difficiles à traiter, de la polyarthrite rhumatoïde à certains cancers, sont alimentées par de petites protéines messagères appelées cytokines qui maintiennent le système immunitaire en état d’activation. Les traitements actuels cherchent principalement à bloquer ces messagers, mais en cas de maladie sévère le signal à neutraliser peut simplement être trop intense. Cette étude explore une idée différente : au lieu de se contenter d’atténuer le signal, peut-on physiquement éliminer ces molécules problématiques de la circulation en les envoyant vers les « centres de recyclage » cellulaires du corps pour y être détruites ?
Une nouvelle manière d’éliminer les molécules problématiques
Les chercheurs se concentrent sur l’interleukine‑6 (IL‑6), une cytokine inflammatoire puissante, et son récepteur soluble, qui ensemble pilotent de nombreux troubles immunitaires chroniques et aigus. Plutôt que de concevoir un énième anticorps bloqueur, l’équipe met au point des « dégradeurs biologiques », ou BioDegs. Il s’agit d’outils protéiques, comme des anticorps ou de petits fragments d’anticorps, qui s’attachent d’abord à l’IL‑6 ou à son récepteur puis se rendent au foie. Là, ils utilisent une poignée à base de sucre pour s’accrocher à un récepteur naturel des cellules hépatiques, entraînant la cytokine dans le système d’élimination de la cellule pour sa dégradation.
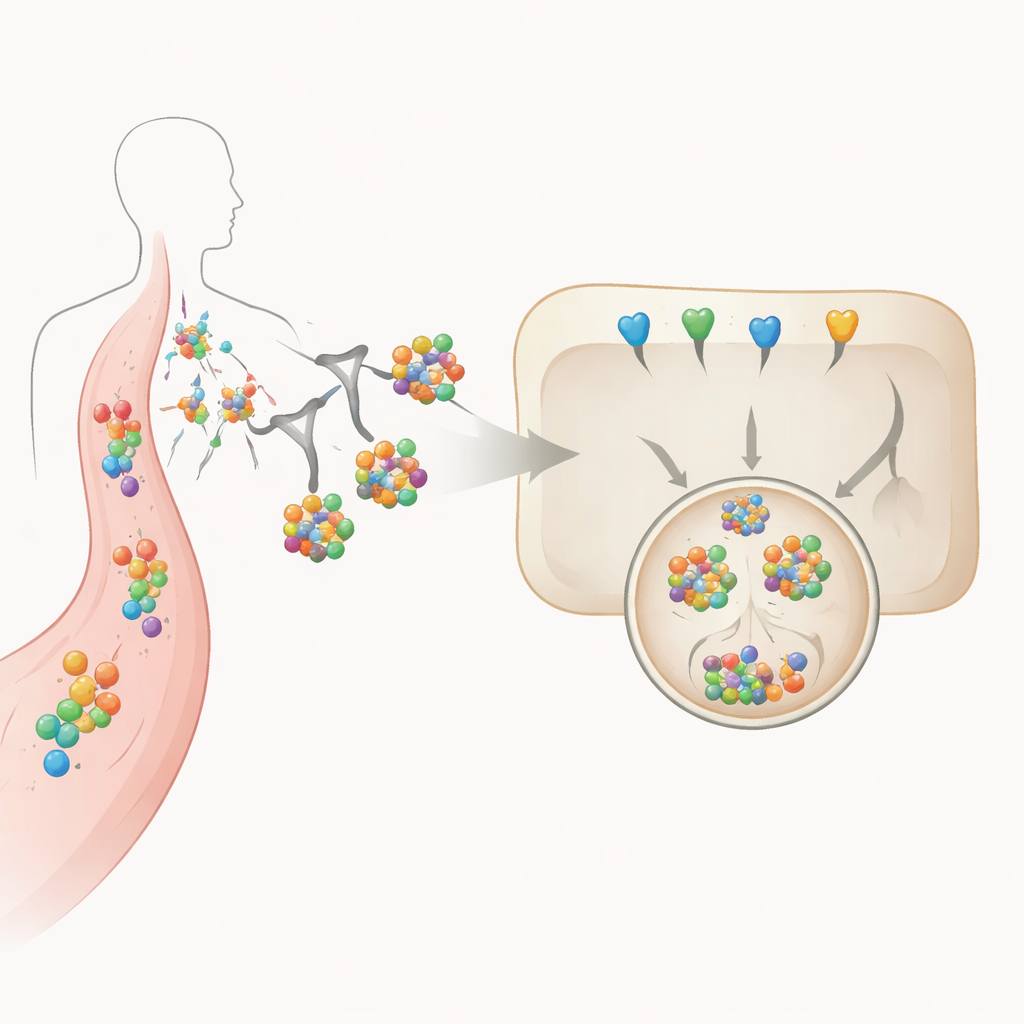
Utiliser des sucres comme étiquettes de livraison de précision
Au cœur de cette approche se trouve une structure sucrée tri‑branche fixée aux protéines dégradeuses. Ce sucre est spécifiquement reconnu par le récepteur des asialoglycoprotéines, une molécule présente principalement sur les cellules du foie. Lorsqu’un dégradeur marqué par ce sucre se lie à l’IL‑6 ou à son récepteur dans la circulation, l’ensemble est attiré vers la surface des cellules hépatiques, internalisé, puis acheminé à travers des compartiments internes jusqu’au lysosome, une vésicule acide riche en enzymes digestives. Les auteurs varient de façon systématique le nombre de groupes sucrés attachés et le « châssis » protéique qui les porte, puis mesurent comment ces choix de conception influent sur la stabilité, l’affinité, l’absorption cellulaire et la destruction effective de l’IL‑6 dans des cellules de type hépatique cultivées en laboratoire.
Tester différents designs de dégradeurs biologiques
L’équipe compare plusieurs formats : des anticorps thérapeutiques de pleine taille ciblant déjà l’IL‑6 ou son récepteur, un fragment d’anticorps monodomaines de camélidé compact (connu sous le nom de VHH) qui se lie à l’IL‑6, et une version soluble du récepteur de l’IL‑6 réutilisée comme leurre. Tous sont chimiquement décorés de la structure sucrée tri‑branche en quantités graduées. Dans des cellules de cancer du foie cultivées qui portent naturellement le récepteur sucré pertinent, les anticorps et le VHH marqués entraînent avec succès l’IL‑6 ou son récepteur à l’intérieur des cellules et les dirigent vers les lysosomes. Plus il y a de groupes sucrés attachés (dans certaines limites), plus l’internalisation des complexes est efficace, et plus l’IL‑6 disparaît du milieu environnant sur environ une journée. Fait notable, le petit dégradeur basé sur le VHH, malgré un plus faible nombre de sites d’attachement sucrés, se révèle particulièrement efficace pour internaliser et éliminer l’IL‑6, probablement parce que sa forme compacte favorise la formation d’un complexe mieux adapté à l’absorption.
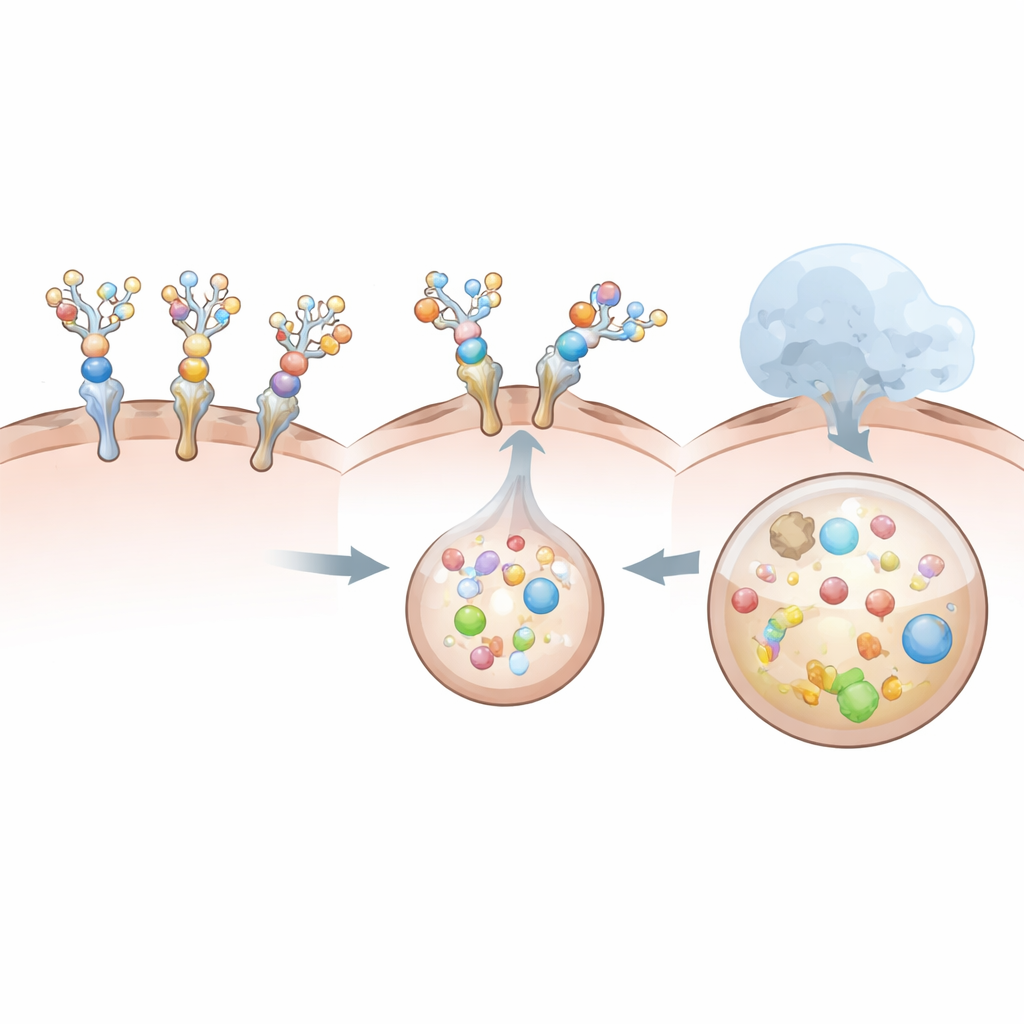
Pourquoi certains designs fonctionnent mieux que d’autres
Tous les dégradeurs ne sont pas également performants. Le design à base de récepteur soluble, bien qu’il soit facilement internalisé par les cellules hépatiques, s’avère être un médiocre escorteur pour l’IL‑6 lui‑même. Son interaction naturelle avec l’IL‑6 est relativement faible et de courte durée, et une forte décoration sucrée déstabilise encore davantage cette liaison. En conséquence, le récepteur leurre est internalisé seul tandis que la plupart de l’IL‑6 reste à l’extérieur, en grande partie intacte. En revanche, les dégradeurs à base d’anticorps et de VHH lient l’IL‑6 très fortement même après l’ajout des sucres, et interagissent suffisamment avec le récepteur hépatique pour garantir que la cytokine et le dégradeur soient internalisés ensemble. Ces comparaisons montrent que se contenter de lier une cible ne suffit pas : la géométrie globale, la taille et la coopération entre le dégradeur, sa cible et le récepteur hépatique déterminent si le complexe est efficacement englouti et détruit.
Perspectives pour un contrôle plus intelligent de l’inflammation
Pour un non-spécialiste, le message principal est qu’il pourrait bientôt être possible non seulement de bloquer des signaux inflammatoires comme l’IL‑6, mais de les « aspirer » sélectivement hors de la circulation en les redirigeant vers la machinerie d’élimination naturelle du foie. Cette étude propose une feuille de route pratique pour concevoir de tels dégradeurs à base de glycane, montrant quelles caractéristiques moléculaires les rendent les plus efficaces et lesquelles sont moins adaptées. À long terme, l’affinement de ces designs pourrait conduire à des médicaments qui éliminent plus complètement les cytokines responsables de la maladie dans des affections telles que l’arthrite sévère, les orages cytokiniques ou certains cancers, tout en préservant les tissus sains en exploitant le foie comme centre de nettoyage ciblé et sûr.
Citation: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
Mots-clés: dégradation ciblée des protéines, interleukine-6, trafic lysosomal, dégradeurs extracellulaires, immunothérapie