Clear Sky Science · de
Glykanbasierte biologische Degrader, die die Zytokin-Immunachse anvisieren
Die Abschaltung von unkontrollierter Entzündung
Viele schwer behandelbare Erkrankungen, von rheumatoider Arthritis bis zu bestimmten Krebsarten, werden von kleinen Botenproteinen, sogenannten Zytokinen, angetrieben, die das Immunsystem dauerhaft aktiviert halten. Die heutigen Medikamente versuchen meist, diese Botenstoffe zu blockieren, doch bei schweren Verläufen ist das Signal oft zu stark, um es allein zu neutralisieren. Diese Studie untersucht einen anderen Ansatz: Statt das Signal nur zu dämpfen, kann man diese problematischen Moleküle körperlich aus dem Blutkreislauf entfernen, indem man sie zu den zellulären „Recyclingzentren“ des Körpers schickt, wo sie zerstört werden?
Ein neuer Weg, problematische Moleküle zu entfernen
Die Forscher konzentrieren sich auf Interleukin‑6 (IL‑6), ein starkes entzündungsförderndes Zytokin, und seinen löslichen Rezeptor, die zusammen viele chronische und akute Immunstörungen antreiben. Anstatt einen weiteren blockierenden Antikörper zu entwickeln, bauen sie „biologische Degrader“ oder BioDegs. Dabei handelt es sich um proteinbasierte Werkzeuge, wie Antikörper oder kleine Antikörperfragmente, die zunächst IL‑6 oder dessen Rezeptor binden und dann eine Fahrt zur Leber antreten. Dort nutzen sie einen glykanbasierten Griff, um an einen natürlichen Rezeptor auf Leberzellen anzudocken und das Zytokin in das intrazelluläre Entsorgungssystem zur Zersetzung zu ziehen.
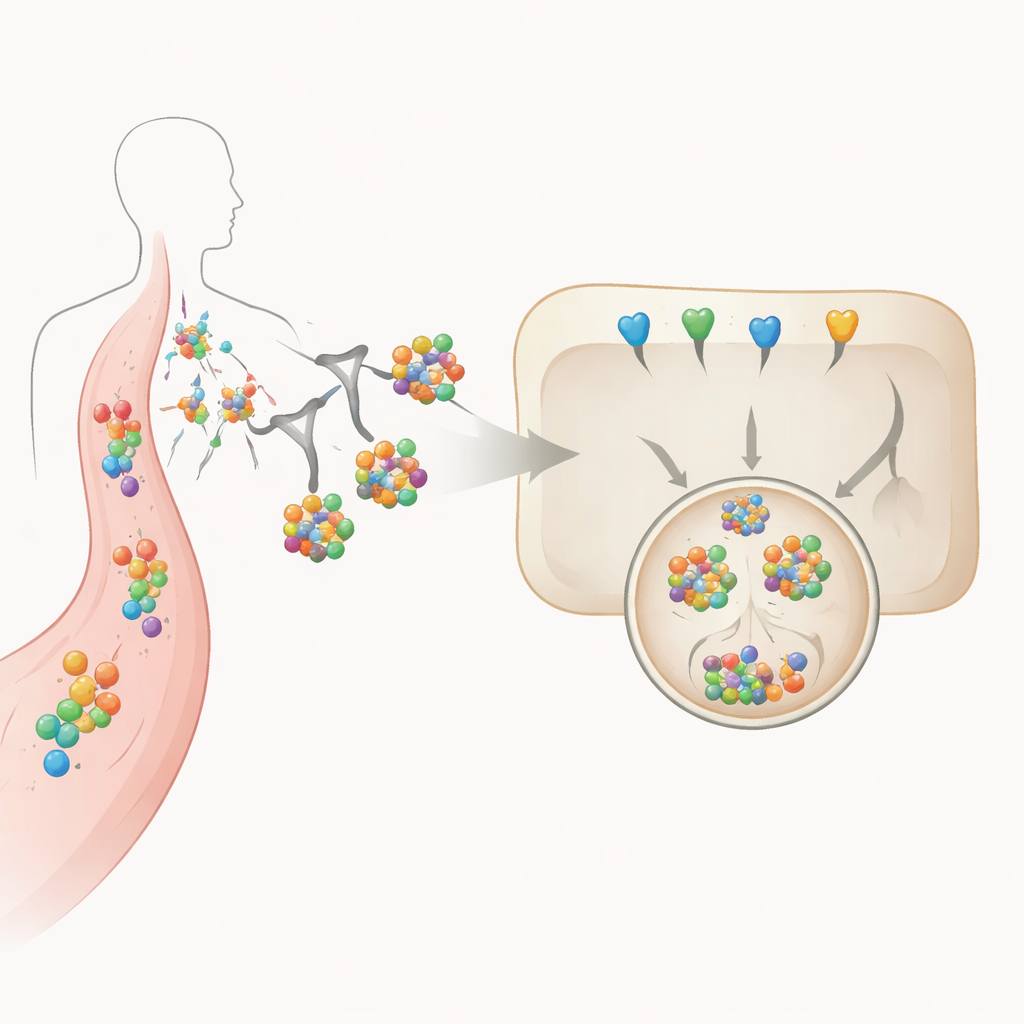
Zucker als präzise Lieferetiketten
Im Kern dieses Ansatzes steht eine dreifach verzweigte Zuckerstruktur, die an die Degrader-Proteine angehängt wird. Dieser Zucker wird spezifisch vom Asialoglykoprotein-Rezeptor erkannt, einem Molekül, das hauptsächlich auf Leberzellen vorkommt. Wenn der zuckermarkierte Degrader IL‑6 oder dessen Rezeptor im Blut bindet, wird der gesamte Komplex zur Leberzelloberfläche gezogen, aufgenommen und durch interne Kompartimente zum Lysosom transportiert, einem sauren Vesikel voller Verdauungsenzyme. Die Autoren variieren systematisch, wie viele Zuckergruppen angebracht sind und welches Protein‑„Gerüst“ sie tragen, und messen dann, wie diese Designentscheidungen Stabilität, Bindungsstärke, zelluläre Aufnahme und den tatsächlichen Abbau von IL‑6 in im Labor gezüchteten leberähnlichen Zellen beeinflussen.
Test verschiedener Designs biologischer Degrader
Das Team vergleicht mehrere Formate: vollwertige therapeutische Antikörper, die bereits IL‑6 oder dessen Rezeptor anvisieren, ein kompaktes Kameliden-Einzel-Domänen-Antikörperfragment (bekannt als VHH), das IL‑6 bindet, und eine lösliche Version des IL‑6-Rezeptors, die als Köder umfunktioniert wurde. Alle werden chemisch mit dem dreifach verzweigten Zucker in abgestuften Mengen versehen. In kultivierten Leberkrebszellen, die den relevanten Zuckerrezeptor natürlich tragen, ziehen die zuckermarkierten Antikörper und VHH IL‑6 oder seinen Rezeptor erfolgreich in die Zellen und leiten sie zu Lysosomen. Je mehr Zuckergruppen angebracht sind (innerhalb gewisser Grenzen), desto effizienter werden die Komplexe hereingezogen, und desto mehr IL‑6 verschwindet innerhalb eines Tages aus dem umgebenden Medium. Bemerkenswert ist, dass der kleine VHH-basierte Degrader, trotz weniger Zuckerbefestigungsstellen, sich als besonders wirksam beim Internalizieren und Entfernen von IL‑6 erweist — vermutlich, weil seine kompakte Form einen günstigeren Komplex für die Aufnahme bildet.
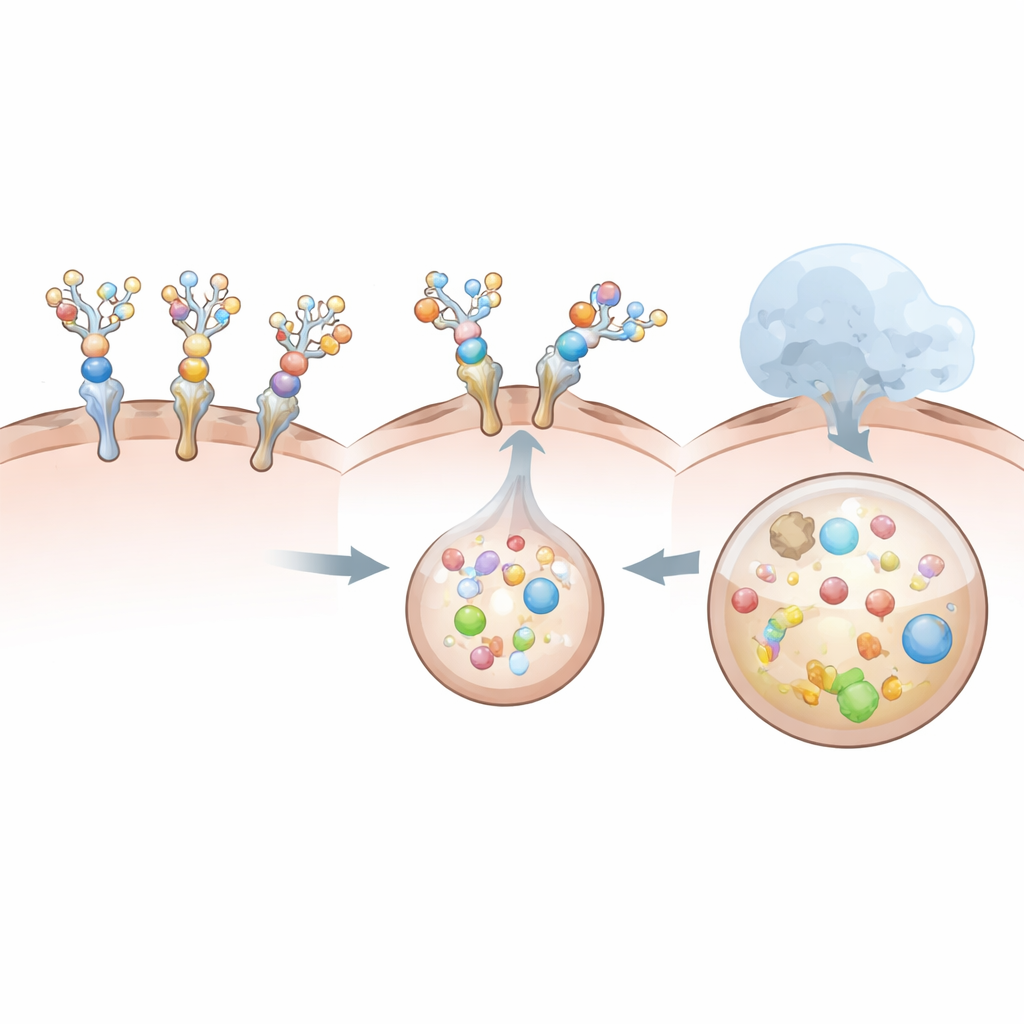
Warum einige Designs besser funktionieren als andere
Nicht alle Degrader sind gleich leistungsfähig. Das auf dem löslichen Rezeptor basierende Design wird zwar bereitwillig von Leberzellen aufgenommen, erweist sich jedoch als schlechter Begleiter für IL‑6 selbst. Seine natürliche Interaktion mit IL‑6 ist vergleichsweise schwach und kurzlebig, und starke Zuckerdekoration destabilisiert diese Bindung noch weiter. Infolgedessen wird der Köder‑Rezeptor allein internalisiert, während der Großteil des IL‑6 außen bleibt und weitgehend unbehelligt ist. Im Gegensatz dazu binden die Antikörper- und VHH-Degrader IL‑6 extrem fest, selbst nach Zuckeranbindung, und interagieren immer noch ausreichend stark mit dem Leberrezeptor, sodass Zytokin und Degrader gemeinsam internalisiert werden. Diese Vergleiche zeigen, dass die bloße Bindung an ein Ziel nicht ausreicht: Gesamtgeometrie, Größe und das Zusammenspiel zwischen Degrader, seinem Ziel und dem Leberrezeptor bestimmen, ob der Komplex effizient verschluckt und zerstört wird.
Ausblick auf klügere Entzündungskontrolle
Für Nicht-Fachleute ist die Kernbotschaft, dass es bald möglich sein könnte, entzündungsfördernde Signale wie IL‑6 nicht nur zu blockieren, sondern sie gezielt aus dem Kreislauf zu „absaugen“, indem man sie zur natürlichen Entsorgungsmaschinerie der Leber umleitet. Diese Studie legt eine praktische Roadmap für das Design solcher glykanbasierter Degrader vor und zeigt, welche molekularen Eigenschaften sie am wirksamsten machen und welche zu kurz greifen. Langfristig könnte die Verfeinerung dieser Designs zu Medikamenten führen, die krankheitsfördernde Zytokine bei Zuständen wie schwerer Arthritis, Zytokinstürmen oder bestimmten Krebsarten umfassender beseitigen, während gesunde Gewebe verschont bleiben, indem die Leber als sicherer, gezielter Aufräumort genutzt wird.
Zitation: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
Schlüsselwörter: zielgerichteter Proteinabbau, Interleukin-6, lysosomaler Transport, extrazelluläre Degrader, Immuntherapie