Clear Sky Science · ar
المحلِّلات الحيوية القائمة على الغليكَّان التي تستهدف محور السيتوكين المناعي
إيقاف الالتهاب الخارج عن السيطرة
العديد من الأمراض الصعبة العلاج، من التهاب المفاصل الروماتويدي إلى بعض أنواع السرطان، تغذيها بروتينات رسولة صغيرة تُسمى السيتوكينات التي تُبقي الجهاز المناعي في حالة تنشيط مستمر. تحاول الأدوية الحالية في الغالب حجب هذه الرسائل، لكن في حالات المرض الشديدة قد يكون هناك ببساطة قدر كبير من الإشارة لا يمكن تحييده. تستكشف هذه الدراسة فكرة مختلفة: بدلاً من كتم الإشارة فحسب، هل يمكننا إزالة هذه الجزيئات المزعجة فعلاً من مجرى الدم عن طريق إرسالها إلى "مراكز إعادة التدوير" الخلوية في الجسم لتدميرها؟
طريقة جديدة لإزالة الجزيئات المسببة للمشكلة
يركز الباحثون على إنترلوكين-6 (IL-6)، وهو سيتوكين ملتهب قوي، ومستقبله المنحل في المحلول، اللذين يدفعان معاً العديد من الاضطرابات المناعية المزمنة والحادة. بدلاً من تصميم مضاد جسم آخر يحجب فقط، يبني الفريق "محلِّلات حيوية" أو BioDegs. هذه أدوات مبنية من بروتينات، مثل الأجسام المضادة أو شظايا صغيرة من الأجسام المضادة، تلتقط أولاً IL-6 أو مستقبلها ثم تستقل وسيلة نقل إلى الكبد. هناك، تستخدم مقبضاً قائماً على السكر للالتصاق بمستقبل طبيعي على خلايا الكبد، مما يسحب السيتوكين داخل نظام التخلص الخلوي لتحلله.
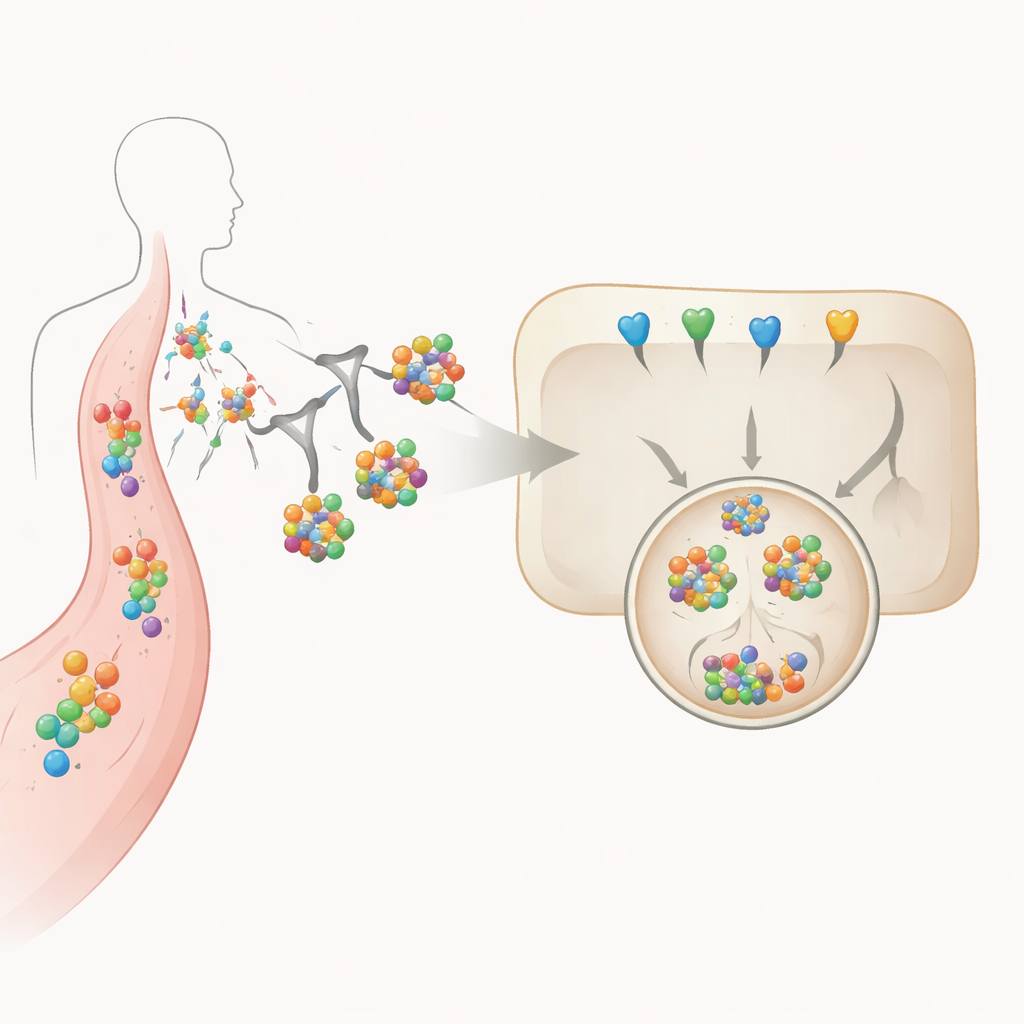
استخدام السكريات كعلامات توصيل دقيقة
في صلب هذا النهج تركيبة سكرية ثلاثية التفرع متصلة ببروتينات المحلل. يتعرف على هذا السكر مستقبل الغليكوبروتينات الخالية من السيجليك (asialoglycoprotein receptor)، وهو جزيء يوجد بشكل رئيسي على خلايا الكبد. عندما يربط المحلل الموسوم بالسكر IL-6 أو مستقبله في مجرى الدم، يُسحَبُ المركب بأكمله إلى سطح خلية الكبد، وتبتلعه الخلية وتُنقَل عبر مقصورات داخلية إلى الجسيم الحالّي، وهو حويصلة حمضية مليئة بإنزيمات هاضمة. يقوم المؤلفون بتغيير عدد مجموعات السكر المرفقة ونوع "السقالة" البروتينية التي تحملها بشكل منهجي، ثم يقيسون كيف تؤثر هذه الخيارات التصميمية على الثبات، وقوة الارتباط، وابتلاع الخلايا، والتدمير الفعلي لـ IL-6 في خلايا شبيهة بالكبد مزروعة في المختبر.
اختبار تصميمات مختلفة للمحلِّلات الحيوية
يقارن الفريق عدة صيغ: أجسام مضادة علاجية كاملة الحجم تستهدف بالفعل IL-6 أو مستقبله، شظية مضادة من نوع اللاما أو الجمل (المعروفة باسم VHH) تربط IL-6، ونسخة منحلّة من مستقبل IL-6 أعيد توظيفها كطُعْم. جميعها مزخرفة كيميائياً بالسكر ثلاثي التفرع بنِسَب متفاوتة. في خلايا سرطان الكبد المزروعة التي تحمل بطبيعتها مستقبل السكر المعني، تنجح الأجسام المضادة وVHH الموسومة بالسكر في سحب IL-6 أو مستقبله إلى داخل الخلايا وتوجيههما إلى الجسيمات الحالّة. كلما زاد عدد مجموعات السكر المرفقة (ضمن حدود)، ازدادت كفاءة سحب المركبات إلى الداخل، وتلاشى المزيد من IL-6 من الوسط المحيط خلال حوالي يوم. ومن اللافت أن المحلل الصغير القائم على VHH، بالرغم من امتلاكه مواقع ارتباط سكرية أقل، يثبت فعالية خاصة في الابتلاع والتصفية، ربما لأن شكله المدمج يُكوّن مركباً أكثر ملاءمة للابتلاع.
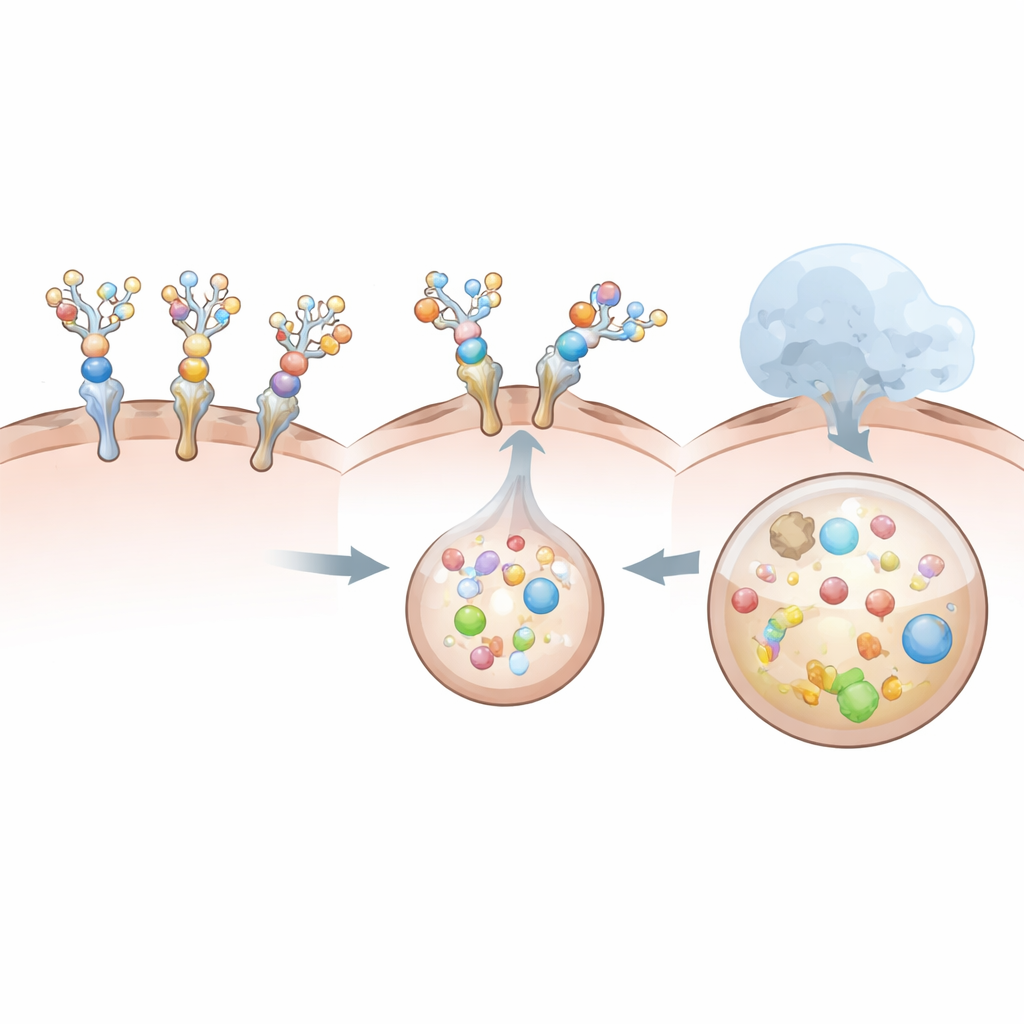
لماذا تعمل بعض التصاميم أفضل من غيرها
ليست كل المحلِّلات متكافئة في الأداء. تصميم المستقبل المنحل، رغم ابتلاعه بسهولة بواسطة خلايا الكبد، يتبيّن أنه مرشد ضعيف لـ IL-6 نفسه. تفاعله الطبيعي مع IL-6 ضعيف نسبياً وقصير الأمد، وزيادة تزيينه بالسكر تُضعف هذا الارتباط أكثر. ونتيجة لذلك، يتم ابتلاع مستقبل الطُعم بمفرده بينما يبقى معظم IL-6 خارج الخلية، إلى حد كبير دون تغيير. على النقيض من ذلك، ترتبط المحلِّلات القائمة على الأجسام المضادة وVHH بـ IL-6 بقوة كبيرة حتى بعد إرفاق السكر، وتظل تتفاعل مع مستقبل الكبد بقوة كافية لضمان ابتلاع السيتوكين والمحلِّل معاً. تكشف هذه المقارنات أن مجرد ارتباط المستهدف ليس كافياً: فالهندسة الإجمالية، والحجم، والتعاون بين المحلل، والمستهدف، ومستقبل الكبد كلها تحدد ما إذا كان المركب سيُبتلع ويُدمَّر بكفاءة.
نظرة إلى المستقبل: تحكم أذكى بالالتهاب
بالنسبة لغير المتخصص، الرسالة الأساسية هي أنه قد يصبح بالإمكان قريباً ليس فقط حجب إشارات الالتهاب مثل IL-6 بل أيضاً "شفطها" من الدورة الدموية بشكل انتقائي عن طريق إعادة توجيهها إلى آليات الإزالة الطبيعية في الكبد. تضع هذه الدراسة خارطة طريق عملية لتصميم مثل هذه المحلِّلات القائمة على الغليكَّان، موضحةً أي السمات الجزيئية تجعلها أكثر فعالية وأيها تقصّر الأداء. على المدى الطويل، قد تؤدي صقل هذه التصميمات إلى أدوية تنظف بشكل أكثر اكتمالاً السيتوكينات المسببة للأمراض في حالات مثل التهاب المفاصل الشديد، أو عواصف السيتوكين، أو بعض السرطانات، مع الحفاظ على أنسجة صحية من خلال استخدام الكبد كمركز تنظيف آمن ومحدد الهدف.
الاستشهاد: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
الكلمات المفتاحية: تحلل البروتين المستهدف, إنترلوكين-6, نقل إلى الجسيمات الحالّة, المحلِّلات الخارجية الخلوية, العلاج المناعي