Clear Sky Science · es
Degradadores biológicos basados en glicanos dirigidos al eje inmunitario de las citocinas
Apagar la inflamación descontrolada
Muchas enfermedades difíciles de tratar, desde la artritis reumatoide hasta ciertos cánceres, están alimentadas por pequeñas proteínas mensajeras llamadas citocinas que mantienen el sistema inmunitario activado. Los fármacos actuales intentan principalmente bloquear estas señales, pero en enfermedades graves puede haber simplemente demasiada señal para neutralizar. Este estudio explora una idea distinta: en lugar de solo amortiguar la señal, ¿podemos eliminar físicamente estas moléculas problemáticas del torrente sanguíneo enviándolas a los “centros de reciclaje” celulares del cuerpo para su destrucción?
Una nueva forma de eliminar moléculas problemáticas
Los investigadores se centran en la interleucina‑6 (IL‑6), una citocina inflamatoria potente, y su receptor soluble, que juntos impulsan muchos trastornos inmunitarios crónicos y agudos. En lugar de diseñar otra anticuerpo bloqueante más, el equipo construye “degradadores biológicos”, o BioDegs. Se trata de herramientas basadas en proteínas, como anticuerpos o pequeños fragmentos de anticuerpo, que primero capturan la IL‑6 o su receptor y luego toman un “paseo” hacia el hígado. Allí usan una etiqueta basada en azúcares para enlazarse a un receptor natural en las células hepáticas, arrastrando la citocina hacia el sistema de eliminación de desechos celular para su degradación.
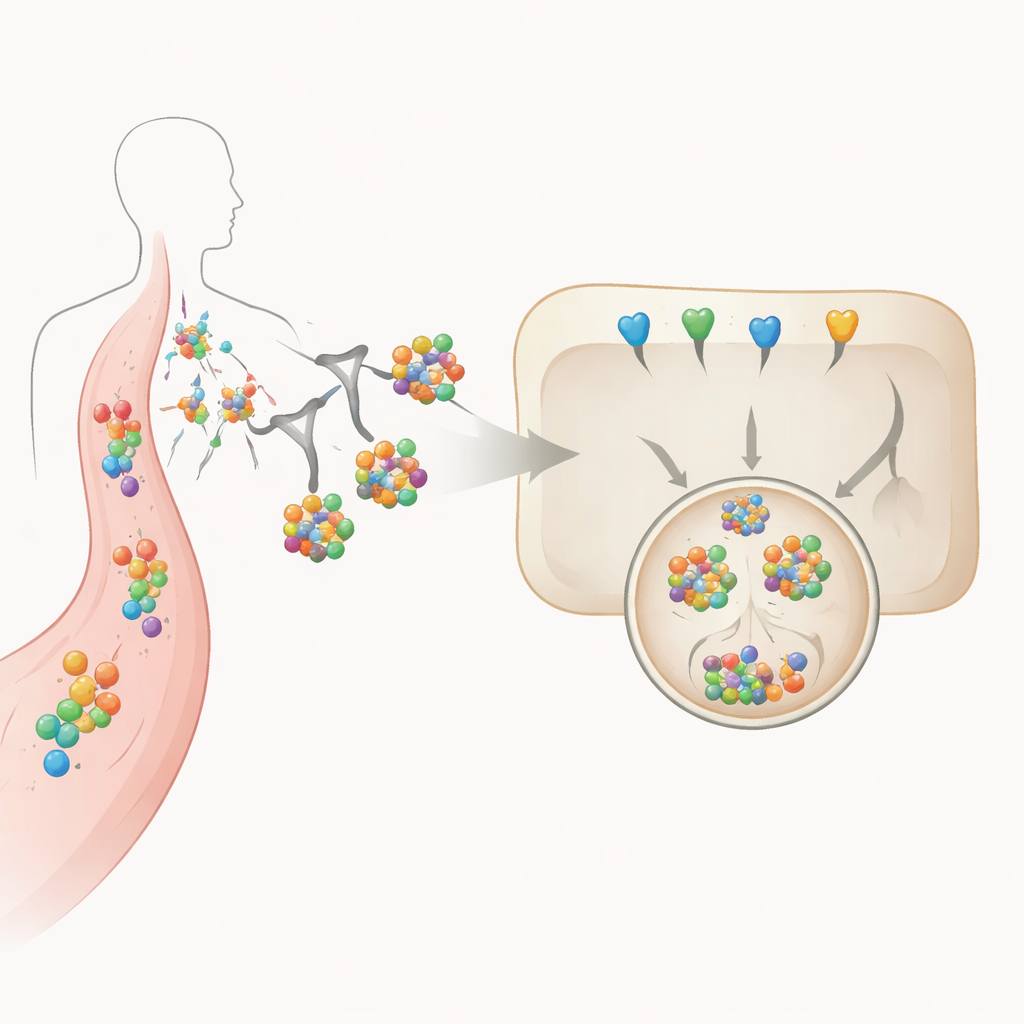
Usar azúcares como etiquetas de entrega de precisión
En el corazón de este enfoque hay una estructura azucarada trifurcada unida a las proteínas degradadoras. Este azúcar es reconocido específicamente por el receptor de asialoglicoproteínas, una molécula presente principalmente en las células del hígado. Cuando el degradador con etiqueta de azúcar se une a la IL‑6 o a su receptor en el torrente sanguíneo, todo el complejo es atraído a la superficie de la célula hepática, engullido y transportado por compartimentos internos hasta el lisosoma, una vesícula ácida repleta de enzimas digestivas. Los autores varían sistemáticamente cuántos grupos de azúcar están unidos y qué “andamiaje” proteico los porta, y luego miden cómo estas decisiones de diseño afectan la estabilidad, la fuerza de unión, la captación celular y la destrucción efectiva de la IL‑6 en células con apariencia hepática cultivadas en el laboratorio.
Probar distintos diseños de degradadores biológicos
El equipo compara varios formatos: anticuerpos terapéuticos de tamaño completo que ya se dirigen a la IL‑6 o a su receptor, un fragmento de anticuerpo monocatenario de camélido compacto (conocido como VHH) que se une a la IL‑6, y una versión soluble del receptor de IL‑6 reutilizada como señuelo. Todos están decorados químicamente con el azúcar trifurcado en cantidades graduadas. En células de cáncer hepático cultivadas que llevan de forma natural el receptor azucarado relevante, los anticuerpos y el VHH etiquetados con azúcar arrastran con éxito la IL‑6 o su receptor hacia el interior celular y los dirigen a los lisosomas. Cuantos más grupos de azúcar se adjuntan (dentro de ciertos límites), con mayor eficacia se internalizan los complejos, y más IL‑6 desaparece del medio circundante en aproximadamente un día. Es notable que el degradador pequeño basado en VHH, a pesar de tener menos sitios de unión para azúcares, resulta especialmente eficaz en internalizar y eliminar la IL‑6, probablemente porque su forma compacta forma un complejo más favorable para la captación.
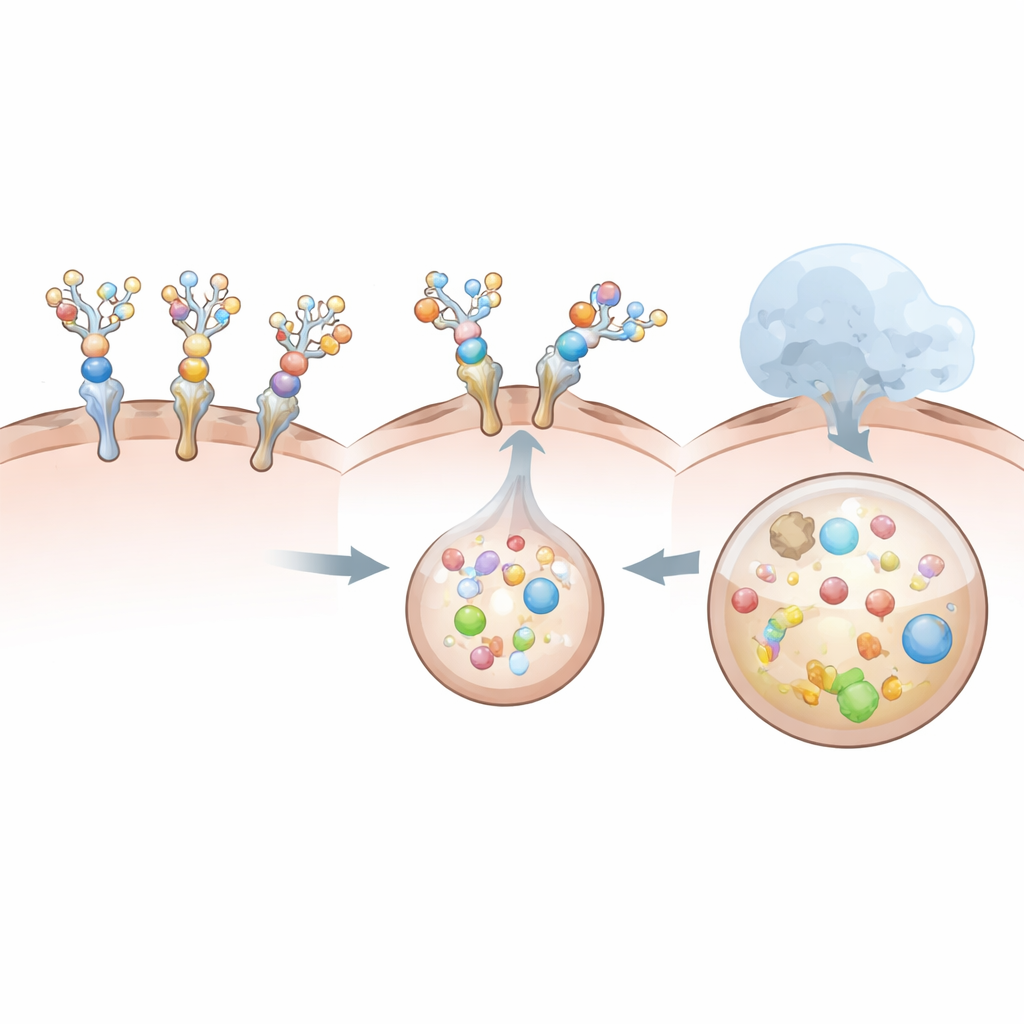
Por qué algunos diseños funcionan mejor que otros
No todos los degradadores rinden igual. El diseño basado en el receptor soluble, aunque es internalizado con facilidad por las células hepáticas, resulta ser un acompañante pobre para la propia IL‑6. Su interacción natural con la IL‑6 es relativamente débil y de corta duración, y una fuerte decoración con azúcares desestabiliza aún más esa unión. Como resultado, el receptor señuelo se internaliza solo mientras que la mayor parte de la IL‑6 permanece afuera, en gran medida intacta. Por el contrario, los degradadores basados en anticuerpos y VHH se unen a la IL‑6 con mucha firmeza incluso después de la adición de azúcares, y siguen interactuando con el receptor hepático con suficiente fuerza como para asegurar que la citocina y el degradador se internalicen juntos. Estas comparaciones muestran que simplemente unirse al objetivo no es suficiente: la geometría global, el tamaño y la cooperación entre el degradador, su objetivo y el receptor hepático determinan si el complejo es eficientemente engullido y destruido.
Mirando hacia un control más inteligente de la inflamación
Para un no especialista, el mensaje clave es que pronto podría ser posible no solo bloquear señales inflamatorias como la IL‑6, sino «aspirarlas» selectivamente de la circulación redirigiéndolas a la maquinaria natural de eliminación del hígado. Este estudio traza una hoja de ruta práctica para diseñar tales degradadores basados en glicanos, mostrando qué características moleculares los hacen más efectivos y cuáles se quedan cortas. A largo plazo, refinar estos diseños podría conducir a medicamentos que eliminen de manera más completa las citocinas que impulsan la enfermedad en condiciones como la artritis severa, tormentas de citocinas o ciertos cánceres, al tiempo que preservan los tejidos sanos aprovechando al hígado como un centro de limpieza seguro y dirigido.
Cita: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
Palabras clave: degradación dirigida de proteínas, interleucina-6, transporte lisosomal, degradadores extracelulares, inmunoterapia