Clear Sky Science · ru
Биологические деградаторы на основе гликанов, нацеленные на цитокиновую иммунную ось
Отключение неконтролируемого воспаления
Многие трудноизлечимые болезни — от ревматоидного артрита до некоторых опухолей — подпитываются малыми сигнальными белками, называемыми цитокинами, которые поддерживают иммунитет в постоянно включённом состоянии. Современные препараты в основном пытаются блокировать эти посредники, но при тяжёлом течении болезни сигнала может быть слишком много, чтобы его нейтрализовать. В этом исследовании рассматривается другой подход: вместо того чтобы просто приглушать сигнал, можно ли физически удалить эти проблемные молекулы из кровотока, направив их в «перерабатывающие центры» клеток для уничтожения?
Новый способ удаления проблемных молекул
Исследователи сосредоточились на интерлейкине‑6 (IL‑6), мощном провоспалительном цитокине, и его растворимом рецепторе, которые вместе стимулируют многие хронические и острые иммунные нарушения. Вместо разработки ещё одного блокирующего антитела команда создала «биологические деградаторы», или BioDeg. Это белковые инструменты — антитела или небольшие фрагменты антител — которые сначала захватывают IL‑6 или его рецептор, а затем направляются в печень. Там они используют основанный на сахарах «хватательный» элемент, чтобы зацепиться за природный рецептор на клетках печени и провести цитокин в систему утилизации клетки для разрушения.
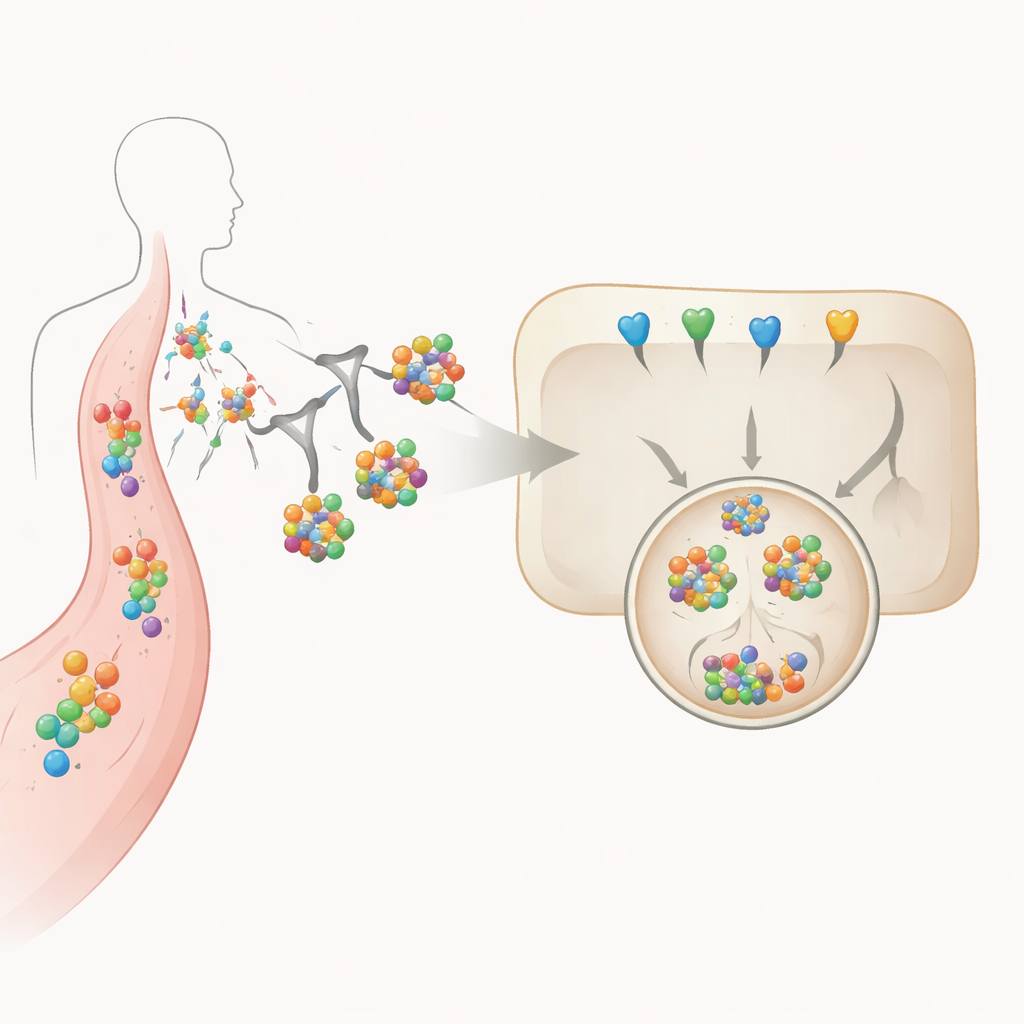
Использование сахаров как меток точной доставки
В основе этого подхода лежит триветвистая сахарная структура, прикреплённая к белкам-деградаторам. Этот сахар распознаётся рецептором аспалогликопротеинов (ASGPR), молекулой, встречающейся преимущественно на клетках печени. Когда сахаромеченый деградатор связывает IL‑6 или его рецептор в кровотоке, весь комплекс притягивается к поверхности печёночной клетки, захватывается и транспортируется через внутриклеточные отсеки в лизосому — кислотный везикул, наполненный ферментами для переваривания. Авторы систематически меняют число присоединённых сахарных групп и белковый «каркас», который их несёт, и измеряют, как эти проектные решения влияют на стабильность, силу связывания, клеточное поглощение и фактическое разрушение IL‑6 в клетках, похожих на печёночные, выращенных в лаборатории.
Тестирование разных конструкций биологических деградаторов
Команда сравнивает несколько форматов: полноразмерные терапевтические антитела, уже нацеленные на IL‑6 или его рецептор, компактный однодоменный фрагмент антитела верблюдового типа (известный как VHH), связывающий IL‑6, и растворимую версию рецептора IL‑6, переосмысленную как «приманка». Все они химически украшены триветвистой сахарной группой в разном объёме. В культивируемых клетках рака печени, которые естественно экспрессируют соответствующий сахарный рецептор, сахаромеченые антитела и VHH успешно втягивают IL‑6 или его рецептор в клетки и направляют их в лизосомы. Чем больше присоединённых сахарных групп (в пределах разумного), тем эффективнее комплексы поглощаются, и тем больше IL‑6 исчезает из окружающей среды примерно за сутки. Примечательно, что небольшой деградатор на основе VHH, несмотря на меньшее число сайтов для присоединения сахаров, оказывается особенно эффективным в интернализации и очистке IL‑6, вероятно, потому, что его компактная форма образует более благоприятный комплекс для захвата клеткой.
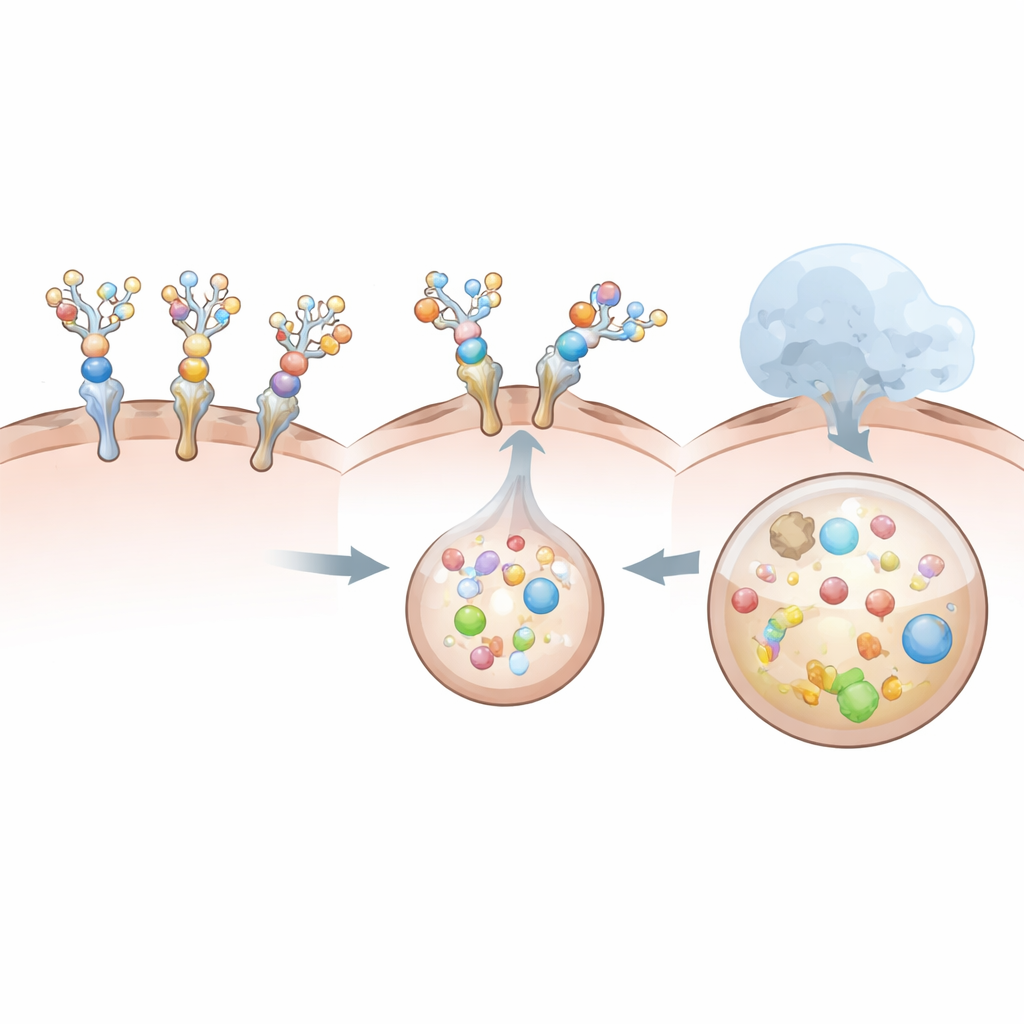
Почему одни конструкции работают лучше других
Не все деградаторы работают одинаково эффективно. Конструкция на основе растворимого рецептора, хотя и быстро поглощается клетками печени, оказывается плохим «сопровождающим» для самого IL‑6. Её естественное взаимодействие с IL‑6 относительно слабое и короткоживущее, а массивное сахарное украшение дополнительно дестабилизирует это связывание. В результате «приманка» поступает в клетку в одиночку, в то время как большая часть IL‑6 остаётся снаружи и практически не тронута. Напротив, антительные и VHH-деградаторы связывают IL‑6 крайне прочно даже после присоединения сахаров и при этом достаточно хорошо взаимодействуют с печёночным рецептором, чтобы гарантировать совместную интернализацию цитокина и деградатора. Эти сравнения показывают, что простого связывания цели недостаточно: итоговая геометрия, размер и кооперация между деградатором, его целью и печёночным рецептором определяют, будет ли комплекс эффективно захвачен и разрушен.
Взгляд в будущее: умное управление воспалением
Для неспециалиста ключевая мысль в том, что вскоре может стать возможным не просто блокировать провоспалительные сигналы, такие как IL‑6, а выборочно «высасывать» их из кровообращения, перенаправляя в природную утилизационную систему печени. Это исследование предлагает практическую дорожную карту для проектирования таких гликан-ориентированных деградаторов, показывая, какие молекулярные характеристики делают их наиболее эффективными, а какие — неудачными. В долгосрочной перспективе совершенствование этих конструкций может привести к лекарствам, которые более полно очищают цитокины, поддерживающие болезнь, при состояниях вроде тяжёлого артрита, цитокинового шторма или некоторых видов рака, при этом щадя здоровые ткани за счёт использования печени в качестве безопасного целевого центра очистки.
Цитирование: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
Ключевые слова: таргетное разрушение белков, интерлейкин-6, лизосомная транспортировка, внеклеточные деградаторы, иммунотерапия