Clear Sky Science · it
Degradatori biologici a base di glicani mirati all'asse immunitario delle citochine
Spegnere l'infiammazione fuori controllo
Molte malattie difficili da trattare, dall'artrite reumatoide ad alcuni tumori, sono alimentate da piccole proteine messaggere chiamate citochine che mantengono il sistema immunitario costantemente attivato. I farmaci attuali cercano per lo più di bloccare questi messaggeri, ma nelle forme gravi la quantità di segnale può essere semplicemente troppo elevata per essere neutralizzata. Questo studio esplora un'idea diversa: invece di limitarsi ad attenuare il segnale, è possibile rimuovere fisicamente queste molecole problematiche dal flusso sanguigno inviandole ai “centri di riciclo” cellulari del corpo per la loro distruzione?
Un nuovo modo per eliminare molecole problematiche
I ricercatori si concentrano sull'interleuchina‑6 (IL‑6), una potente citochina infiammatoria, e sul suo recettore solubile, che insieme guidano molti disturbi immunitari cronici e acuti. Anziché progettare un'altra anticorpo bloccante, il team costruisce “degradatori biologici”, o BioDeg. Si tratta di strumenti a base proteica, come anticorpi o piccoli frammenti di anticorpi, che prima afferrano l'IL‑6 o il suo recettore e poi prendono a prestito una scorciatoia verso il fegato. Lì utilizzano una maniglia a base di zucchero per agganciarsi a un recettore naturale sulle cellule epatiche, trascinando la citochina nel sistema di smaltimento cellulare per la sua degradazione.
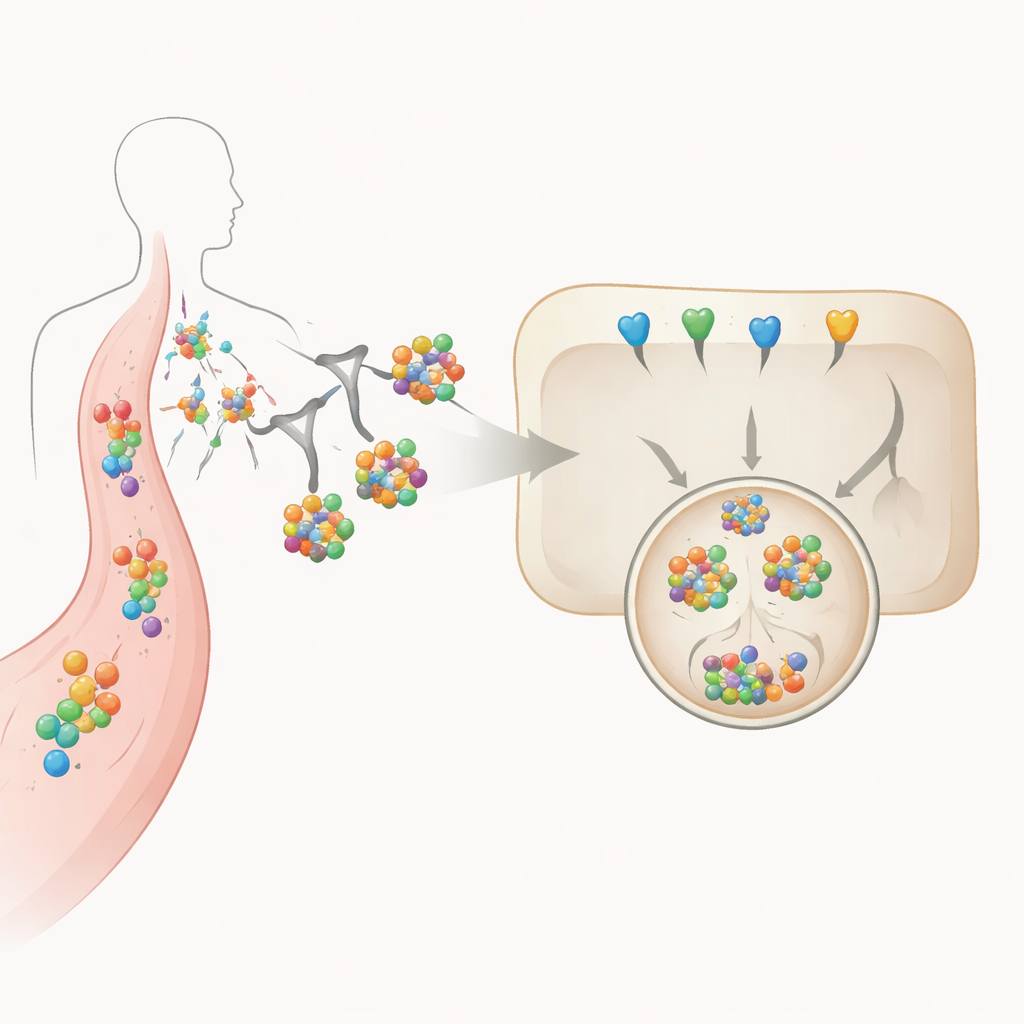
Usare gli zuccheri come etichette di consegna di precisione
Al centro di questo approccio c'è una struttura zuccherina a tre rami attaccata alle proteine degradatrici. Questo zucchero è riconosciuto specificamente dal recettore delle asialoglicoproteine, una molecola presente principalmente sulle cellule del fegato. Quando il degradatore marcato con lo zucchero lega l'IL‑6 o il suo recettore nel flusso sanguigno, l'intero complesso viene attratto alla superficie della cellula epatica, inglobato e trasportato attraverso compartimenti interni fino al lisosoma, una vescicola acida carica di enzimi digestivi. Gli autori variano sistematicamente il numero di gruppi zuccherini attaccati e quale “impalcatura” proteica li porta, quindi misurano come queste scelte progettuali influenzano stabilità, forza di legame, captazione cellulare e reale degradazione dell'IL‑6 in cellule di tipo epatico coltivate in laboratorio.
Testare diversi design di degradatori biologici
Il team confronta vari formati: anticorpi terapeutici di dimensione completa che già prendono di mira l'IL‑6 o il suo recettore, un compatto frammento di anticorpo a dominio singolo di camelidi (conosciuto come VHH) che lega l'IL‑6, e una versione solubile del recettore dell'IL‑6 riutilizzata come esca. Tutti sono chimicamente decorati con lo zucchero a tre rami in quantità graduali. In cellule di carcinoma epatico coltivate che esprimono naturalmente il recettore zuccherino rilevante, gli anticorpi e i VHH marcati con lo zucchero trascinano con successo l'IL‑6 o il suo recettore all'interno delle cellule e li indirizzano ai lisosomi. Più gruppi zuccherini sono attaccati (entro certi limiti), più efficacemente i complessi vengono internalizzati e più l'IL‑6 scompare dal mezzo circostante nell'arco di circa un giorno. Degno di nota, il piccolo degradatore a base di VHH, nonostante abbia meno siti di attacco per gli zuccheri, risulta particolarmente efficace nell'internalizzare e rimuovere l'IL‑6, probabilmente perché la sua forma compatta genera un complesso più favorevole per l'assorbimento.
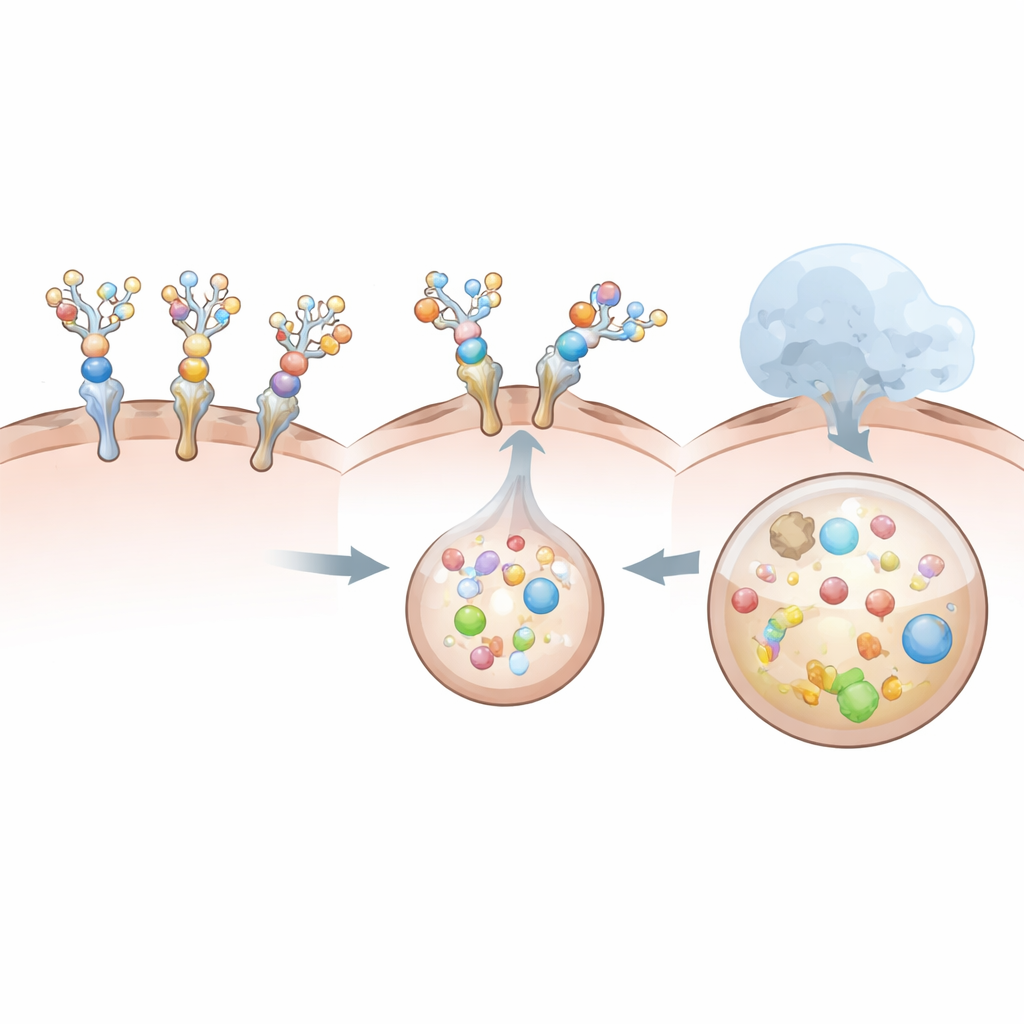
Perché alcuni design funzionano meglio di altri
Non tutti i degradatori performano allo stesso modo. Il design basato sul recettore solubile, sebbene venga facilmente assorbito dalle cellule epatiche, si rivela un cattivo scorta per l'IL‑6 stesso. La sua interazione naturale con l'IL‑6 è relativamente debole e di breve durata, e una pesante decorazione con zuccheri destabilizza ulteriormente questo legame. Di conseguenza, il recettore esca viene internalizzato da solo mentre la maggior parte dell'IL‑6 resta all'esterno, in gran parte intatta. Al contrario, gli anticorpi e i degradatori a base di VHH legano l'IL‑6 in modo estremamente forte anche dopo l'aggiunta degli zuccheri, e allo stesso tempo ingaggiano il recettore epatico con sufficiente forza da garantire che citochina e degradatore vengano internalizzati insieme. Questi confronti rivelano che legare semplicemente un bersaglio non è sufficiente: la geometria complessiva, le dimensioni e la cooperazione tra degradatore, suo bersaglio e recettore epatico determinano se il complesso viene efficacemente inglobato e distrutto.
Sguardo futuro verso un controllo più intelligente dell'infiammazione
Per un non specialista, il messaggio chiave è che potrebbe presto essere possibile non solo bloccare segnali infiammatori come l'IL‑6, ma “aspirarli” selettivamente dalla circolazione reindirizzandoli al naturale meccanismo di smaltimento del fegato. Questo studio traccia una roadmap pratica per progettare tali degradatori a base di glicani, mostrando quali caratteristiche molecolari li rendono più efficaci e quali risultano insufficienti. A lungo termine, l'affinamento di questi design potrebbe portare a farmaci che eliminano in modo più completo le citochine che guidano la malattia in condizioni come l'artrite severa, le tempeste di citochine o alcuni tumori, risparmiando i tessuti sani grazie all'uso del fegato come centro di pulizia mirato e sicuro.
Citazione: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
Parole chiave: degradazione proteica mirata, interleuchina-6, traffico lisosomiale, degradatori extracellulari, immunoterapia