Clear Sky Science · he
מד-מולקולרי מבוסס גליקן שמופנה לציר החיסוני של הציטוקינים
כיבוי דלקת יוצאת־ממיטה
מחלות קשות לטיפול רבות, מריאומטואיד ארטריטיס ועד סוגים מסוימים של סרטן, מונעות על ידי חלבוני שליח קטנים הנקראים ציטוקינים שממשיכים להפעיל את המערכת החיסונית. התרופות הקיימות נוטות בעיקר לנטרל את השליחים האלה, אך במחלה קשה האותות עלולים להיות חסרי־מניעה ולא ניתן לנטרלם מספיק. המחקר הזה בוחן רעיון אחר: במקום רק להשתיק את האות, האם אפשר להסיר פיזית את המולקולות הבעייתיות מהדם על‑ידי שליחתם ל"מרכזי המיחזור" התאית של הגוף להרס?
דרך חדשה להסרת מולקולות בעייתיות
החוקרים מתמקדים באינטרלוקין‑6 (IL‑6), ציטוקין דלקתי חזק, ובקולטן המסיס שלו, שמניעים יחדיו הפרעות חיסוניות כרוניות ואקוטיות רבות. במקום לעצב עוד נוגדן חוסם, הקבוצה בונה "מדכאים ביולוגיים" (BioDegs). אלה כלים מבוססי חלבון, כגון נוגדנים או קטעי נוגדן זעירים, שמתחילים בתפיסת IL‑6 או הקולטן שלו ואז מתניידים אל הכבד. שם הם משתמשים ב"ידית" מבוססת סוכר כדי להתחבר לקולטן טבעי על תאי הכבד, תוך משיכת הציטוקין לתוך מערכת ההריסה התאית לצמצום ולשבירה.
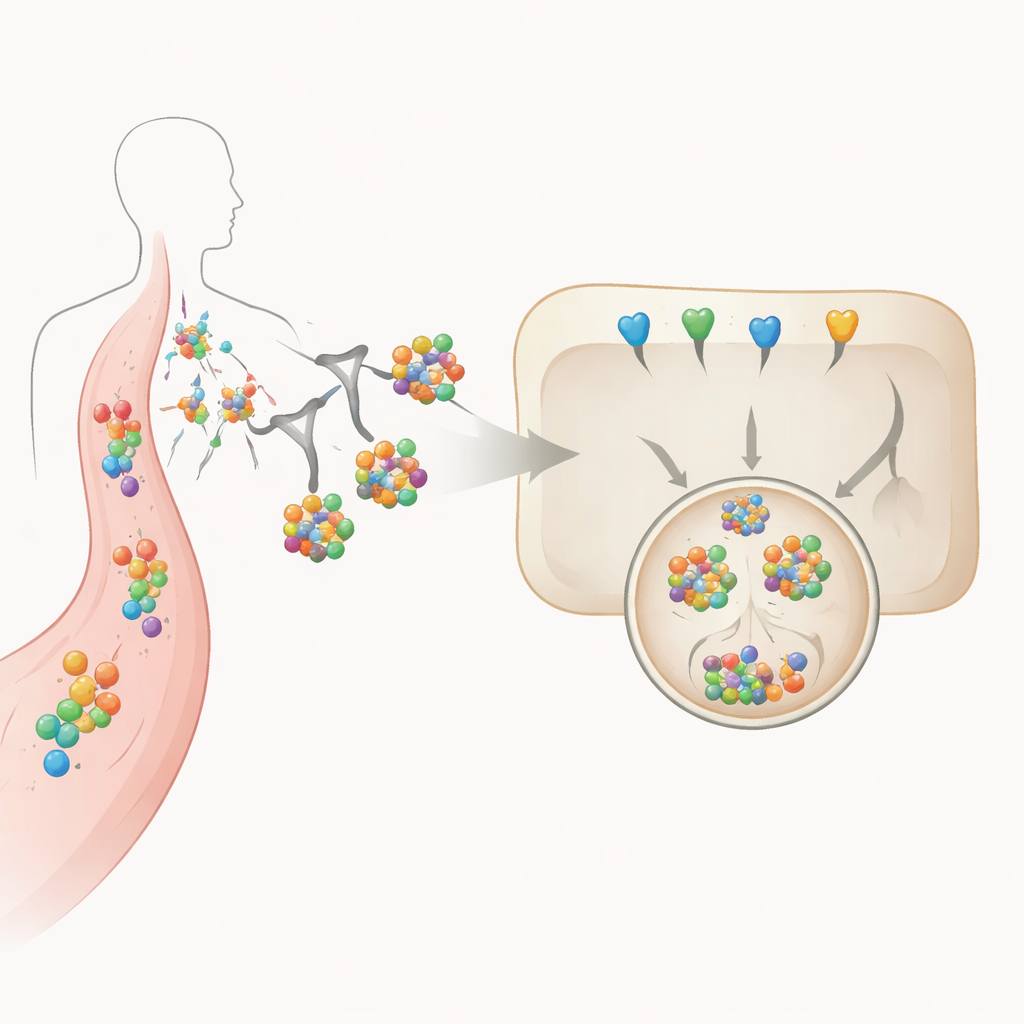
שימוש בסוכרים כתגי הובלה מדויקים
בלב הגישה הזו עומדת מבנה סוכר תלת‑ענפי שמחובר לחלבוני המדכא. סוכר זה מזוהה במיוחד על ידי קולטן האזיאוגליקופרוטאין (ASGPR), מולקולה הנמצאת בעיקר על תאי כבד. כאשר המדכא המסומן בסוכר נקשר ל‑IL‑6 או לקולטן שלו בזרם הדם, כל המורכב מצטבר על פני תא הכבד, נבלע ומועבר דרך מחלקות פנימיות אל הליזוזום — וזיקולה חומצית מלאת אנזימי עיכול. המחברים שינו באופן שיטתני את מספר קבוצות הסוכר המחוברות ואת "השלד" החלבוני הנושא אותן, ואז מדדו כיצד בחירות עיצוב אלה משפיעות על יציבות, חוזק קשירה, ייבוא תאי וערעור ממשי של IL‑6 בתאי כבד דמוים‑מעבדה.
בחינת עיצובים שונים של מדכאים ביולוגיים
הקבוצה משווה כמה פורמטים: נוגדנים טיפוליים בגודל מלא שכבר מכוונים ל‑IL‑6 או לקולטן שלו, מקטע נוגדן חד‑תחומי קמלאידי קומפקטי (מוכר כ‑VHH) שנקשר ל‑IL‑6, וגרסה מסיסה של קולטן IL‑6 הממוחזרת לשמש כפתיון. כולם מקושטים כימית בסוכר התלת‑ענפי בכמויות מדורגות. בתאי סרטן כבד תרביתיים שנושאים באופן טבעי את הקולטן המתאים, הנוגדנים וה‑VHH המסומנים בסוכר מושכים בהצלחה את IL‑6 או את קולטן שלו אל תוך התאים ומעבירים אותם לליזוזומים. ככל שמחוברות יותר קבוצות סוכר (בתוך גבולות), כך המורכבים נמשכים פנימה ביעילות גדולה יותר, וכך יותר IL‑6 נעלם מהנוזל הסביבתי בתוך כשבוע יום. ראוי לציון כי המדכא המבוסס VHH הקטן, אף שהיה עם פחות אתרי חיבור לסוכר, הוכיח יעילות מיוחדת ביעול התהליך והסרת IL‑6, ככל הנראה מפני שתצורתו הקומפקטית יוצרת מורכב תלת‑ממדי נוח יותר לייבוא.
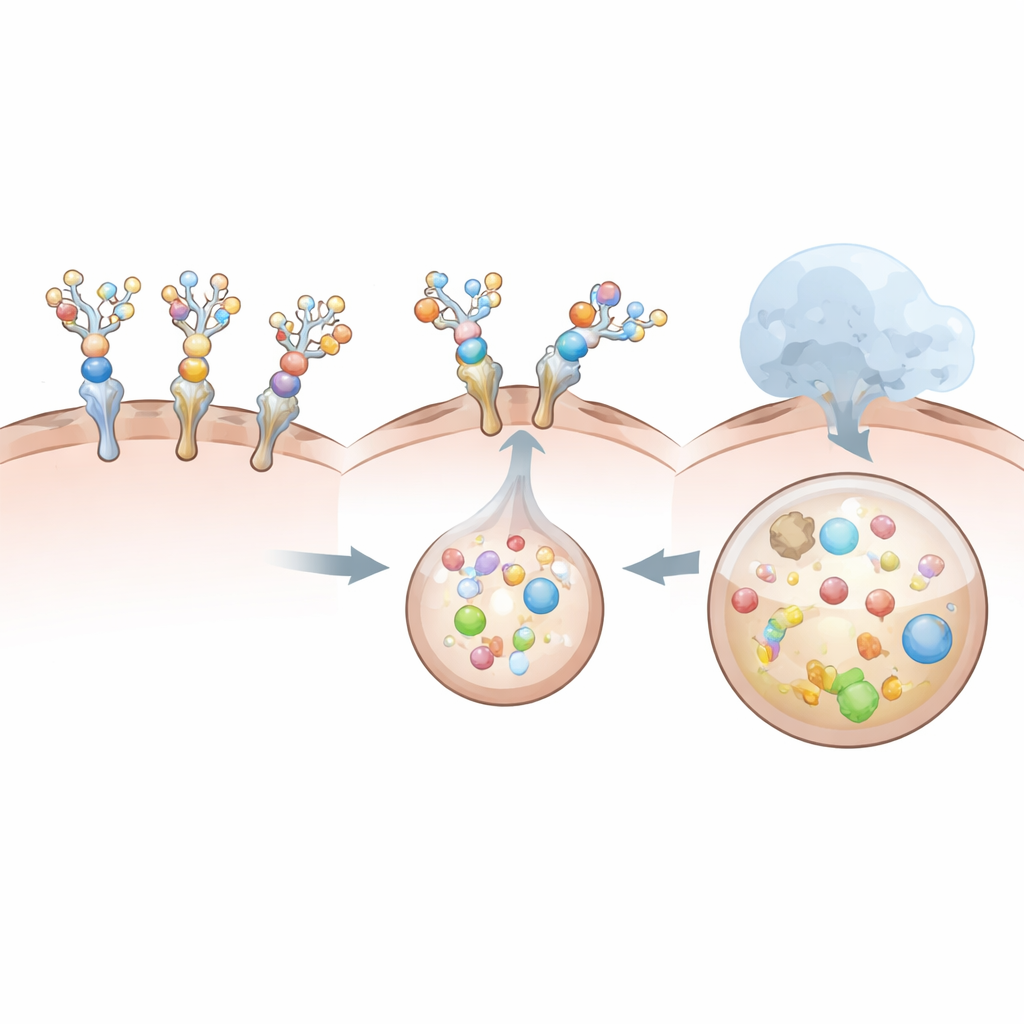
מדוע חלק מהעיצובים עובדים טוב יותר מאחרים
לא כל המדכאים מפיקים את אותן תוצאות. עיצוב מבוסס‑קולטן מסיס, אף שהוא נלקח פנימה בקלות על‑ידי תאי כבד, מתברר כמלווה גרוע ל‑IL‑6 עצמו. האינטראקציה הטבעית שלו עם IL‑6 יחסית חלשה וקצרת‑טווח, וקישוט סוכרי כבד מחליש עוד יותר את הקשירה הזו. כתוצאה מכך, קולטן הפתיון מובל פנימה לבדו בעוד שרוב IL‑6 נשאר מחוץ, כמעט בלתי מושפע. לעומת זאת, המדכאים מבוססי נוגדן ו‑VHH נקשרים ל‑IL‑6 בחוזקה רבה גם לאחר חיבור הסוכר, ועדיין מתקשרים עם קולטן הכבד בעוצמה מספקת כדי להבטיח שהציטוקין והמדכא יובילו פנימה יחד. השוואות אלה מראות כי קשירה של מטרה לבדה אינה מספיקה: הגיאומטריה הכוללת, הגודל ושיתוף הפעולה בין המדכא, המטרה וקולטן הכבד קובעים האם המורכב נבלע ונהרס ביעילות.
מבט לעתיד של שליטה חכמה בדלקת
ללא מומחיות מיוחדת, המסר המרכזי הוא כי יתכן שבקרוב תהיה אפשרות לא רק לחסום אותות דלקתיים כמו IL‑6 אלא גם "לשאוב" אותם באופן סלקטיבי מהמחזור על‑ידי הפנייתם למכונת ההרס הטבעית של הכבד. המחקר ממפה דרך מעשית לעיצוב מדכאים מבוססי גליקן כאלה, ומראה איזה מאפיינים מולקולריים הופכים אותם ליעילים ביותר ואילו נכשלים. בטווח הארוך, עידון העיצובים האלה עלול להוליד תרופות המניקות בצורה מלאה יותר ציטוקינים שמניעים מחלות במצבים כגון דלקת מפרקים קשה, סערות ציטוקיניות או סוגים מסוימים של סרטן, תוך שמירה על רקמות בריאות על‑ידי ניצול הכבד כמרכז ניקוי בטוח וממוקד.
ציטוט: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
מילות מפתח: דגרדציה ממוקדת של חלבונים, אינטרלוקין-6, מסלול תנועה לליזוזום, מדכאים חוץ‑תאיים, אימונותרפיה