Clear Sky Science · pl
Biologiczne degradery oparte na glikanach celujące w oś immunologiczną cytokin
Wyłączanie wymykającego się spod kontroli zapalenia
Wiele chorób trudnych do leczenia — od reumatoidalnego zapalenia stawów po niektóre nowotwory — napędzanych jest przez małe białka sygnałowe zwane cytokinami, które utrzymują układ odpornościowy w stanie ciągłej aktywacji. Obecne leki przede wszystkim próbują te sygnały zablokować, ale w ciężkich chorobach sygnału może być po prostu zbyt dużo, by go neutralizować. W tym badaniu autorzy rozważają inną koncepcję: zamiast jedynie tłumić sygnał, czy można fizycznie usunąć te kłopotliwe cząsteczki z krwiobiegu, kierując je do komórkowych „punktów recyklingu” organizmu w celu zniszczenia?
Nowy sposób usuwania problematycznych cząsteczek
Naukowcy koncentrują się na interleukinie‑6 (IL‑6), silnej cytokinie prozapalnej, oraz jej rozpuszczalnym receptorze, które razem napędzają wiele przewlekłych i ostrych zaburzeń odpornościowych. Zamiast projektować kolejne przeciwciało blokujące, zespół tworzy „biologiczne degradery”, czyli BioDegi. Są to narzędzia oparte na białkach, takie jak przeciwciała lub malutkie fragmenty przeciwciał, które najpierw chwytają IL‑6 lub jego receptor, a następnie „podróżują” z nimi do wątroby. Tam wykorzystują cukrowy uchwyt, by przyczepić się do naturalnego receptora na komórkach wątroby, wciągając cytokinę do systemu usuwania odpadów komórkowych w celu rozkładu.
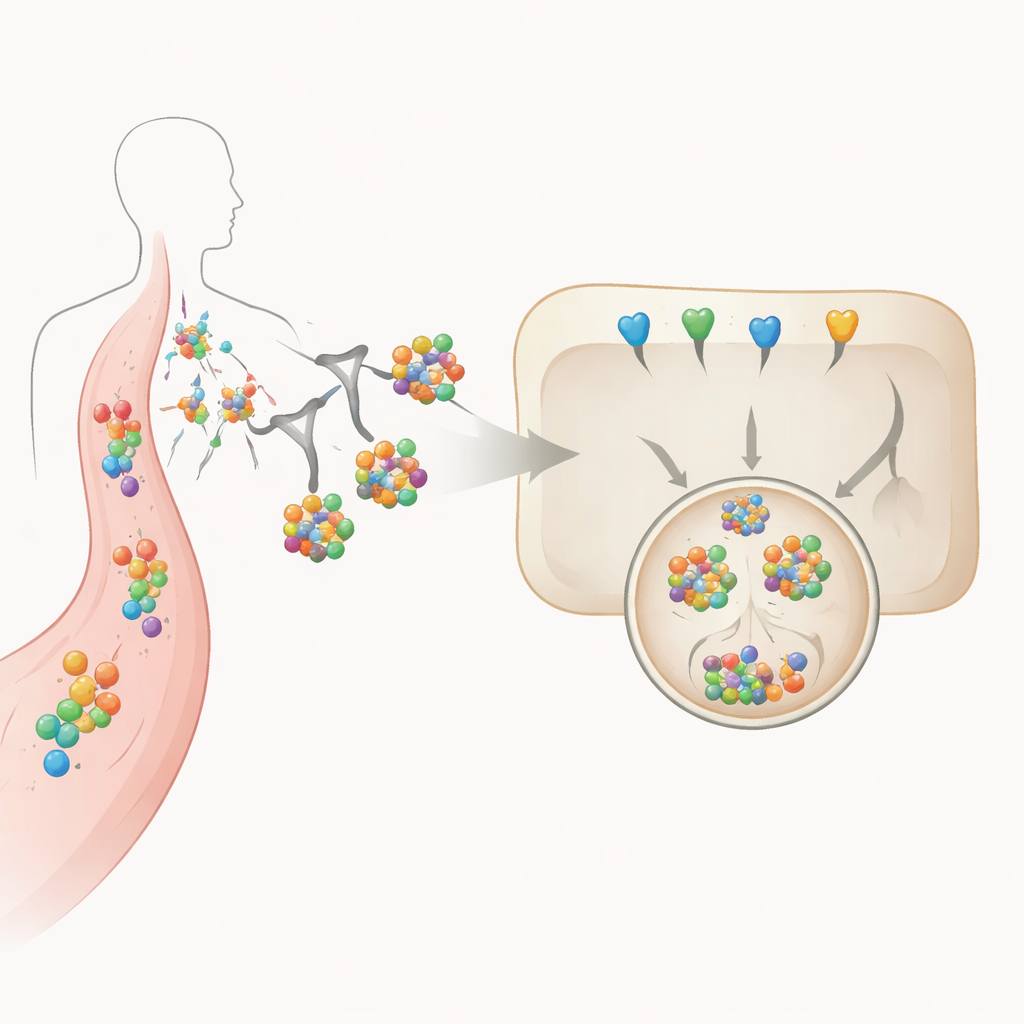
Wykorzystanie cukrów jako precyzyjnych tagów dostarczenia
W centrum tego podejścia znajduje się trójodgałęziona struktura cukrowa przymocowana do białkowych degraderów. Ten glikan jest specyficznie rozpoznawany przez receptor asialoglikoproteinowy, cząsteczkę występującą głównie na komórkach wątroby. Gdy degrader z oznaczeniem cukrowym wiąże IL‑6 lub jego receptor we krwi, cały kompleks zostaje przyciągnięty do powierzchni komórki wątroby, pochłonięty i przetransportowany przez wewnętrzne przedziały do lizosomu — kwaśnego pęcherzyka bogatego w enzymy trawiące. Autorzy systematycznie zmieniają liczbę przyłączonych grup cukrowych i które białkowe „rusztowanie” je niesie, a następnie mierzą, jak te wybory projektowe wpływają na stabilność, siłę wiązania, wychwyt komórkowy oraz rzeczywiste niszczenie IL‑6 w komórkach przypominających wątrobę hodowanych w laboratorium.
Testowanie różnych projektów biologicznych degraderów
Zespół porównuje kilka formatów: pełnowymiarowe przeciwciała terapeutyczne, które już celują w IL‑6 lub jego receptor, kompaktowy jednowartościowy fragment przeciwciała wielbłądowatego (znany jako VHH) wiążący IL‑6 oraz rozpuszczalną wersję receptora IL‑6 przekształconą w przynętę. Wszystkie są chemicznie „ozdobione” trójodgałęzionym cukrem w stopniowanych ilościach. W hodowlach komórek raka wątroby, które naturalnie noszą wspomniany receptor cukrowy, oznakowane cukrem przeciwciała i VHH skutecznie wciągają IL‑6 lub jego receptor do wnętrza komórek i kierują je do lizosomów. Im więcej przyłączonych grup cukrowych (w granicach rozsądku), tym wydajniej kompleksy są transportowane do wnętrza i tym więcej IL‑6 znika z otaczającego medium w ciągu około doby. Co istotne, mały degrader oparty na VHH, mimo że ma mniej miejsc przyłączenia cukrów, okazuje się szczególnie efektywny w internalizacji i usuwaniu IL‑6, prawdopodobnie dlatego, że jego kompaktowy kształt tworzy korzystniejszy kompleks do wychwytu.
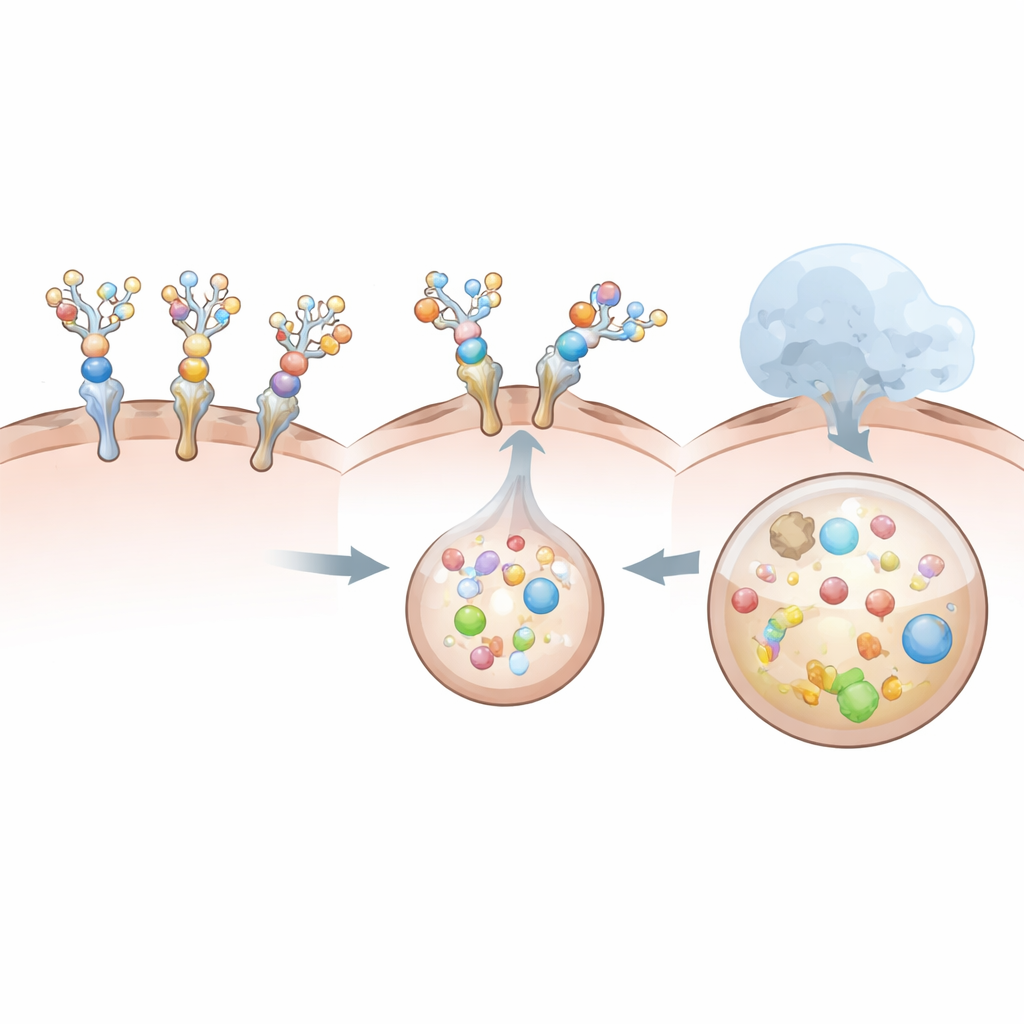
Dlaczego niektóre projekty działają lepiej niż inne
Nie wszystkie degradery działają równie dobrze. Projekt oparty na rozpuszczalnym receptorze, choć łatwo internalizowany przez komórki wątroby, okazuje się słabym eskortem dla samego IL‑6. Jego naturalna interakcja z IL‑6 jest stosunkowo słaba i krótkotrwała, a silne „ubrązowienie” cukrowe dodatkowo destabilizuje to wiązanie. W rezultacie przynęta receptorowa jest internalizowana sama, podczas gdy większość IL‑6 pozostaje na zewnątrz, w dużej mierze nietknięta. Dla kontrastu, przeciwciała i degradery oparte na VHH wiążą IL‑6 bardzo mocno nawet po przyłączeniu cukrów i wciąż angażują receptor wątroby na tyle silnie, by zapewnić wspólną internalizację cytokiny i degradatora. Te porównania pokazują, że samo wiązanie celu nie wystarcza: ogólna geometria, rozmiar i współpraca między degraderem, jego celem i receptorem wątroby decydują o tym, czy kompleks zostanie sprawnie pochłonięty i zniszczony.
Perspektywy na inteligentniejszą kontrolę zapalenia
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że wkrótce może być możliwe nie tylko blokowanie sygnałów zapalnych, takich jak IL‑6, ale selektywne „odkurzanie” ich z krążenia przez przekierowanie do naturalnej maszyny utylizacyjnej wątroby. Badanie przedstawia praktyczną mapę drogową projektowania takich degraderów opartych na glikanach, pokazując, które cechy molekularne czynią je najbardziej skutecznymi, a które zawiodą. W dłuższej perspektywie dopracowanie tych rozwiązań może doprowadzić do leków, które skuteczniej usuwają cytokiny napędzające choroby w stanach takich jak ciężkie zapalenie stawów, burze cytokinowe czy niektóre nowotwory, jednocześnie oszczędzając zdrowe tkanki dzięki wykorzystaniu wątroby jako bezpiecznego, ukierunkowanego centrum oczyszczania.
Cytowanie: Seifert, M., Kollenkirchen, T., Ernst, A. et al. Glycan-based biological degraders targeting the cytokine immune axis. Commun Biol 9, 530 (2026). https://doi.org/10.1038/s42003-026-10001-9
Słowa kluczowe: ukierunkowane niszczenie białek, interleukina-6, transport do lizosomów, zewnątrzkomórkowe degradery, immunoterapia