Clear Sky Science · zh
一个发生学-细胞因子代码决定巨噬细胞反应极性和肿瘤结局
为何机体的“吞噬大将”细胞在癌症中至关重要
被称为巨噬细胞的免疫细胞是实体肿瘤中最丰富的细胞类型之一。这些细胞“大吃者”既可以攻击癌细胞,也可以帮助癌症扩散,因此许多新疗法旨在将它们推向抗癌一侧。然而,患者中的疗效令人失望,部分原因在于我们仍缺乏清晰的图谱来说明什么使巨噬细胞有益或有害。本研究揭示了一个隐匿的“代码”,将巨噬细胞的发源地、所接收的信号以及其最终如何影响肿瘤生长和转移联系了起来。
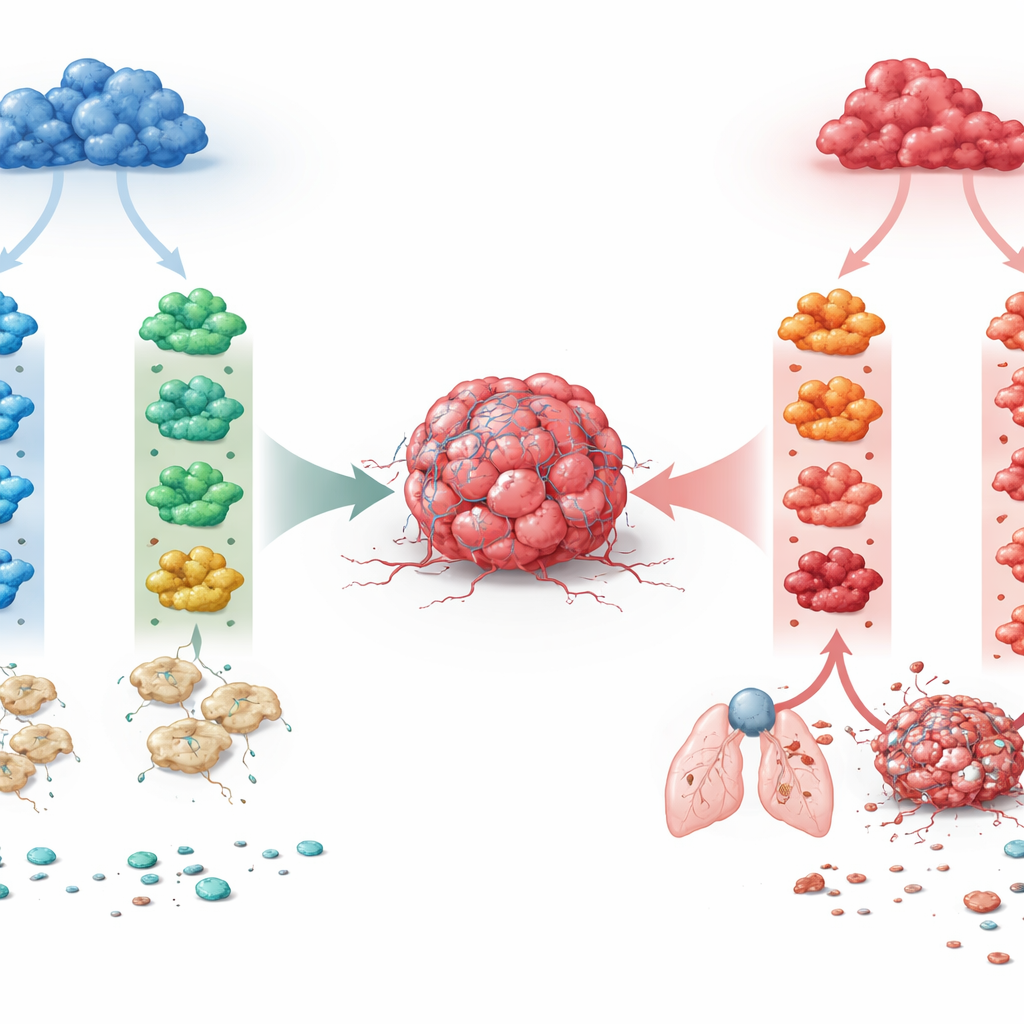
两大家族的巨噬细胞,多种可能命运
研究者将注意力集中在存在于多种组织中的两条主要巨噬细胞谱系。一条谱系依赖于名为M-CSF的生长因子,倾向于维持日常组织稳态;另一条在促炎生长因子GM-CSF作用下产生,本质上更具反应性。研究团队从小鼠骨髓中沿任一谱系培养巨噬细胞,然后将它们暴露于肿瘤中常见的四种免疫信号:IFN-γ、IL-4、IL-10和TGF-β。由此形成了八种定义明确的巨噬细胞状态。通过对整体和单细胞RNA测序读取全局基因活动,他们发现发育起源是主导因素:它比任何单一细胞因子更能区分这两条谱系。因此,相同的信号可以将两大家族推向截然不同的基因与功能程序。
相同信号如何从朋友变成敌人
一个关键发现是,长期与伤口修复和“替代”激活相关的细胞因子IL-4,其效应取决于巨噬细胞的起源。当IL-4作用于M-CSF来源的巨噬细胞时,它触发了与组织重塑相关的基因程序,诱导酶ARG1的表达,使细胞呈现拉长形态,并降低了它们向T细胞呈递抗原的能力。在功能上,这些巨噬细胞支持肿瘤生长、侵入周围基质并播种肺转移。相反,IL-4作用于GM-CSF来源的巨噬细胞时,驱动其进入更具炎症性的、类似树突状细胞的状态,表现出强烈的抗原呈递能力和抑瘤行为。因此,相同的细胞因子可根据巨噬细胞的发育背景要么助长癌症,要么帮助抑制它。对IL-10也观察到类似但不那么戏剧性的谱系依赖性分叉,而IFN-γ在两条谱系中始终具有抗肿瘤作用,TGF-β则在两者中始终促进肿瘤。
观察肿瘤与巨噬细胞如何相互塑造
为了观察这些被程式化的巨噬细胞随时间如何影响肿瘤细胞,研究团队构建了三维球体,将带荧光标记的癌细胞与不同极化的巨噬细胞混合。几天内的单细胞分析揭示了一个有趣的模式。巨噬细胞无论起始状态如何,都会逐渐收敛到以氧化应激反应为主的共同“肿瘤教育”谱;相比之下,肿瘤细胞则表现出多样化。在对照或IFN-γ极化的巨噬细胞存在下,癌细胞继续分裂但侵袭性有限。当与IL-4或TGF-β处理的M-CSF巨噬细胞,或与IL-10/TGF-β处理的GM-CSF巨噬细胞共同培养时,肿瘤细胞转向上皮-间质转化的、具侵袭准备的身份。尽管肿瘤随后重塑了巨噬细胞的基因特征,它们的初始程式化已经将癌细胞引导到截然不同的轨迹上。
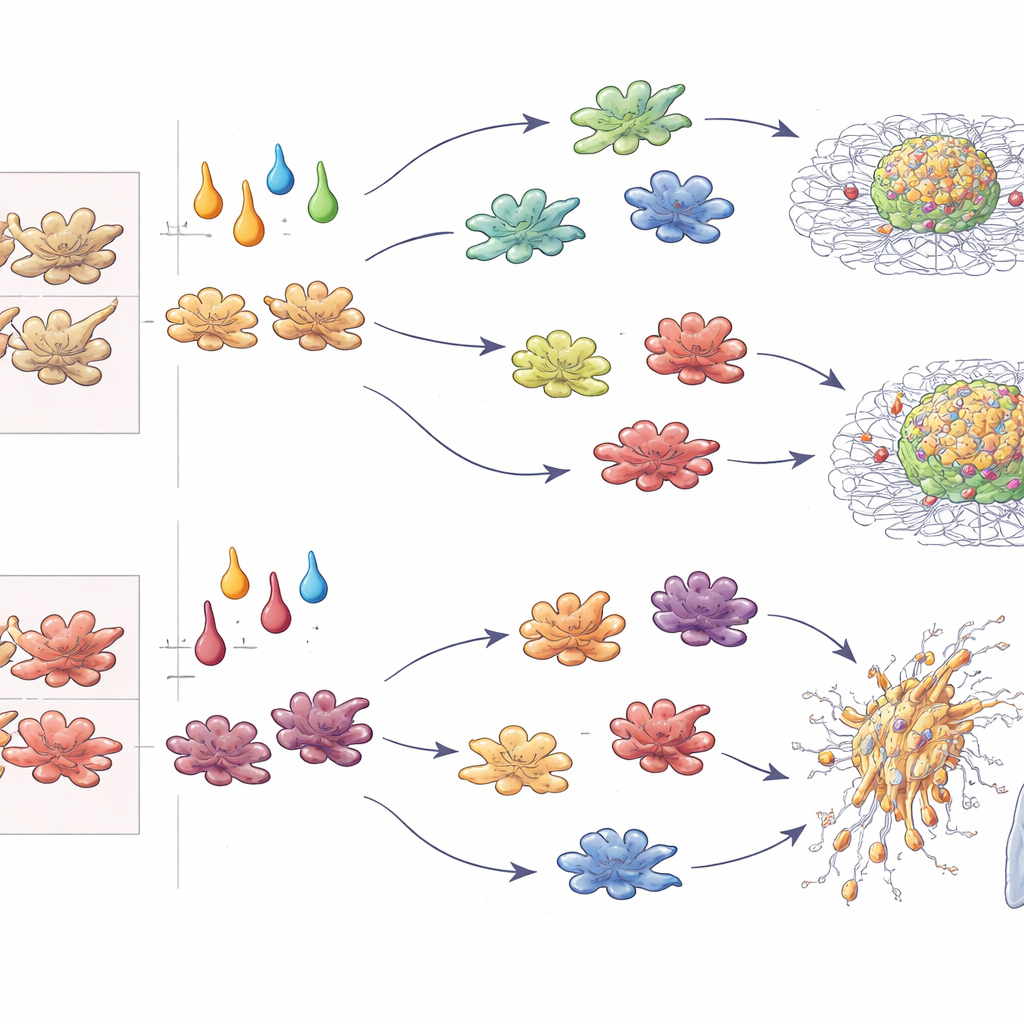
从体外球体到蔓延的肿瘤
除了基因读出,作者还量化了肿瘤球体生长速度以及它们侵入周围凝胶的深度。在3D培养中,经IL-4或TGF-β处理的M-CSF巨噬细胞显著促进了肿瘤扩张和径向侵入,而IFN-γ极化的细胞则杀伤或限制了肿瘤。引人注目的是,当相同细胞因子作用于GM-CSF巨噬细胞时,IL-4角色转换,反而抑制了肿瘤生长,而IL-10和TGF-β则驱动了最具侵袭性的行为。将混合球体注入小鼠证实了这些体内模式:无论起源如何,TGF-β处理的巨噬细胞均促进肺转移;IFN-γ处理的则始终限制转移;IL-4则根据巨噬细胞来自M-CSF或GM-CSF谱系而要么增强要么阻断转移。通过将生长、侵袭、转移和T细胞刺激整合为标准化评分,作者将这些模式提炼为一个可预测巨噬细胞对肿瘤影响的“发生学—细胞因子代码”。
这对未来癌症疗法意味着什么
对非专业读者来说,主要信息是并非所有肿瘤相关巨噬细胞都相同,其行为不能用简单的好与坏或M1对M2的标签来概括。相反,这项工作表明,巨噬细胞的发育根源与其局部细胞因子环境像密码锁上的数字一样相互作用,决定其是滋养肿瘤还是帮助摧毁肿瘤。忽视这一代码的疗法——例如广泛消耗巨噬细胞或在不考虑谱系的情况下投放某种细胞因子——可能削弱自身疗效甚至产生相反效果。未来,若能判定肿瘤是由M-CSF还是GM-CSF信号主导,再据此定制细胞因子阻断或递送策略,或可将巨噬细胞由不确定的盟友转变为癌症治疗中的可靠伙伴。
引用: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
关键词: 肿瘤相关巨噬细胞, 细胞因子信号, 癌症免疫治疗, 肿瘤微环境, 转移