Clear Sky Science · de
Ein Ontogenie‑Zytokin‑Code bestimmt die Polarität von Makrophagenantworten und Tumorverläufe
Warum die „Großfresser“-Zellen des Körpers bei Krebs wichtig sind
Immunzellen, die als Makrophagen bezeichnet werden, gehören zu den zahlreichsten Zellen in soliden Tumoren. Diese zellulären „Großfresser“ können entweder Krebs bekämpfen oder dessen Ausbreitung fördern, und viele neue Therapien zielen darauf ab, sie in die krebsbekämpfende Richtung zu lenken. Die Ergebnisse bei Patienten sind jedoch enttäuschend, zum Teil weil uns noch eine klare Landkarte fehlt, die erklärt, was einen Makrophagen hilfreich oder schädlich macht. Diese Studie legt einen verborgenen „Code“ offen, der Herkunft eines Makrophagen, die Signale, die er wahrnimmt, und wie er letztlich Tumorwachstum und Metastasenbildung beeinflusst, miteinander verknüpft.
Zwei Makrophagenfamilien, viele mögliche Schicksale
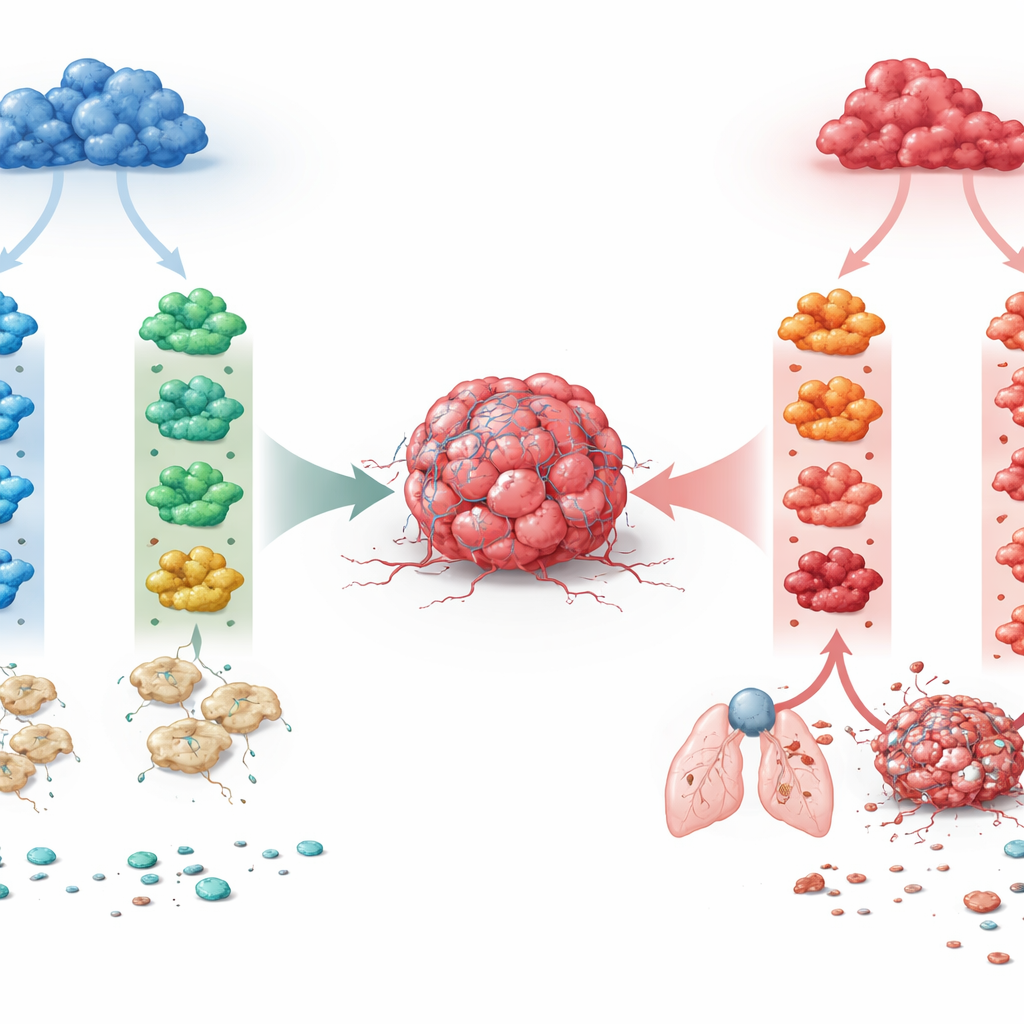
Die Forschenden konzentrierten sich auf zwei große Makrophagen‑Linien, die in vielen Geweben vorkommen. Die eine Linie ist abhängig von einem Wachstumsfaktor namens M‑CSF und trägt tendenziell zur alltäglichen Gewebe‑Homöostase bei. Die andere entsteht unter dem inflammatorischen Wachstumsfaktor GM‑CSF und ist von Natur aus reaktiver. Aus Knochenmark von Mäusen züchtete das Team Makrophagen in Richtung einer der beiden Linien und setzte sie anschließend vier Immun‑Signalen aus, die in Tumoren häufig vorkommen: IFN-γ, IL-4, IL-10 und TGF-β. So entstanden acht klar definierte Makrophagenzustände. Durch Ablesen der globalen Genaktivität mit Bulk‑ und Einzelzell‑RNA‑Sequenzierung zeigte sich, dass die entwicklungsbedingte Herkunft der dominante Faktor war: Sie trennte die beiden Linien stärker als jedes einzelne Zytokin. Dasselbe Signal konnte daher die beiden Makrophagenfamilien in sehr unterschiedliche genetische und funktionelle Programme treiben.
Wie dasselbe Signal vom Freund zum Feind werden kann
Eine Schlüsselerkenntnis war, dass IL‑4, ein Zytokin, das lange mit Wundheilung und „alternativer“ Aktivierung assoziiert ist, je nach Makrophagenherkunft gegensätzliche Wirkungen hatte. Wirkte IL‑4 auf M‑CSF‑abgeleitete Makrophagen, löste es Genprogramme aus, die mit Gewebeumbau verbunden sind, induzierte das Enzym ARG1, verlieh den Zellen eine längliche Form und verringerte ihre Fähigkeit, Antigen T‑Zellen zu präsentieren. Funktionell förderten diese Makrophagen Tumorwachstum, Invasion in die umgebende Matrix und Aussaat von Lungenmetastasen. Im Gegensatz dazu trieb IL‑4 bei GM‑CSF‑abgeleiteten Makrophagen einen stärker inflammatorischen, dendritischen Zustand mit ausgeprägter Antigenpräsentation und tumor‑unterdrückendem Verhalten voran. Somit konnte dasselbe Zytokin je nach entwicklungsbedingtem Hintergrund des Makrophagen entweder Krebs nähren oder seine Eindämmung unterstützen. Ein ähnlicher, wenn auch weniger dramatischer, linienabhängiger Unterschied zeigte sich für IL‑10, während IFN‑γ durchgehend tumorbekämpfend und TGF‑β durchgehend tumorfördernd in beiden Linien blieb.
Beobachtung, wie Tumoren und Makrophagen sich gegenseitig formen
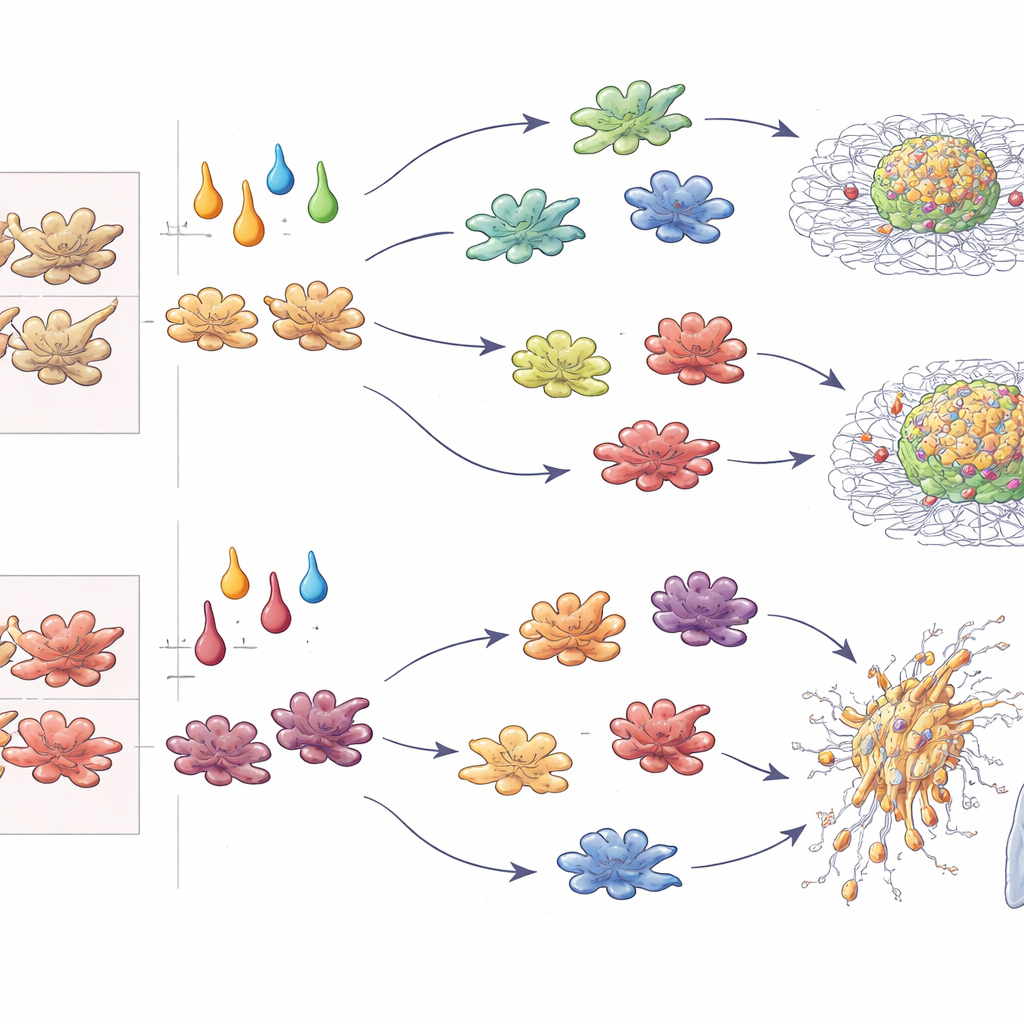
Um zu sehen, wie diese programmierten Makrophagen Tumorzellen über die Zeit beeinflussen, bauten die Forschenden dreidimensionale Spheroide, die fluoreszent markierte Krebszellen mit unterschiedlich polarisierten Makrophagen mischten. Einzelzellanalyse über mehrere Tage zeigte ein interessantes Muster. Makrophagen konvergierten, unabhängig von ihrem Ausgangszustand, allmählich zu einem gemeinsamen „tumor‑einerzogenen“ Profil, das von Reaktionen auf oxidativen Stress dominiert war. Im Gegensatz dazu diversifizierten sich die Tumorzellen. In Anwesenheit von Kontroll‑ oder IFN‑γ‑polarisierten Makrophagen teilten sich die Krebszellen weiter, zeigten aber nur begrenztes invasives Verhalten. Wurden sie mit IL‑4‑ oder TGF‑β‑behandelten M‑CSF‑Makrophagen oder mit IL‑10/TGF‑β‑behandelten GM‑CSF‑Makrophagen ko‑kultiviert, verschoben sich die Tumorzellen in Richtung einer epithelial‑zu‑mesenchymalen, invasionsbereiten Identität. Obwohl die Genprofile der Makrophagen später vom Tumor umgeformt wurden, hatte ihre anfängliche Programmierung die Krebszellen bereits auf sehr unterschiedliche Bahnen gelenkt.
Von Labor‑Spheroiden zu sich ausbreitenden Tumoren
Über Genablesungen hinaus quantifizierten die Autorinnen und Autoren, wie schnell Tumorspheroide wuchsen und wie tief sie in ein umgebendes Gel invasiv eindrangen. In 3D‑Kultur steigerten M‑CSF‑Makrophagen, die mit IL‑4 oder TGF‑β behandelt wurden, stark die Tumorexpansion und radiale Invasion, während IFN‑γ‑polarisierte Zellen Tumore abtöteten oder einschränkten. Auffällig war, dass dieselben Zytokine bei GM‑CSF‑Makrophagen andere Rollen einnahmen: IL‑4 schaltete die Rolle um und unterdrückte nun das Tumorwachstum, während IL‑10 und TGF‑β das aggressivste Verhalten förderten. Das Injizieren gemischter Spheroide in Mäuse bestätigte diese Muster in vivo: TGF‑β‑konditionierte Makrophagen förderten Lungenmetastasen unabhängig von der Herkunft; IFN‑γ‑konditionierte beschränkten sie konsequent; IL‑4 verstärkte oder blockierte Metastasen je nachdem, ob die Makrophagen aus der M‑CSF‑ oder GM‑CSF‑Linie stammten. Durch die Kombination von Wachstum, Invasion, Metastasierung und T‑Zell‑Stimulation zu standardisierten Scores destillierten die Autorinnen und Autoren diese Muster in einen „Ontogenie–Zytokin‑Code“, der die Auswirkung von Makrophagen auf Tumoren vorhersagt.
Was das für künftige Krebstherapien bedeutet
Für Nicht‑Spezialisten lautet die Kernbotschaft: Nicht alle tumorassoziierten Makrophagen sind gleich, und ihr Verhalten lässt sich nicht mit einer einfachen Gut‑gegen‑Böse‑ oder M1‑gegen‑M2‑Einteilung erfassen. Stattdessen zeigt diese Arbeit, dass die entwicklungsbedingten Wurzeln eines Makrophagen und seine lokale Zytokin‑Umgebung wie Ziffern eines Zahlenschlosses zusammenwirken, um zu entscheiden, ob er einen Tumor nährt oder bei seiner Zerstörung hilft. Therapien, die diesen Code ignorieren – etwa durch breit angelegtes Depletieren von Makrophagen oder das Verabreichen eines Zytokins ohne Beachtung der Linie – könnten ihre eigene Wirksamkeit abschwächen oder sogar schädlich wirken. Künftige Ansätze, die zuerst analysieren, ob ein Tumor von M‑CSF‑ oder GM‑CSF‑Signalgebung dominiert wird, und dann Zytokin‑blockierende oder ‑liefernde Medikamente entsprechend anpassen, könnten Makrophagen von ungewissen Verbündeten in verlässliche Partner der Krebstherapie verwandeln.
Zitation: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
Schlüsselwörter: tumorassoziierte Makrophagen, Zytokin‑Signalgebung, Krebsimmuntherapie, Tumormikroumgebung, Metastase