Clear Sky Science · sv
En ontogenetisk-cytokinkod bestämmer makrofagers responspolaritet och tumörutfall
Varför kroppens "stora ätare" är viktiga vid cancer
Immunceller som kallas makrofager är bland de mest talrika cellerna i solida tumörer. Dessa cellulära "stora ätare" kan antingen attackera cancer eller hjälpa den att sprida sig, och många nya behandlingar syftar till att styra dem mot den cancerbekämpande sidan. Ändå har resultaten hos patienter varit nedslående, delvis eftersom vi fortfarande saknar en tydlig karta över vad som gör en makrofag hjälpsam eller skadlig. Denna studie avslöjar en dold "kod" som länkar var en makrofag härstammar ifrån, vilka signaler den ser och hur den slutligen formar tumörtillväxt och metastasering.
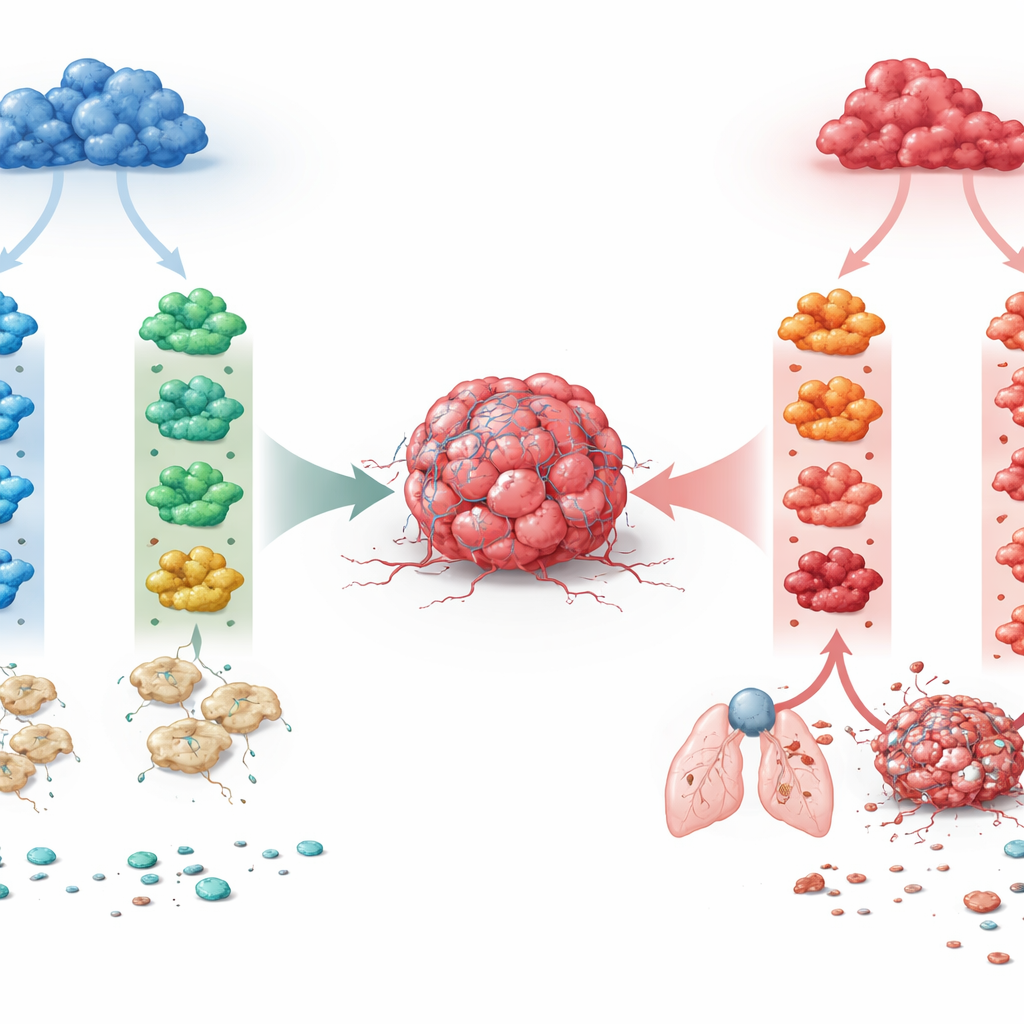
Två makrofagfamiljer, många möjliga öden
Forskarna fokuserade på två huvudsakliga makrofaglinjer som finns i många vävnader. Den ena linjen är beroende av en tillväxtfaktor kallad M-CSF och tenderar att upprätthålla vardaglig vävnadsbalans. Den andra uppstår under en inflammatorisk tillväxtfaktor, GM-CSF, och är naturligt mer reaktiv. Från musens benmärg odlade teamet makrofager längs vardera linje och exponerade dem sedan för fyra immunsignaler som ofta förekommer i tumörer: IFN-γ, IL-4, IL-10 och TGF-β. Detta gav upphov till åtta väldefinierade makrofagtillstånd. Genom att läsa av global genaktivitet med bulk- och single-cell RNA-sekvensering fann de att utvecklingsursprung var den dominerande kraften: det skilde de två linjerna starkare än någon enstaka cytokin. Samma signal kunde alltså driva de två makrofagfamiljerna in i mycket olika genetiska och funktionella program.
Hur samma signal kan växla från vän till fiende
En nyckelupptäckt var att IL-4, en cytokin länge förknippad med sårreparation och "alternativ" aktivering, hade motsatta effekter beroende på makrofagens ursprung. När IL-4 verkade på M-CSF–härledda makrofager aktiverade det genprogram kopplade till vävnadsombyggnad, inducerade enzymet ARG1, gav cellerna en förlängd form och minskade deras förmåga att presentera antigen för T-celler. Funktionellt stödde dessa makrofager tumörtillväxt, invasion i omgivande matrix och sådd av lungmetastaser. I kontrast drev IL-4 som verkade på GM-CSF–härledda makrofager ett mer inflammatoriskt, dendritcellsliknande tillstånd med stark antigenpresentation och tumörhämmande beteende. Således kunde samma cytokin antingen främja cancer eller hjälpa till att hejda den, beroende på makrofagens utvecklingsbakgrund. En liknande, om än mindre dramatisk, linjeberoende uppdelning observerades för IL-10, medan IFN-γ konsekvent förblev tumörbekämpande och TGF-β konsekvent tumörfrämjande över båda linjerna.
Att iaktta hur tumörer och makrofager formar varandra
För att se hur dessa programmerade makrofager påverkar tumörceller över tid byggde teamet tredimensionella sfäroider som blandade fluorescerande märkta cancerceller med olika polariserade makrofager. Single-cell-analys över flera dagar avslöjade ett intressant mönster. Makrofager, oavsett deras utgångstillstånd, konvergerade gradvis mot en gemensam "tumörutbildad" profil dominerad av responser på oxidativ stress. Däremot diversifierades tumörcellerna. I närvaro av kontroll- eller IFN-γ–polariserade makrofager fortsatte cancercellerna att dela sig men visade begränsat invasivt beteende. När de samexponerades med IL-4– eller TGF-β–behandlade M-CSF-makrofager — eller med IL-10/TGF-β–behandlade GM-CSF-makrofager — skiftade tumörcellerna mot en epitel-till-mesenkymal, invasionsbered identitet. Även om makrofagernas gensignaturer senare omformades av tumören hade deras initiala programmering redan styrt cancercellerna in på mycket olika banor.
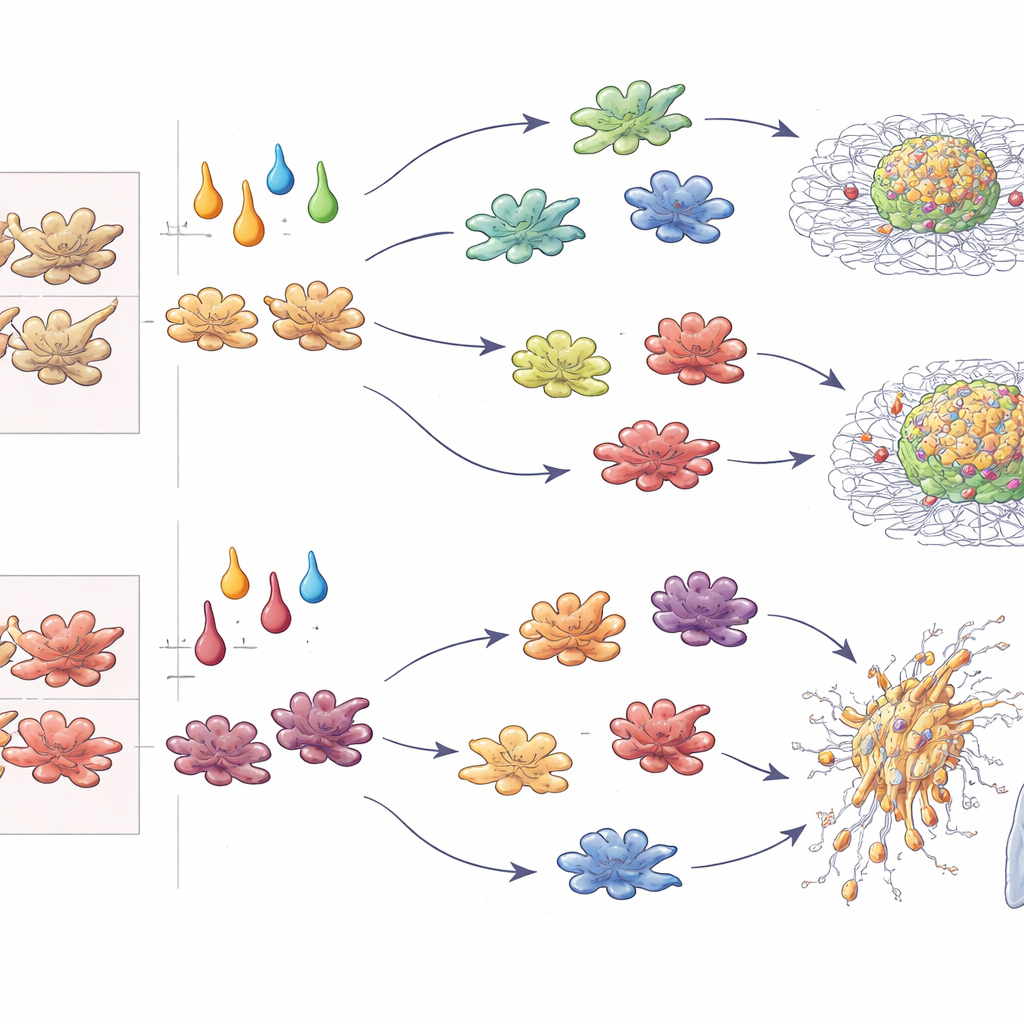
Från laboratoriesfäroider till spridande tumörer
Utöver genavläsningar kvantifierade författarna hur snabbt tumörsfäroiderna växte och hur djupt de invaderade en omgivande gel. I 3D-kultur ökade M-CSF-makrofager behandlade med IL-4 eller TGF-β starkt tumörekspansion och radiell invasion, medan IFN-γ–polariserade celler dödade eller begränsade tumörer. Slående nog, när samma cytokiner verkade på GM-CSF-makrofager bytte IL-4 roll och undertryckte nu tumörtillväxt, medan IL-10 och TGF-β drev det mest aggressiva beteendet. Injektion av blandade sfäroider i möss bekräftade dessa mönster in vivo: TGF-β–konditionerade makrofager främjade lungmetastaser oavsett ursprung; IFN-γ–konditionerade konsekvent begränsade dem; IL-4 antingen ökade eller blockerade metastasering beroende på om makrofagerna kom från M-CSF- eller GM-CSF-linjen. Genom att kombinera tillväxt, invasion, metastas och T-cellsstimulering i standardiserade poäng destillerade författarna dessa mönster till en "ontogeny–cytokin-kod" som förutspår makrofagers påverkan på tumörer.
Vad detta betyder för framtida cancerterapier
För icke-specialister är huvudbudskapet att inte alla tumörassocierade makrofager är skapade lika, och deras beteende fångas inte av en enkel god-mot-ond- eller M1-mot-M2-etikett. I stället visar detta arbete att en makrofags utvecklingsrötter och dess lokala cytokinmiljö samverkar som siffror i ett kombinationslås för att avgöra om den kommer att föda en tumör eller hjälpa till att förstöra den. Terapier som ignorerar denna kod — till exempel genom att brett utrota makrofager eller leverera en cytokin utan hänsyn till linjetillhörighet — kan dämpa sin egen effektivitet eller till och med slå tillbaka. I framtiden kan profilering av om en tumör domineras av M-CSF- eller GM-CSF-signalering, och därefter skräddarsydda cytokin-blockerande eller cytokinlevererande läkemedel, förvandla makrofager från osäkra allierade till pålitliga partners i cancerbehandling.
Citering: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
Nyckelord: tumörassocierade makrofager, cytokinsignalering, cancerimmunterapi, tumörmikromiljö, metastas