Clear Sky Science · fr
Un code ontogénétique-cytokinique détermine la polarité de la réponse des macrophages et les issues tumorales
Pourquoi les cellules « gros mangeurs » du corps comptent dans le cancer
Les cellules immunitaires appelées macrophages figurent parmi les cellules les plus abondantes à l’intérieur des tumeurs solides. Ces « gros mangeurs » cellulaires peuvent soit attaquer le cancer, soit favoriser sa propagation, et de nombreux traitements récents cherchent à les orienter vers le versant anticancéreux. Pourtant, les résultats chez les patients ont été décevants, en partie parce qu’il nous manque encore une cartographie claire des facteurs qui rendent un macrophage utile ou nuisible. Cette étude révèle un « code » caché qui relie l’origine d’un macrophage, les signaux qu’il reçoit et la manière dont il influence en fin de compte la croissance tumorale et les métastases.
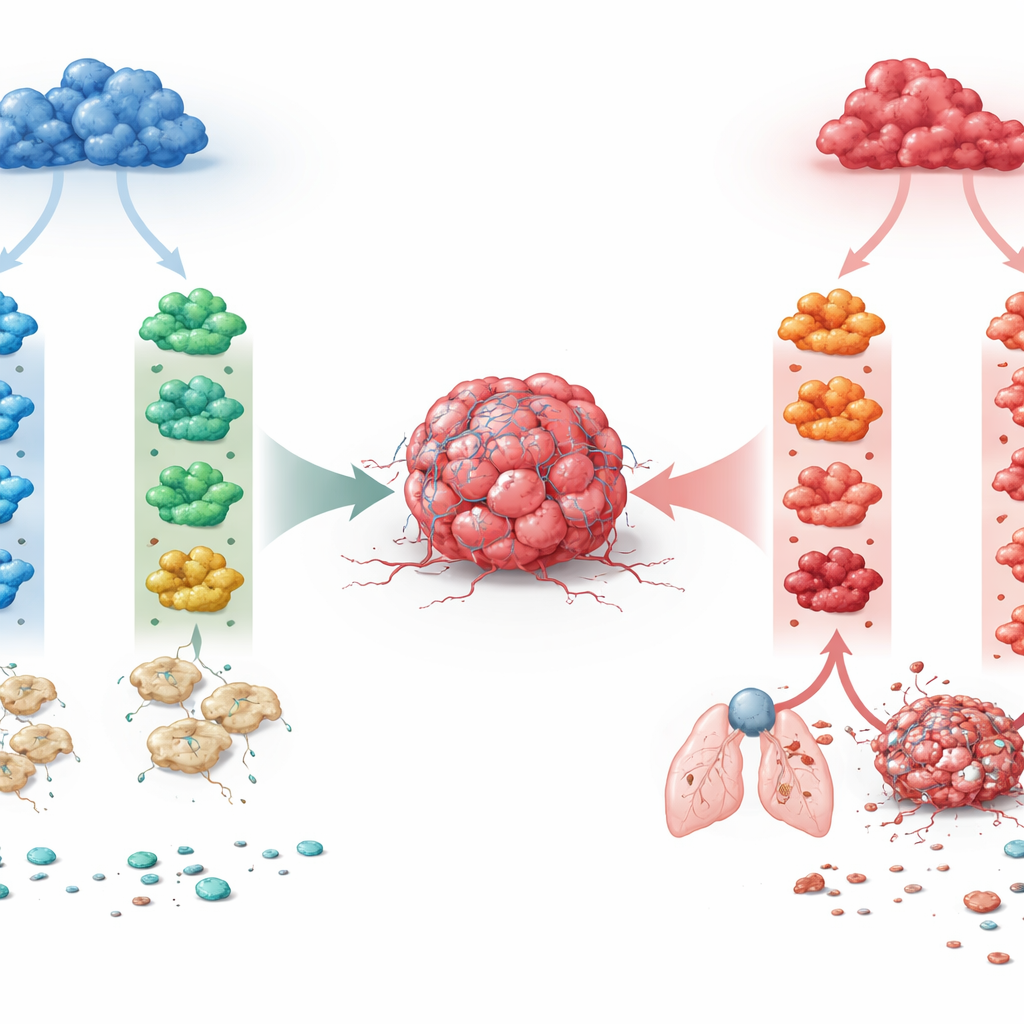
Deux familles de macrophages, de nombreux destins possibles
Les chercheurs se sont concentrés sur deux grandes lignées de macrophages présentes dans de nombreux tissus. Une lignée dépend d’un facteur de croissance appelé M-CSF et tend à maintenir l’homéostasie tissulaire au quotidien. L’autre émerge sous l’effet d’un facteur pro-inflammatoire, le GM-CSF, et est naturellement plus réactive. À partir de moelle osseuse murine, l’équipe a développé des macrophages selon l’une ou l’autre lignée, puis les a exposés à quatre signaux immunitaires fréquemment présents dans les tumeurs : IFN-γ, IL-4, IL-10 et TGF-β. Cela a produit huit états macrophagiques bien définis. En mesurant l’activité génique globale par séquençage ARN en masse et en cellule unique, ils ont constaté que l’origine développementale était la force dominante : elle séparait les deux lignées plus fortement que n’importe quelle cytokine prise isolément. Le même signal pouvait donc pousser les deux familles de macrophages vers des programmes génétiques et fonctionnels très différents.
Comment un même signal peut passer d’ami à ennemi
Une découverte clé est que l’IL-4, une cytokine traditionnellement associée à la réparation tissulaire et à une activation « alternative », avait des effets opposés selon l’origine du macrophage. Quand l’IL-4 agissait sur des macrophages dérivés de M-CSF, elle déclenchait des programmes géniques liés au remodelage tissulaire, induisait l’enzyme ARG1, donnait aux cellules une forme allongée et réduisait leur capacité à présenter l’antigène aux lymphocytes T. Fonctionnellement, ces macrophages favorisaient la croissance tumorale, l’invasion de la matrice environnante et l’ensemencement de métastases pulmonaires. En revanche, l’IL-4 agissant sur des macrophages dérivés de GM-CSF induisait un état plus inflammatoire, proche des cellules dendritiques, avec une forte présentation d’antigène et un comportement suppresseur de tumeur. Ainsi, la même cytokine pouvait soit alimenter le cancer, soit contribuer à le contenir, selon l’origine développementale du macrophage. Une division dépendante de la lignée, quoique moins marquée, a été observée pour l’IL-10, tandis que l’IFN-γ restait systématiquement anti-tumoral et le TGF-β systématiquement pro-tumoral dans les deux lignées.
Observer la co-évolution des tumeurs et des macrophages
Pour voir comment ces macrophages programmés influencent les cellules tumorales au fil du temps, l’équipe a construit des sphéroïdes tridimensionnels mélangeant des cellules cancéreuses marquées par fluorescence et des macrophages polarisés différemment. L’analyse en cellule unique sur plusieurs jours a révélé un schéma intéressant. Les macrophages, quel que soit leur état initial, convergaient progressivement vers un profil commun « éduqué par la tumeur » dominé par des réponses au stress oxydatif. En revanche, les cellules tumorales se diversifiaient. En présence de macrophages témoins ou polarisés par IFN-γ, les cellules cancéreuses continuaient de se diviser mais montraient peu de comportement invasif. Lorsqu’elles étaient co-cultivées avec des macrophages M-CSF traités par IL-4 ou TGF-β — ou avec des macrophages GM-CSF traités par IL-10/TGF-β — les cellules tumorales basculaient vers un phénotype épithélial-vers-mésenchymateux prêt à envahir. Même si les signatures géniques des macrophages étaient ensuite remodelées par la tumeur, leur programmation initiale avait déjà orienté les cellules cancéreuses vers des trajectoires très différentes.
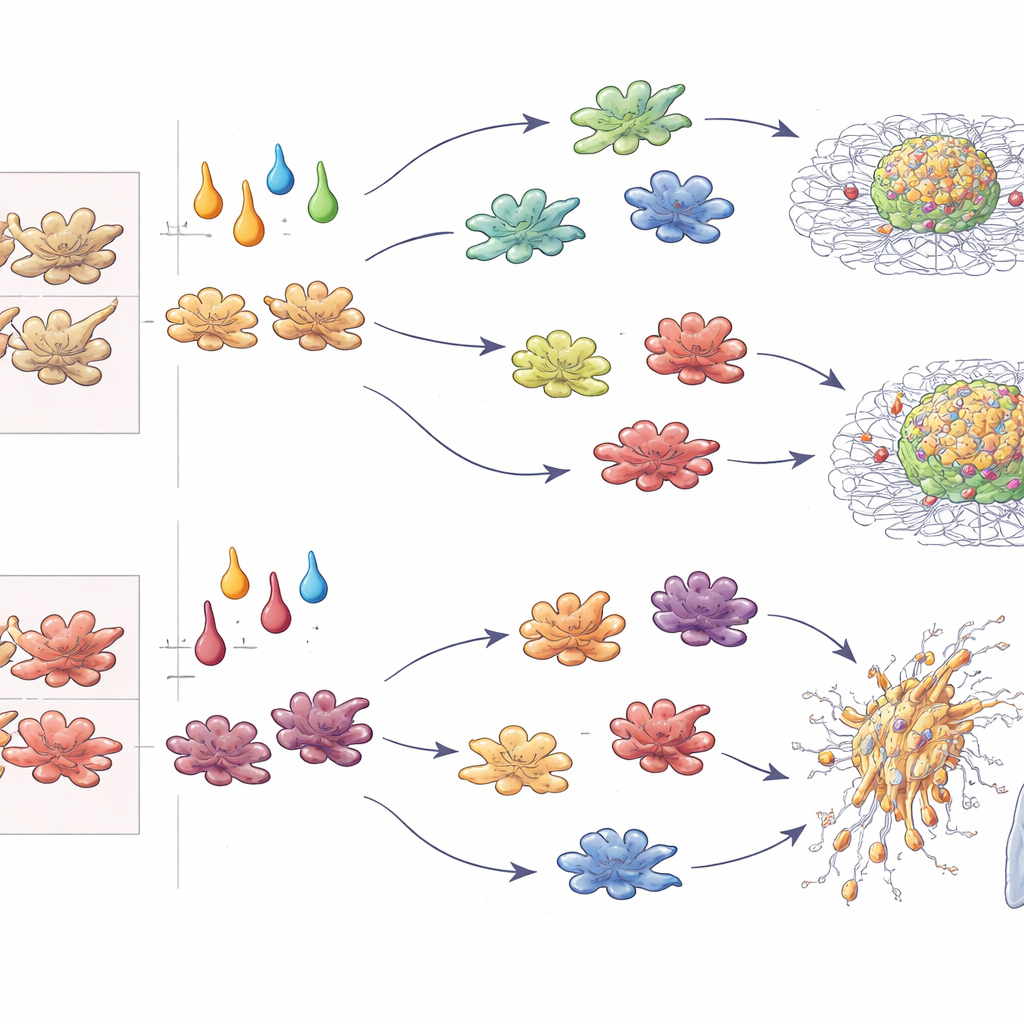
Des sphéroïdes de laboratoire aux tumeurs disséminées
Au-delà des profils géniques, les auteurs ont quantifié la vitesse de croissance des sphéroïdes tumoraux et la profondeur d’invasion dans un gel environnant. En culture 3D, les macrophages M-CSF traités par IL-4 ou TGF-β augmentaient fortement l’expansion tumorale et l’invasion radiale, tandis que les cellules polarisées par IFN-γ tuaient ou freinaient les tumeurs. De manière frappante, lorsque les mêmes cytokines agissaient sur des macrophages GM-CSF, l’IL-4 changeait de rôle et supprimait la croissance tumorale, alors que l’IL-10 et le TGF-β suscitaient le comportement le plus agressif. L’injection de sphéroïdes mixtes chez la souris a confirmé ces schémas in vivo : les macrophages conditionnés par le TGF-β favorisaient les métastases pulmonaires quelle que soit leur origine ; ceux conditionnés par l’IFN-γ les limitaient systématiquement ; l’IL-4 augmentait ou bloquait les métastases selon que les macrophages provenaient de la lignée M-CSF ou GM-CSF. En combinant croissance, invasion, métastase et stimulation des cellules T en scores standardisés, les auteurs ont synthétisé ces schémas en un « code ontogénie–cytokine » qui prédit l’impact des macrophages sur les tumeurs.
Ce que cela signifie pour les thérapies anticancers futures
Pour les non-spécialistes, le message principal est que tous les macrophages associés aux tumeurs ne se valent pas, et que leur comportement ne peut pas être résumé par une simple étiquette bon-contre-mauvais ou M1-contre-M2. Ce travail montre plutôt que les racines développementales d’un macrophage et son environnement local en cytokines interagissent comme des chiffres dans un cadenas à combinaison pour décider s’il nourrira la tumeur ou contribuera à la détruire. Des thérapies qui ignorent ce code — par exemple en éliminant massivement les macrophages ou en délivrant une cytokine sans tenir compte de la lignée — risquent d’affaiblir leur propre efficacité voire d’être contre-productives. À l’avenir, profiler si une tumeur est dominée par une signalisation M-CSF ou GM-CSF, puis adapter des médicaments bloquant ou délivrant des cytokines en conséquence, pourrait transformer les macrophages d’alliés incertains en partenaires fiables dans le traitement du cancer.
Citation: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
Mots-clés: macrophages associés aux tumeurs, signalisation des cytokines, immunothérapie du cancer, <keyword>métastase