Clear Sky Science · ar
شفرة تطورية-سايتوكين تحدد قطبية استجابة البلاعم ونتائج الأورام
لماذا تهم خلايا «الالتهام الكبيرة» بالجسم في السرطان
خلايا مناعية تُدعى البلاعم تعد من بين أكثر الخلايا وفرة داخل الأورام الصلبة. هذه «الالتهامات الكبيرة» الخلوية يمكن أن تهاجم السرطان أو تساعده على الانتشار، وتسعى العديد من العلاجات الحديثة إلى دفعها نحو الجانب المقاتل للسرطان. لكن النتائج لدى المرضى كانت مخيّبة، جزئياً لأننا ما زلنا نفتقر إلى خريطة واضحة لما يجعل البلاعم مفيدة أو ضارة. تكشف هذه الدراسة عن «شفرة» مخفية تربط مصدر البلاعم، والإشارات التي تتعرض لها، وكيف تؤثر في النهاية على نمو الورم وانتشاره.
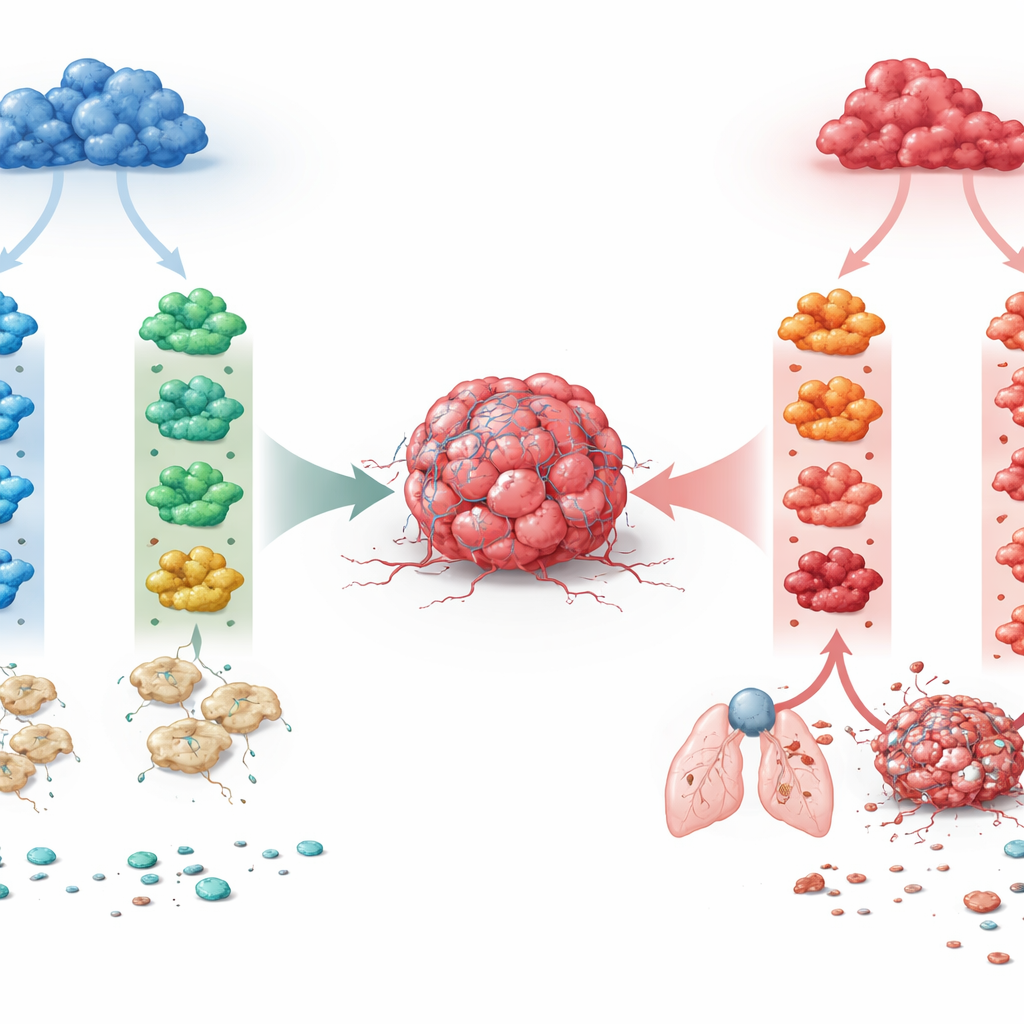
عائلتان من البلاعم، ومسارات كثيرة ممكنة
ركز الباحثون على سلالتين رئيسيتين من البلاعم الموجودتين في أنسجة عديدة. تعتمد إحدى السلالتين على عامل نمو يُسمى M-CSF وتميل إلى المحافظة على توازن الأنسجة في الأحوال الطبيعية. تنشأ الأخرى تحت عامل نمو التهابي، GM-CSF، وتكون بطبيعتها أكثر تفاعلاً. من نخاع عظم الفئران، نما الفريق البلاعم على طول كل سلالة، ثم عرضها لأربع إشارات مناعية تتواجد كثيراً في الأورام: IFN-γ وIL-4 وIL-10 وTGF-β. أنتج ذلك ثمانية حالات بلاعم محددة جيداً. بقراءة النشاط الجيني الشامل عبر تسلسل RNA الخلوي الكتلي والفردي، وجدوا أن الأصل التطوري كان القوة المهيمنة: فقد فصل السلالتين بقوة أكبر من أي سايتوكين منفرد. وبذلك يمكن للإشارة نفسها أن تدفع عائلتي البلاعم إلى برامج جينية ووظيفية مختلفة جداً.
كيف يمكن أن تتحول نفس الإشارة من صديق إلى عدو
كان اكتشاف رئيسي أن IL-4، وهو سايتوكين مرتبط منذ زمن بالتصليح الجِرحي والتنشيط «البديل»، له تأثيرات متعاكسة اعتماداً على أصل البلاعم. عند تأثير IL-4 على البلاعم المشتقة من M-CSF، أطلق برامج جينية مرتبطة بإعادة تشكيل الأنسجة، وحفّز إنزيم ARG1، وأعطى الخلايا شكلًا ممدودًا، وقلل قدرتها على عرض المستضد للخلايا التائية. وظيفياً، دعمت هذه البلاعم نمو الورم والغزو إلى المصفوفة المحيطة وبذر النقائل الرئوية. في المقابل، أدى IL-4 على البلاعم المشتقة من GM-CSF إلى حالة أكثر التهابية، أشبه بالخلايا الشجرية، مع عرض قوي للمستضد وسلوك مثبط للورم. هكذا، يمكن للسايتوكين نفسه أن يزود السرطان بالوقود أو يساعد في تقييده، اعتماداً على الخلفية التطورية للبلاعم. لوحظ انقسام اعتماداً على السلالة أيضاً بالنسبة لـIL-10، وإن كان أقل دراماتيكية، بينما ظل IFN-γ مقاوماً للأورام بشكل ثابت وTGF-β محفزاً للورم عبر كلا السلالتين.
مراقبة كيف يشكل الورم والبلاعم بعضهما بعضاً
لمعرفة كيف تؤثر هذه البلاعم المبرمجة على خلايا الورم مع مرور الوقت، بنى الفريق كُرَيّات ثلاثية الأبعاد مزجت خلايا سرطانية معلمة فلوريسينياً مع بلاعم مستقطبة بشكل مختلف. كشف التحليل الخلوي الفردي على مدى عدة أيام نمطاً مثيراً: تلاقت البلاعم، بغض النظر عن حالتها الابتدائية، تدريجياً على ملف «متعلم من الورم» مشترك تهيمن عليه استجابات الإجهاد التأكسدي. بالمقابل، تنوّعت خلايا الورم. في وجود بلاعم الضابطة أو البلاعم المستقطبة بـIFN-γ، واصلت خلايا السرطان الانقسام لكن أظهرت سلوكاً غزوياً محدوداً. عند التعايش مع بلاعم M-CSF المعالجة بـIL-4 أو TGF-β — أو مع بلاعم GM-CSF المعالجة بـIL-10/TGF-β — انحرفت خلايا الورم نحو هوية من النوع الظهاري إلى اللحمي ممهدة للغزو. مع أن تواقيع الجينات لدى البلاعم أعيد تشكيلها لاحقاً بفعل الورم، فإن برمجتها الأولية كانت قد وجهت خلايا السرطان بالفعل إلى مسارات مختلفة جداً.
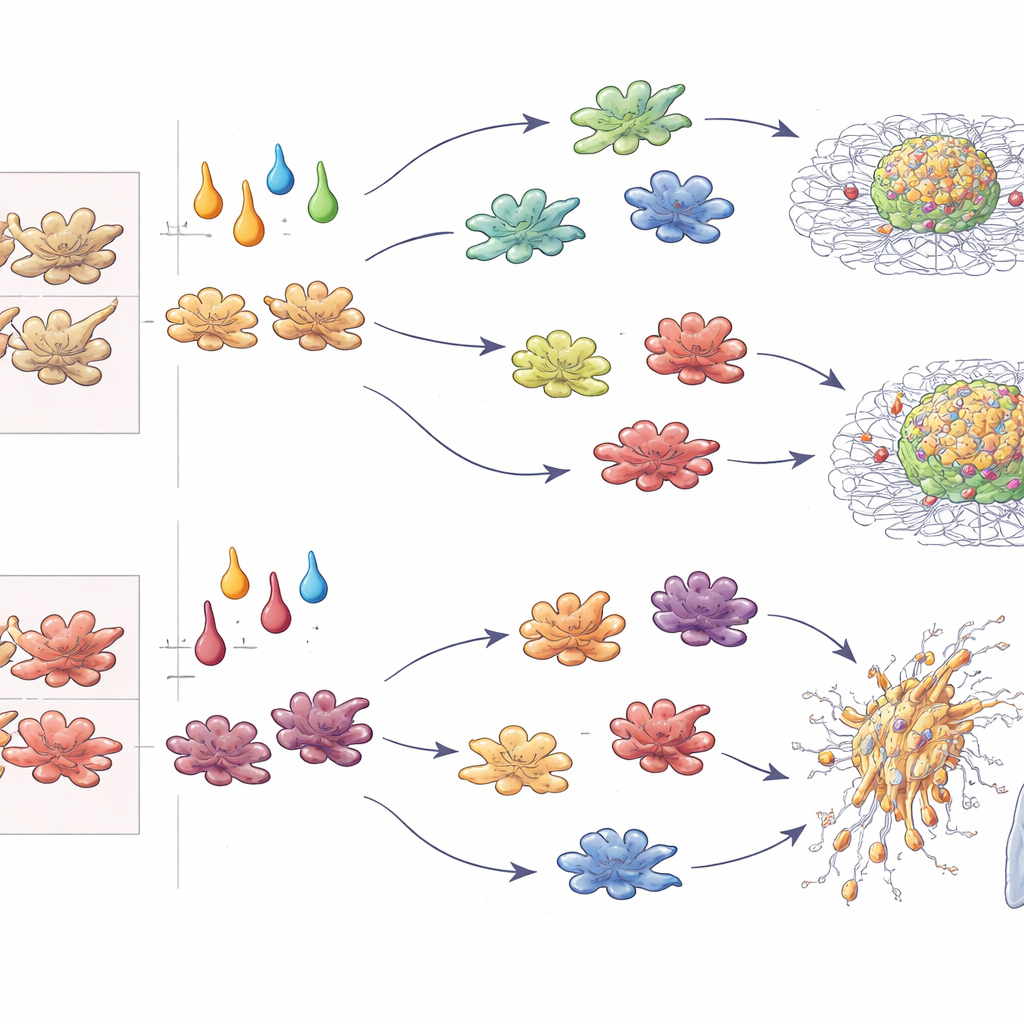
من كُريات المختبر إلى الأورام المنتشرة
بعيداً عن قراءات الجينات، قاس المؤلفون مدى سرعة نمو كُرَيّات الورم وعمق غزوها لمحلول هلامي محيط. في الزراعة ثلاثية الأبعاد، عززت البلاعم المشتقة من M-CSF والمعالجة بـIL-4 أو TGF-β توسيع الورم والغزو الشعاعي بشكل قوي، بينما قتلت الخلايا المستقطبة بـIFN-γ الأورام أو قيدتها. لافت للنظر، عندما أثرت نفس السايتوكينات على بلاعم GM-CSF، قلب IL-4 دوره فصار يكبح نمو الورم، في حين قادت IL-10 وTGF-β السلوك الأكثر عدوانية. حقن الكُرَيّات المختلطة في الفئران أكد هذه الأنماط في الجسم الحي: شجعت البلاعم المهيأة بـTGF-β النقائل الرئوية بغض النظر عن الأصل؛ حدّت البلاعم المهيأة بـIFN-γ منها باستمرار؛ أما IL-4 فزاد أو منع النقائل حسب ما إذا كانت البلاعم من سلالة M-CSF أو GM-CSF. من خلال جمع النمو والغزو والنقائل وتحفيز الخلايا التائية في درجات موحدة، استخلص المؤلفون هذه الأنماط إلى «شفرة تطورية–سايتوكين» تتنبأ بتأثير البلاعم على الأورام.
ماذا يعني هذا لعلاجات السرطان المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن جميع البلاعم المرتبطة بالورم ليست متساوية، ولا يمكن التقاط سلوكها بتسمية بسيطة جيدة-مضرة أو M1-مقابل-M2. بدلاً من ذلك، يُظهر هذا العمل أن جذور البلاعم التطورية وبيئتها المحلية من السايتوكينات تتفاعلان مثل أرقام في قفل تركيبي لتقرير ما إذا كانت ستغذي الورم أو تساعد في تدميره. العلاجات التي تتجاهل هذه الشفرة — مثلاً عبر استنزاف البلاعم على نطاق واسع أو توصيل سايتوكين دون مراعاة السلالة — قد تضعف فعاليتها أو تعود بنتائج عكسية. في المستقبل، قد يؤدي تحديد ما إذا كان الورم مهيمنًا عليه إشارات M-CSF أو GM-CSF، ومن ثم تخصيص أدوية حجب أو توصيل السايتوكين وفقاً لذلك، إلى تحويل البلاعم من حلفاء مترددين إلى شركاء موثوقين في علاج السرطان.
الاستشهاد: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
الكلمات المفتاحية: البلاعم المرتبطة بالأورام, إشارة السايتوكينات, العلاج المناعي للسرطان, البيئة المجهرية للورم, النقائل