Clear Sky Science · ja
発生由来とサイトカインのコードがマクロファージの応答極性と腫瘍転帰を決定する
がんにおける“大型の貪食細胞”が重要な理由
マクロファージと呼ばれる免疫細胞は、固形腫瘍内で最も豊富に存在する細胞の一つです。これらの“大型の貪食細胞”はがんを攻撃することもあれば、逆に拡散を助けることもあり、多くの新しい治療はマクロファージをがんと戦う側に傾けることを目指しています。とはいえ、患者での成績は期待外れに終わることが多く、その一因はマクロファージが有益か有害かを決める明確な地図がまだ欠けている点にあります。本研究は、マクロファージの由来場所、どのシグナルを受けるか、そして最終的に腫瘍成長や転移をどのように形作るかを結びつける隠れた“コード”を明らかにします。
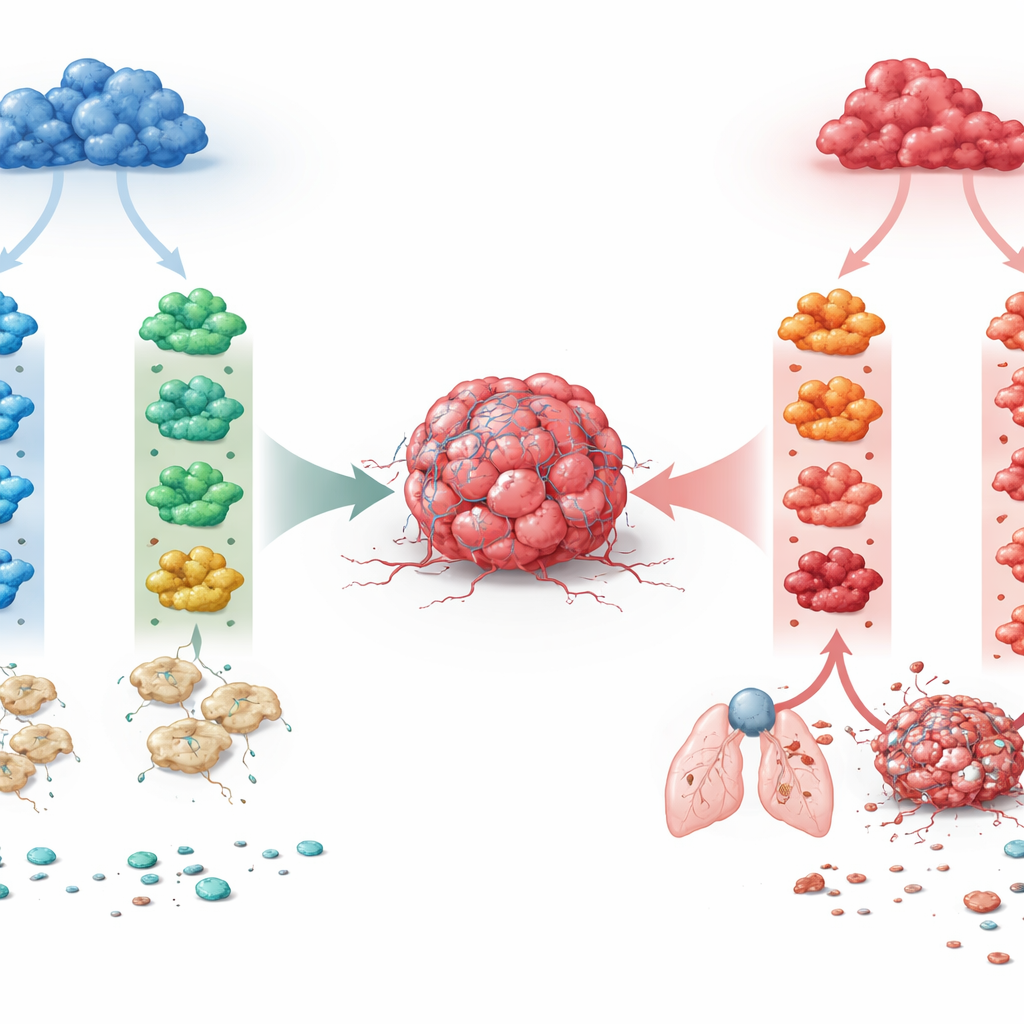
二つのマクロファージ系統、数多の運命
研究者たちは多くの組織に存在する二つの主要なマクロファージ系列に着目しました。一つはM-CSFと呼ばれる増殖因子に依存し、日常的な組織恒常性を維持する傾向があります。もう一つは炎症性の増殖因子であるGM-CSFの下で生じ、自然により反応的です。マウスの骨髄から両系列に沿ってマクロファージを培養し、腫瘍でよく見られる四つの免疫シグナル(IFN-γ、IL-4、IL-10、TGF-β)に曝露させました。これにより八つの明確に定義されたマクロファージ状態が得られました。バルクおよび単一細胞RNAシーケンシングで全遺伝子発現を読み取ると、発生起源が支配的な力であることが示されました:それは任意の単一サイトカインよりも二つの系列を強く分けました。したがって同じシグナルでも、二つのマクロファージ系統を非常に異なる遺伝的・機能的プログラムへ押しやることがあり得ます。
同じシグナルが味方から敵へ転じる仕組み
重要な発見は、長く創傷修復や「代替的」活性化と結び付けられてきたサイトカインIL-4が、マクロファージの起源によって逆の効果を示すことでした。IL-4がM-CSF由来のマクロファージに作用すると、組織再構築に関連する遺伝子プログラムが誘導され、酵素ARG1が発現し、細胞は細長い形状を取り、T細胞への抗原提示能が低下しました。機能的には、これらのマクロファージは腫瘍成長、周囲マトリックスへの侵入、肺への転移播種を支援しました。対照的に、IL-4がGM-CSF由来のマクロファージに作用すると、より炎症性で樹状細胞様の状態が誘導され、強い抗原提示と腫瘍抑制的な挙動を示しました。したがって同じサイトカインが、マクロファージの発生的背景に応じてがんを助長することも抑えることもあり得ます。IL-10でも系統依存の分岐が見られましたが程度は小さく、IFN-γは一貫して腫瘍抑制的、TGF-βは両系統で一貫して腫瘍促進的でした。
腫瘍とマクロファージが互いに形作り合う様子を観察する
これらにプログラムされたマクロファージが時間とともに腫瘍細胞にどう影響するかを調べるために、研究チームは蛍光標識したがん細胞と異なる偏向を受けたマクロファージを混ぜた三次元スフェロイドを作成しました。数日にわたる単一細胞解析は興味深いパターンを示しました。マクロファージは出発時の状態に関わらず、徐々に酸化ストレス応答が支配的な共通の“腫瘍教育”プロファイルへ収束しました。対照的に腫瘍細胞は多様化しました。コントロールまたはIFN-γ偏向マクロファージの存在下では、がん細胞は分裂を続けながらも侵襲性は限定的でした。IL-4またはTGF-βで処理したM-CSFマクロファージ、あるいはIL-10/TGF-βで処理したGM-CSFマクロファージと共培養すると、腫瘍細胞は上皮間葉転換に向かい、侵襲に備えた性質へと変化しました。マクロファージの遺伝子署名は後に腫瘍によって再形成されたにもかかわらず、初期のプログラミングは既にがん細胞を非常に異なる軌道へ導いていました。
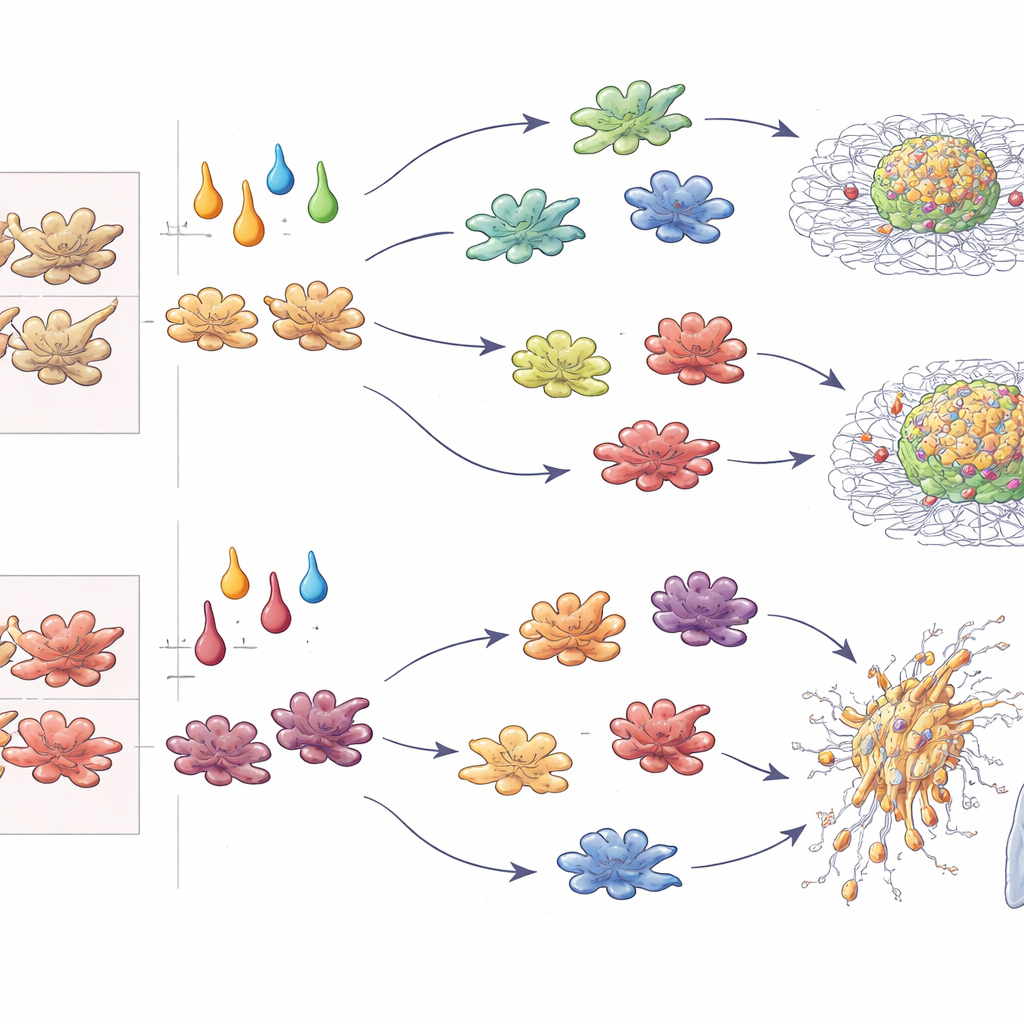
培養スフェロイドから広がる腫瘍へ
遺伝子発現だけでなく、著者らは腫瘍スフェロイドの増殖速度や周囲のゲルへの侵入深度も定量化しました。3D培養において、IL-4またはTGF-βで処理されたM-CSFマクロファージは腫瘍の拡大と放射状侵入を強く促進し、IFN-γ偏向マクロファージは腫瘍を死滅させるか制限しました。注目すべきは、同じサイトカインがGM-CSFマクロファージに作用した場合にIL-4の役割が逆転し、腫瘍成長を抑制し、IL-10とTGF-βが最も攻撃的な挙動を駆動したことです。混合スフェロイドをマウスに注入するとこれらのパターンは生体内でも確認されました:TGF-βで条件付けされたマクロファージは起源に関係なく肺転移を促進し、IFN-γで条件付けされたものは一貫してそれを制限し、IL-4はマクロファージがM-CSF系列由来かGM-CSF系列由来かによって転移を促進することも阻止することもありました。増殖、侵入、転移、T細胞刺激を標準化したスコアに統合することで、著者らはこれらのパターンをマクロファージが腫瘍に与える影響を予測する“発生–サイトカインコード”へと凝縮しました。
将来のがん治療にとっての意味
専門外の読者に向けた主なメッセージは、すべての腫瘍関連マクロファージが同じではなく、その挙動は単純な善悪やM1対M2のラベルでは捉えられないということです。本研究は、マクロファージの発生的起源と局所のサイトカイン環境が組み合わせロックの桁のように相互作用して、そのマクロファージが腫瘍を養うのか破壊するのかを決めることを示しています。このコードを無視した治療、たとえば広くマクロファージを枯渇させる、あるいは系統を考慮せずにサイトカインを投与するような方法は、自らの有効性を弱めたり、場合によっては逆効果になり得ます。将来的には、腫瘍がM-CSFまたはGM-CSFシグナル支配であるかをプロファイリングし、それに応じてサイトカインを阻害するか供給する薬を個別に調整することで、マクロファージを不確かな味方から信頼できるがん治療のパートナーへと変えることができるかもしれません。
引用: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
キーワード: 腫瘍関連マクロファージ, サイトカインシグナル, がん免疫療法, 腫瘍微小環境, 転移