Clear Sky Science · es
Un código ontogenia-citoquina determina la polaridad de respuesta de los macrófagos y los desenlaces tumorales
Por qué importan las células “gran comedora” del cuerpo en el cáncer
Las células inmunitarias llamadas macrófagos son de las más abundantes dentro de los tumores sólidos. Estos “gran comedores” celulares pueden atacar el cáncer o ayudar a su propagación, y muchos tratamientos nuevos intentan orientarlos hacia el bando antitumoral. Sin embargo, los resultados en pacientes han sido decepcionantes, en parte porque todavía carecemos de un mapa claro de qué hace que un macrófago sea útil o dañino. Este estudio revela un “código” oculto que vincula el origen de un macrófago, las señales que percibe y cómo, en última instancia, condiciona el crecimiento tumoral y la metástasis.
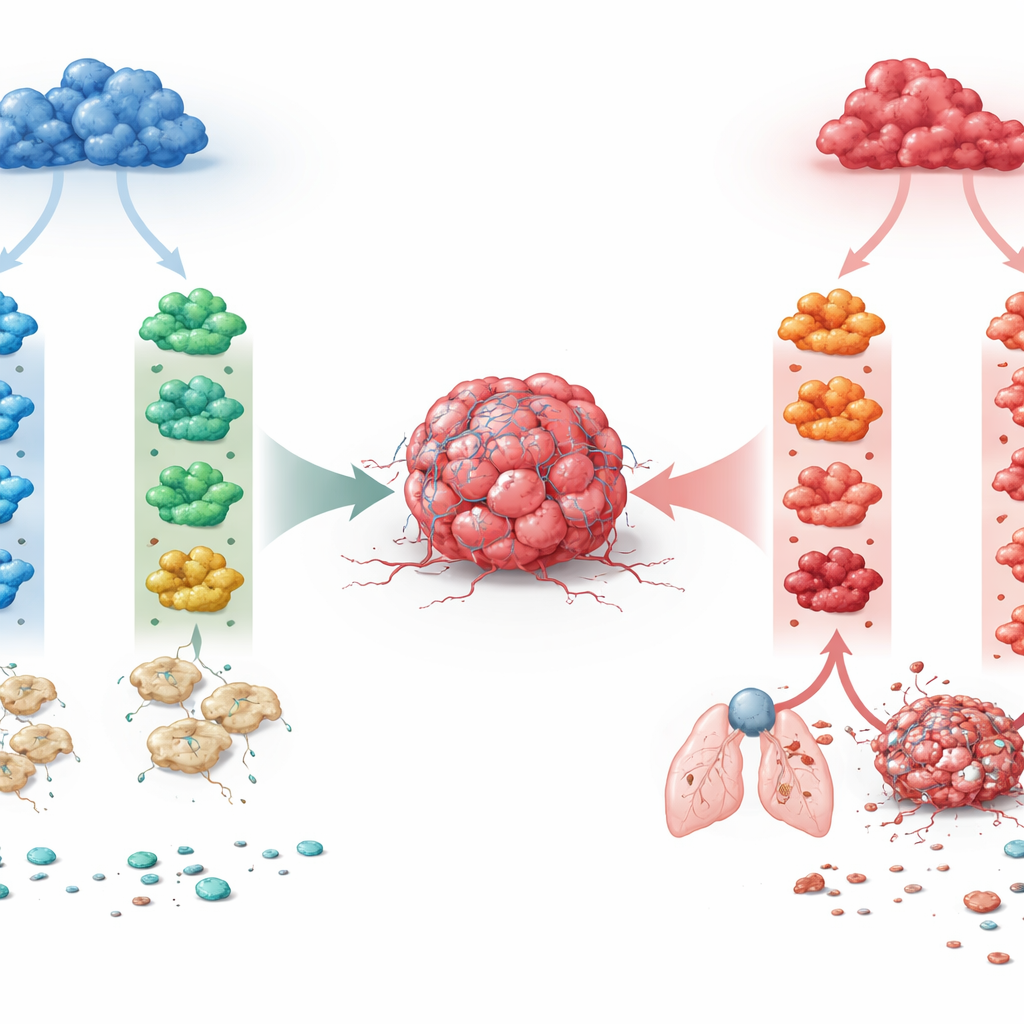
Dos familias de macrófagos, muchos destinos posibles
Los investigadores se centraron en dos linajes principales de macrófagos que existen en muchos tejidos. Un linaje depende de un factor de crecimiento llamado M-CSF y tiende a mantener el equilibrio cotidiano del tejido. El otro surge bajo un factor de crecimiento inflamatorio, GM-CSF, y es de forma natural más reactivo. A partir de médula ósea de ratón, el equipo hizo crecer macrófagos siguiendo cualquiera de los dos linajes y luego los expuso a cuatro señales inmunitarias que se encuentran con frecuencia en tumores: IFN-γ, IL-4, IL-10 y TGF-β. Esto produjo ocho estados definidos de macrófagos. Al leer la actividad génica global con secuenciación de ARN a granel y de célula única, encontraron que el origen desarrollamental fue la fuerza dominante: separó a los dos linajes con mayor intensidad que cualquier citoquina individual. Por tanto, la misma señal podía empujar a las dos familias de macrófagos hacia programas genéticos y funcionales muy distintos.
Cómo la misma señal puede cambiar de aliada a enemiga
Un hallazgo clave fue que la IL-4, una citoquina asociada desde hace tiempo con la reparación de heridas y la activación “alternativa”, tenía efectos opuestos según el origen del macrófago. Cuando la IL-4 actuaba sobre macrófagos derivados de M-CSF, activaba programas genéticos vinculados a la remodelación tisular, inducía la enzima ARG1, daba a las células una morfología alargada y reducía su capacidad de presentar antígeno a las células T. Funcionalmente, estos macrófagos favorecían el crecimiento tumoral, la invasión de la matriz circundante y la siembra de metástasis pulmonares. En contraste, la IL-4 actuando sobre macrófagos derivados de GM-CSF inducía un estado más inflamatorio, parecido a células dendríticas, con fuerte presentación de antígeno y comportamiento supresor del tumor. Así, la misma citoquina podía alimentar el cáncer o ayudar a contenerlo, según los antecedentes desarrollamentales del macrófago. Se observó una división dependiente del linaje similar, aunque menos drástica, para la IL-10, mientras que el IFN-γ siguió siendo consistentemente antitumoral y el TGF-β consistentemente promotor del tumor en ambos linajes.
Observando cómo tumores y macrófagos se moldean mutuamente
Para ver cómo estos macrófagos programados influían en las células tumorales a lo largo del tiempo, el equipo construyó esferoides tridimensionales que mezclaban células cancerosas marcadas con fluorescencia con macrófagos polarizados de distintas maneras. El análisis de célula única durante varios días reveló un patrón intrigante. Los macrófagos, independientemente de su estado inicial, convergieron gradualmente hacia un perfil común “educado por el tumor” dominado por respuestas al estrés oxidativo. En contraste, las células tumorales se diversificaron. En presencia de macrófagos control o polarizados con IFN-γ, las células cancerosas siguieron dividiéndose pero mostraron un comportamiento invasivo limitado. Cuando se co-cultivaron con macrófagos M-CSF tratados con IL-4 o TGF-β —o con macrófagos GM-CSF tratados con IL-10/TGF-β—, las células tumorales cambiaron hacia una identidad de transición epitelio-mesénquima, lista para invadir. Aunque las firmas génicas de los macrófagos fueron posteriormente remodeladas por el tumor, su programación inicial ya había dirigido a las células cancerosas hacia trayectorias muy diferentes.
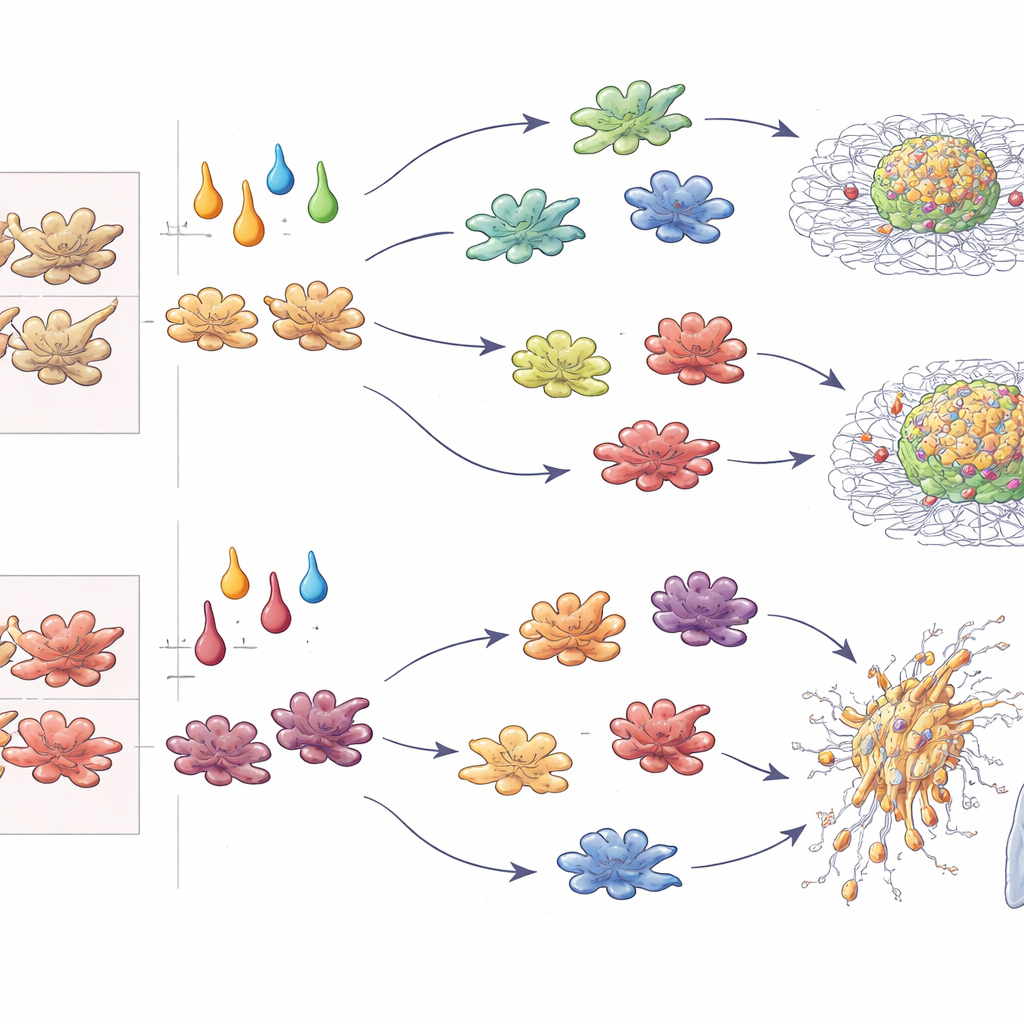
De los esferoides de laboratorio a los tumores diseminantes
Más allá de los perfiles génicos, los autores cuantificaron la velocidad de crecimiento de los esferoides tumorales y la profundidad con que invadían un gel circundante. En cultivo 3D, los macrófagos M-CSF tratados con IL-4 o TGF-β impulsaron con fuerza la expansión tumoral y la invasión radial, mientras que las células polarizadas con IFN-γ mataban o contenían los tumores. De manera llamativa, cuando las mismas citoquinas actuaron sobre macrófagos GM-CSF, la IL-4 cambió de papel y pasó a suprimir el crecimiento tumoral, mientras que la IL-10 y el TGF-β promovieron el comportamiento más agresivo. La inyección de esferoides mixtos en ratones confirmó estos patrones in vivo: los macrófagos condicionados con TGF-β promovieron metástasis pulmonares independientemente de su origen; los condicionados con IFN-γ las limitaron de forma consistente; la IL-4 aumentó o bloqueó la metástasis según si los macrófagos procedían del linaje M-CSF o GM-CSF. Al combinar crecimiento, invasión, metástasis y estimulación de células T en puntuaciones estandarizadas, los autores destilaron estos patrones en un “código ontogenia–citoquina” que predice el impacto de los macrófagos sobre los tumores.
Qué significa esto para futuras terapias contra el cáncer
Para quienes no son especialistas, el mensaje principal es que no todos los macrófagos asociados a tumores son iguales, y su comportamiento no puede resumirse con una simple etiqueta bueno versus malo o M1 frente a M2. En cambio, este trabajo muestra que las raíces desarrollamentales de un macrófago y su entorno local de citoquinas interactúan como dígitos en una cerradura combinatoria para decidir si alimentará un tumor o ayudará a destruirlo. Las terapias que ignoran este código —por ejemplo, al eliminar macrófagos de forma indiscriminada o administrar una citoquina sin tener en cuenta el linaje— pueden reducir su propia efectividad o incluso producir el efecto contrario. En el futuro, perfilar si un tumor está dominado por señalización M-CSF o GM-CSF y, a continuación, adaptar fármacos que bloqueen o suministren citoquinas según ese perfil, podría convertir a los macrófagos de aliados inciertos en socios fiables en el tratamiento del cáncer.
Cita: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
Palabras clave: macrófagos asociados a tumores, señalización por citoquinas, inmunoterapia del cáncer, microambiente tumoral, metástasis