Clear Sky Science · pt
Um código ontogenia-citocina determina a polaridade da resposta de macrófagos e os desfechos tumorais
Por que as células “grandes comedoras” do corpo importam no câncer
Células imunes chamadas macrófagos estão entre as células mais abundantes dentro de tumores sólidos. Esses “grandes comedoras” celulares podem tanto atacar o câncer quanto ajudá-lo a se espalhar, e muitos tratamentos novos visam direcioná‑los para o lado que combate o tumor. Ainda assim, os resultados em pacientes têm sido decepcionantes, em parte porque ainda nos falta um mapa claro do que torna um macrófago útil ou nocivo. Este estudo revela um “código” oculto que vincula de onde um macrófago vem, quais sinais ele recebe e como isso, em última instância, molda o crescimento tumoral e a metástase.
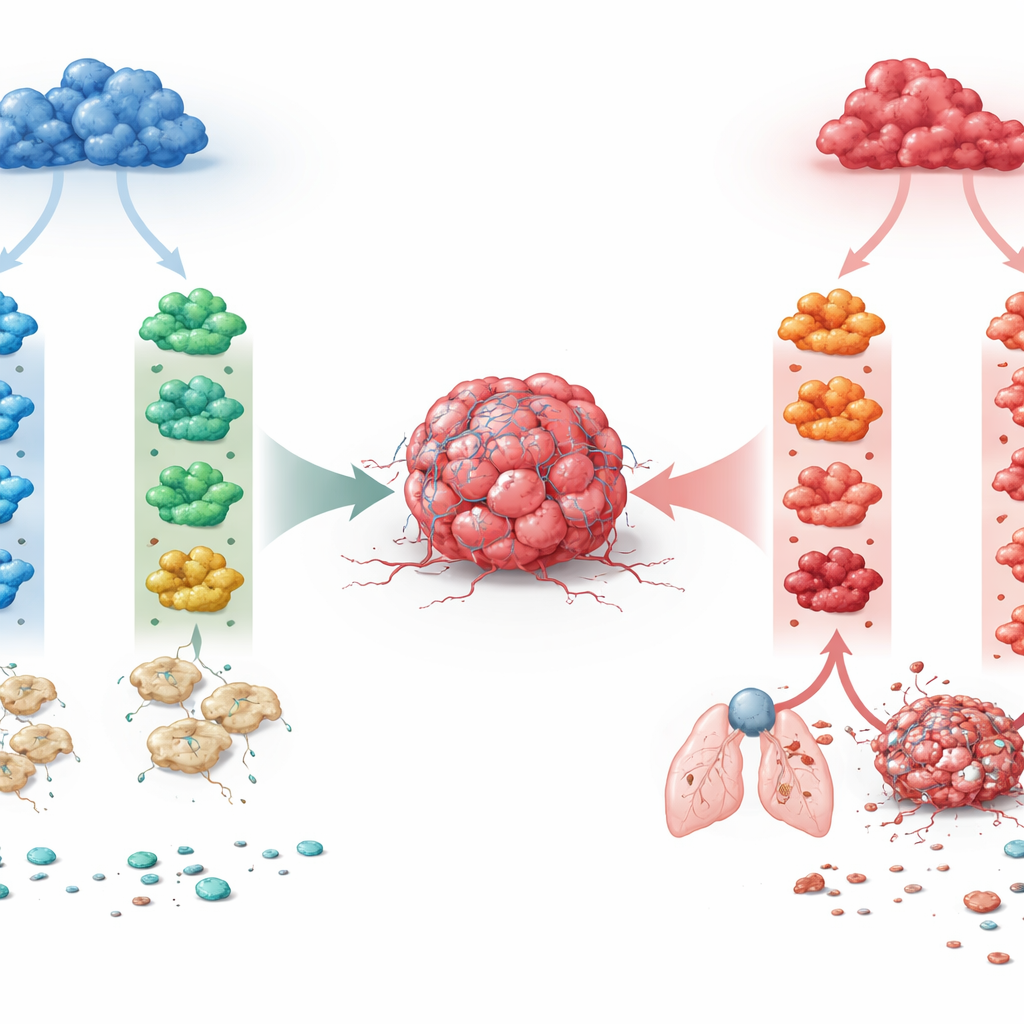
Duas famílias de macrófagos, muitos destinos possíveis
Os pesquisadores focaram em duas linhagens principais de macrófagos que existem em muitos tecidos. Uma linhagem depende de um fator de crescimento chamado M‑CSF e tende a manter o equilíbrio cotidiano dos tecidos. A outra surge sob um fator de crescimento inflamatório, GM‑CSF, e é naturalmente mais reativa. A partir da medula óssea de camundongos, a equipe cultivou macrófagos segundo cada uma das linhagens e então os expôs a quatro sinais imunes frequentemente encontrados em tumores: IFN‑γ, IL‑4, IL‑10 e TGF‑β. Isso produziu oito estados de macrófago bem definidos. Ao ler a atividade gênica global com RNA‑seq em bulk e em célula única, descobriram que a origem do desenvolvimento foi a força dominante: ela separou as duas linhagens mais fortemente do que qualquer citocina isolada. O mesmo sinal podia, portanto, empurrar as duas famílias de macrófagos para programas genéticos e funcionais muito diferentes.
Como o mesmo sinal pode mudar de amigo para inimigo
Uma descoberta-chave foi que a IL‑4, uma citocina há muito associada à reparação de feridas e à ativação “alternativa”, teve efeitos opostos dependendo da origem do macrófago. Quando a IL‑4 atuou em macrófagos derivados de M‑CSF, ela disparou programas gênicos ligados à remodelação tecidual, induziu a enzima ARG1, conferiu às células uma forma alongada e reduziu sua capacidade de apresentar antígeno para células T. Funcionalmente, esses macrófagos favoreceram o crescimento tumoral, a invasão da matriz circundante e o estabelecimento de metástases pulmonares. Em contraste, a IL‑4 agindo sobre macrófagos derivados de GM‑CSF levou a um estado mais inflamatório, similar a células dendríticas, com forte apresentação de antígenos e comportamento supressor de tumor. Assim, a mesma citocina podia tanto alimentar o câncer quanto ajudar a contê‑lo, dependendo do pano de fundo desenvolvimental do macrófago. Uma divisão dependente da linhagem, embora menos dramática, foi observada também para IL‑10, enquanto IFN‑γ permaneceu consistentemente anti‑tumoral e TGF‑β consistentemente pró‑tumoral em ambas as linhagens.
Observando tumores e macrófagos modelarem-se mutuamente
Para ver como esses macrófagos programados influenciam células tumorais ao longo do tempo, a equipe construiu esferoides tridimensionais que misturavam células cancerígenas marcadas por fluorescência com macrófagos polarizados de modo diferente. A análise em célula única ao longo de vários dias revelou um padrão intrigante. Macrófagos, independentemente de seu estado inicial, convergiram gradualmente para um perfil comum “educado pelo tumor” dominado por respostas ao estresse oxidativo. Em contraste, as células tumorais se diversificaram. Na presença de macrófagos controle ou polarizados por IFN‑γ, as células cancerígenas continuaram a se dividir, mas exibiram comportamento invasivo limitado. Quando co‑cultivadas com macrófagos M‑CSF tratados com IL‑4 ou TGF‑β — ou com macrófagos GM‑CSF tratados com IL‑10/TGF‑β — as células tumorais deslocaram‑se para uma identidade epitélio‑a‑mesenquimal, pronta para invasão. Mesmo que as assinaturas gênicas dos macrófagos tenham sido posteriormente remodeladas pelo tumor, seu programa inicial já havia direcionado as células cancerígenas por trajetórias muito distintas.
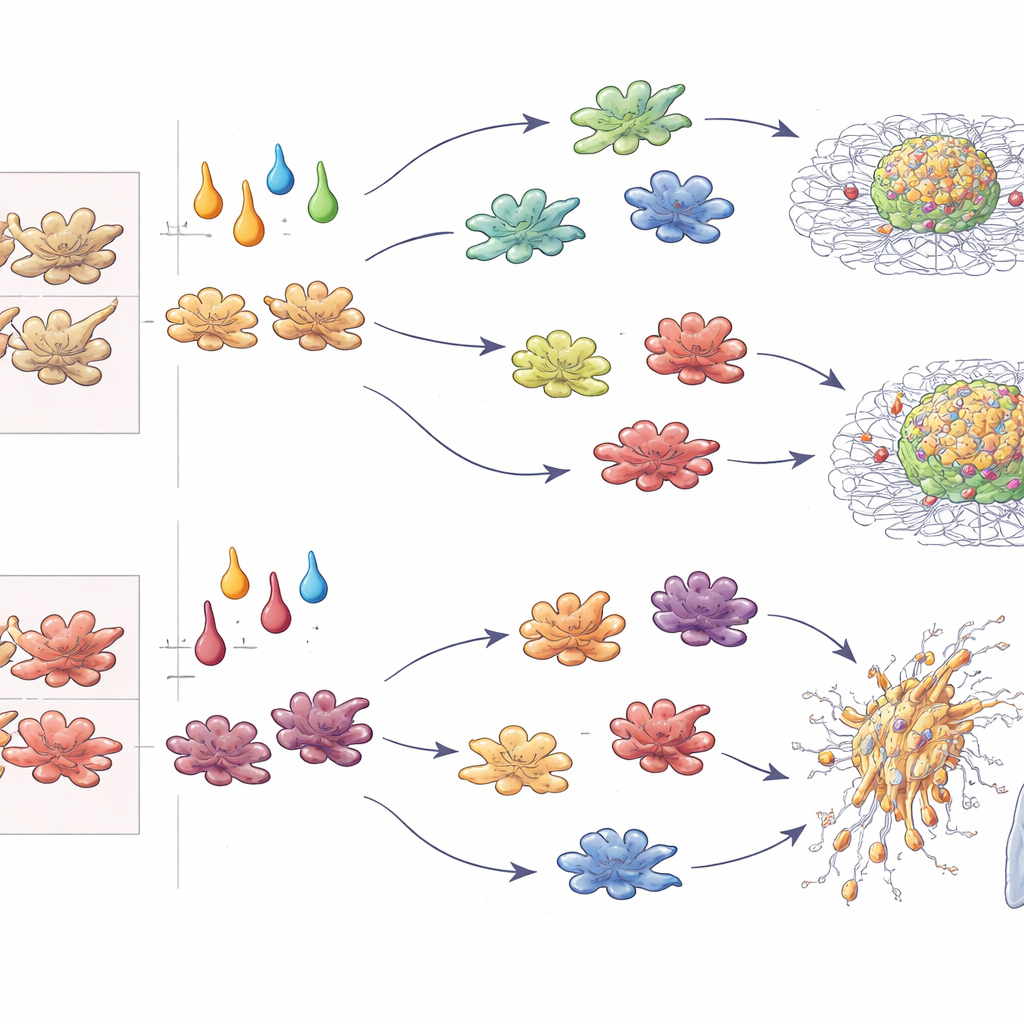
Dos esferoides de laboratório a tumores em expansão
Além das leituras gênicas, os autores quantificaram a velocidade de crescimento dos esferoides tumorais e a profundidade de invasão em um gel circundante. Em cultura 3D, macrófagos M‑CSF tratados com IL‑4 ou TGF‑β impulsionaram fortemente a expansão tumoral e a invasão radial, enquanto células polarizadas por IFN‑γ mataram ou restringiram os tumores. Notavelmente, quando as mesmas citocinas atuaram sobre macrófagos GM‑CSF, a IL‑4 trocou de papel e passou a suprimir o crescimento tumoral, ao passo que IL‑10 e TGF‑β dirigiram o comportamento mais agressivo. A injeção de esferoides mistos em camundongos confirmou esses padrões in vivo: macrófagos condicionados por TGF‑β promoveram metástases pulmonares independentemente da origem; os condicionados por IFN‑γ consistentemente as limitaram; a IL‑4 ou aumentou ou bloqueou a metástase dependendo se os macrófagos provinham da linhagem M‑CSF ou GM‑CSF. Ao combinar crescimento, invasão, metástase e estimulação de células T em pontuações padronizadas, os autores destilaram esses padrões em um “código ontogenia–citocina” que prediz o impacto do macrófago nos tumores.
O que isso significa para terapias futuras contra o câncer
Para não especialistas, a mensagem principal é que nem todos os macrófagos associados a tumores são iguais, e seu comportamento não pode ser capturado por um rótulo simples de bom‑versus‑mal ou M1‑versus‑M2. Em vez disso, este trabalho mostra que as raízes desenvolvimentais de um macrófago e seu ambiente local de citocinas interagem como dígitos em uma fechadura de combinação para decidir se ele vai nutrir um tumor ou ajudar a destruí‑lo. Terapias que ignoram esse código — por exemplo, ao esgotar macrófagos de forma ampla ou ao administrar uma citocina sem considerar a linhagem — podem reduzir sua própria eficácia ou até ter efeito contrário. No futuro, perfilar se um tumor é dominado por sinalização M‑CSF ou GM‑CSF, e então ajustar drogas que bloqueiem ou forneçam citocinas de acordo, pode transformar macrófagos de aliados incertos em parceiros confiáveis no tratamento do câncer.
Citação: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
Palavras-chave: macrófagos associados ao tumor, sinalização por citocinas, imunoterapia do câncer, microambiente tumoral, metástase