Clear Sky Science · tr
Bir ontogeni-sitokin kodu makrofaj yanıtının kutupluluğunu ve tümör sonuçlarını belirler
Neden Vücudun “Büyük Yiyici” Hücreleri Kanserde Önemli?
Makrofaj olarak adlandırılan bağışıklık hücreleri, katı tümörlerin içinde en bol bulunan hücrelerden biridir. Bu hücresel “büyük yiyiciler” ya kanserle savaşabilir ya da onun yayılmasına yardım edebilir; bu nedenle birçok yeni tedavi onları kanserle savaşan yöne itmeye çalışır. Ancak hastalardaki sonuçlar hayal kırıklığı yaratmıştır; bunun bir nedeni de makrofajı yardımcı veya zararlı yapan etkenlerin hâlâ net bir haritasının olmamasıdır. Bu çalışma, bir makrofajın nereden geldiğini, hangi sinyalleri gördüğünü ve nihayetinde tümör büyümesi ile metastazı nasıl şekillendirdiğini birbirine bağlayan gizli bir “kod”u ortaya koyuyor.
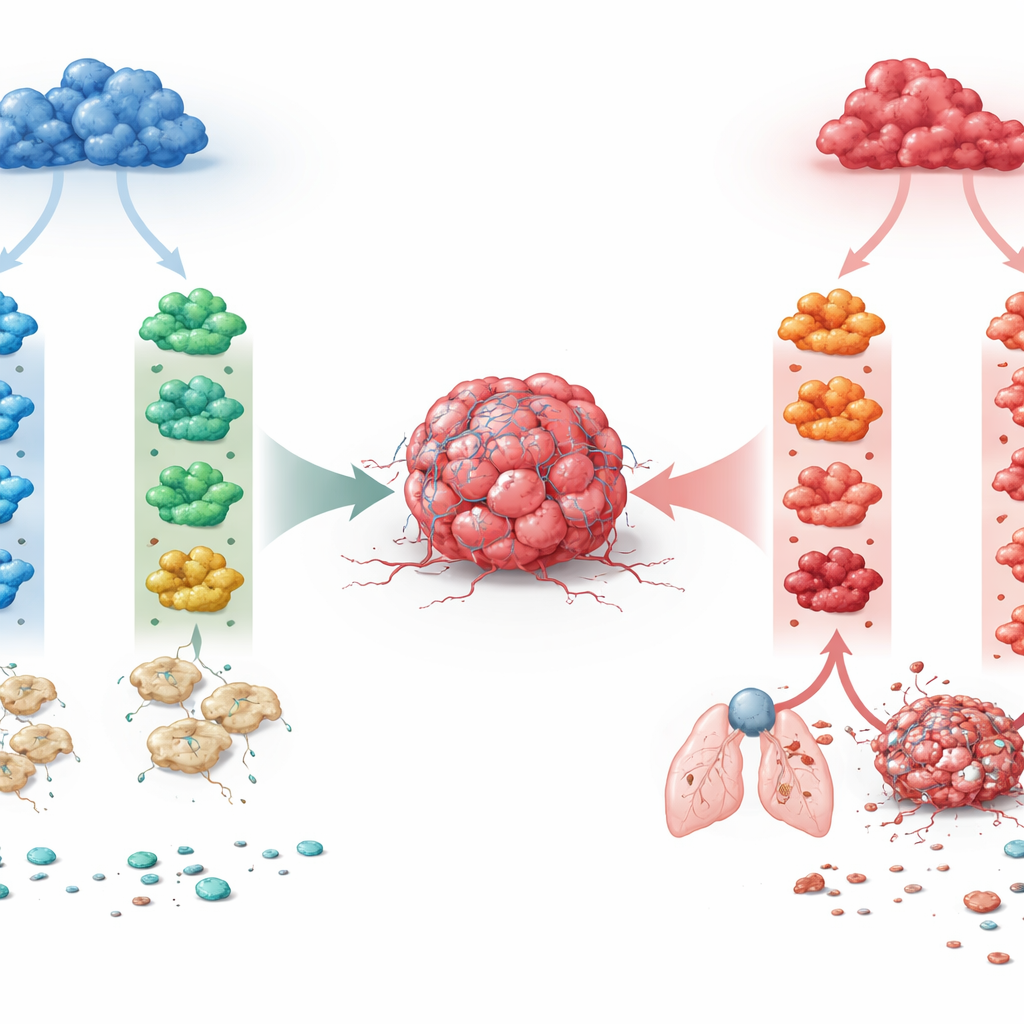
İki Makrofaj Ailesi, Birçok Olası Kader
Araştırmacılar birçok dokuda bulunan iki ana makrofaj soyu üzerine odaklandılar. Bir soy M-CSF adlı bir büyüme faktörüne bağlıdır ve genellikle günlük doku dengesini sürdürme eğilimindedir. Diğer soy ise enflamatuvar bir büyüme faktörü olan GM-CSF altında ortaya çıkar ve doğal olarak daha tepkiseldir. Fare kemik iliğinden ekip, makrofajları bu iki soya göre büyüttü, ardından onları tümörlerde sıkça bulunan dört bağışıklık sinyaline maruz bıraktı: IFN-γ, IL-4, IL-10 ve TGF-β. Bu, sekiz iyi tanımlanmış makrofaj durumunu verdi. Toplu ve tek hücreli RNA dizilemesi ile küresel gen etkinliğini okuyarak, gelişimsel kökenin baskın güç olduğunu buldular: tek bir sitokinden daha güçlü biçimde bu iki soyu birbirinden ayırıyordu. Aynı sinyal bu nedenle iki makrofaj ailesini çok farklı genetik ve fonksiyonel programlara itebiliyordu.
Aynı Sinyalin Nasıl Dosttan Düşmana Dönüştüğü
Önemli bir keşif, yara onarımı ve “alternatif” aktivasyonla uzun süredir ilişkilendirilen IL-4’ün, makrofaj kökenine bağlı olarak zıt etkiler gösterdiğiydi. IL-4, M-CSF kaynaklı makrofajlar üzerinde etkili olduğunda doku yeniden düzenlemesi ile ilişkili gen programlarını tetikledi, ARG1 enzimini indükledi, hücrelere uzamış bir şekil verdi ve T hücrelerine antijen sunma yeteneğini azalttı. Fonksiyonel olarak bu makrofajlar tümör büyümesini, çevreleyen matrikse invazyonu ve akciğer metastazlarının tohumlanmasını destekledi. Buna karşılık IL-4, GM-CSF kökenli makrofajlarda daha enflamatuvar, dendritik hücreye benzeyen bir durum yaratarak güçlü antijen sunumu ve tümörü baskılayıcı davranış tetikledi. Böylece aynı sitokin makrofajın gelişimsel geçmişine bağlı olarak ya kanseri besleyebiliyor ya da onu sınırlamaya yardımcı olabiliyordu. Benzer, ancak daha az dramatik bir soy-bağımlı ayrım IL-10 için gözlenirken, IFN-γ her iki soya karşı tutarlı biçimde tümörle savaşan; TGF-β ise her iki soyda da tutarlı olarak tümörü destekleyen etkiler gösterdi.
Tümörlerin ve Makrofajların Birbirini Nasıl Şekillendirdiğini İzlemek
Bu programlanmış makrofajların zaman içinde tümör hücrelerini nasıl etkilediğini görmek için ekip, floresanla etiketlenmiş kanser hücrelerini farklı kutuplaşmış makrofajlarla karıştıran üç boyutlu sferoidler oluşturdu. Birkaç gün süren tek hücre analizleri ilginç bir desen ortaya koydu. Başlangıç durumundan bağımsız olarak makrofajlar giderek oksidatif stres yanıtlarının egemen olduğu ortak bir “tümör-eğitilmiş” profile yakınsadılar. Buna karşılık tümör hücreleri çeşitlendi. Kontrol veya IFN-γ ile kutuplaşmış makrofajların varlığında kanser hücreleri bölünmeye devam etti ama sınırlı invaziv davranış gösterdi. IL-4 veya TGF-β ile muamele edilmiş M-CSF makrofajlarıyla—ya da IL-10/TGF-β ile muamele edilmiş GM-CSF makrofajlarıyla—ortak kültürde tümör hücreleri epitelden mezenkime dönüşüm, invazyona hazır bir kimliğe kaydı. Makrofajların gen imzaları daha sonra tümör tarafından yeniden şekillendirilse de, onların ilk programlaması kanser hücrelerini çok farklı yörüngelere yönlendirmişti.
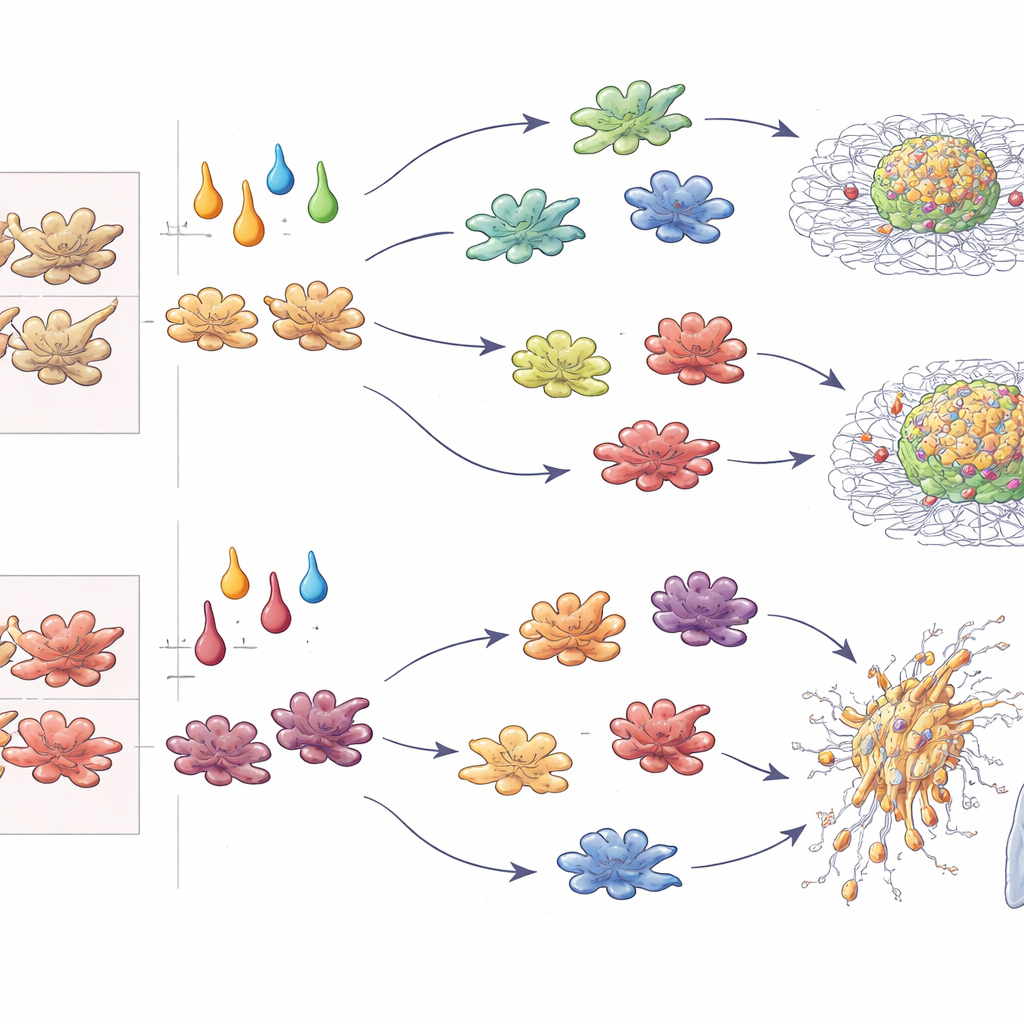
Laboratuvar Sferoidlerinden Yayılan Tümörlere
Gen okumalarının ötesinde, yazarlar tümör sferoidlerinin ne kadar hızlı büyüdüğünü ve etraflarındaki jelde ne kadar derine invaze ettiğini nicelendirildi. 3B kültürde IL-4 veya TGF-β ile muamele edilmiş M-CSF makrofajları tümör genişlemesini ve radyal invazyonu güçlü biçimde artırırken, IFN-γ ile kutuplaşmış hücreler tümörleri öldürdü veya sınırladı. Çarpıcı şekilde, aynı sitokinler GM-CSF makrofajları üzerinde etkili olduğunda IL-4 rol değiştirip artık tümör büyümesini baskılarken, IL-10 ve TGF-β en agresif davranışı tetikledi. Karışık sferoidleri farelere enjekte etmek in vivo bu desenleri doğruladı: TGF-β koşullandırılmış makrofajlar kökene bakılmaksızın akciğer metastazlarını destekledi; IFN-γ koşullandırılmış olanlar ise tutarlı biçimde bunları sınırladı; IL-4 ise makrofajların M-CSF mi yoksa GM-CSF mi kökenli olduğuna bağlı olarak metastazı ya artırdı ya da engelledi. Büyüme, invazyon, metastaz ve T hücresi uyarımını standart puanlara birleştirerek yazarlar bu desenleri makrofaj etkisini tahmin eden bir “ontogeni–sitokin kodu”na indirgediler.
Gelecekteki Kanser Tedavileri İçin Anlamı Ne?
Uzman olmayanlar için ana mesaj, tümöre bağlı makrofajların hepsinin eşit yaratılmadığı ve davranışlarının basit bir iyi-ya-da-kötü ya da M1-ya-da-M2 etiketiyle yakalanamayacağıdır. Bunun yerine bu çalışma, bir makrofajın gelişimsel kökleri ile yerel sitokin ortamının, onu tümörü besleyecek mi yoksa yok etmeye yardım edecek mi kararını belirleyen bir kombinasyon kilidindeki rakamlar gibi etkileştiğini gösteriyor. Bu kodu görmezden gelen terapiler—örneğin makrofajları geniş çapta yok etmek veya soy dikkate alınmadan bir sitokin vermek—kendi etkinliklerini zayıflatabilir hatta ters sonuç verebilir. Gelecekte, bir tümörün M-CSF mi yoksa GM-CSF sinyallemesiyle mi domine edildiğini profilleyip buna göre sitokin engelleyici ya da sitokin verici ilaçları uyarlamak, makrofajları belirsiz müttefiklerden kanser tedavisinde güvenilir ortaklara dönüştürebilir.
Atıf: Schaer, D.J., Schulthess-Lutz, N., Peterhans, M.J. et al. An ontogeny-cytokine code determines macrophage response polarity and tumor outcomes. Commun Biol 9, 592 (2026). https://doi.org/10.1038/s42003-026-09853-y
Anahtar kelimeler: tümöre bağlı makrofajlar, sitokin sinyallemesi, kanser immünoterapisi, tümör mikroyapısı, metastaz