Clear Sky Science · zh
细胞内补体因子H通过调节细胞周期和肌动蛋白细胞骨架促进肿瘤进展
为什么这个隐秘的癌症助力者很重要
癌症常被描述为生长中的肿瘤与免疫系统之间的斗争。本研究揭示了免疫系统自身的一种分子——称为因子H的蛋白——可以悄然“倒戈”。因子H不仅在血液中负责控制炎症,在肿瘤细胞及其邻近的支持细胞中也被发现,并在这些部位帮助癌症生长、存活并可能扩散。理解这种出乎意料的“双重身份”为预测肿瘤侵袭性和设计更智能的治疗策略提供了新路径。
熟悉的蛋白出现在意想不到的地方
因子H最为人所知的是作为补体系统的守护者——补体是固有免疫的一部分,帮助清除血液中的微生物和受损细胞。肿瘤周围高水平的因子H已被发现在包括透明细胞肾癌在内的多种癌症中与较差预后相关。然而,因子H在血液中的传统作用并不能完全解释为何肿瘤过度表达因子H的患者预后通常较差。作者通过结合患者数据、单细胞测序和细胞生物学证据表明,肾脏肿瘤内的许多细胞——尤其是与癌症相关的成纤维细胞和恶性肾细胞——会主动合成自身的因子H,并将其中一部分保留在细胞内而非全部分泌出去。
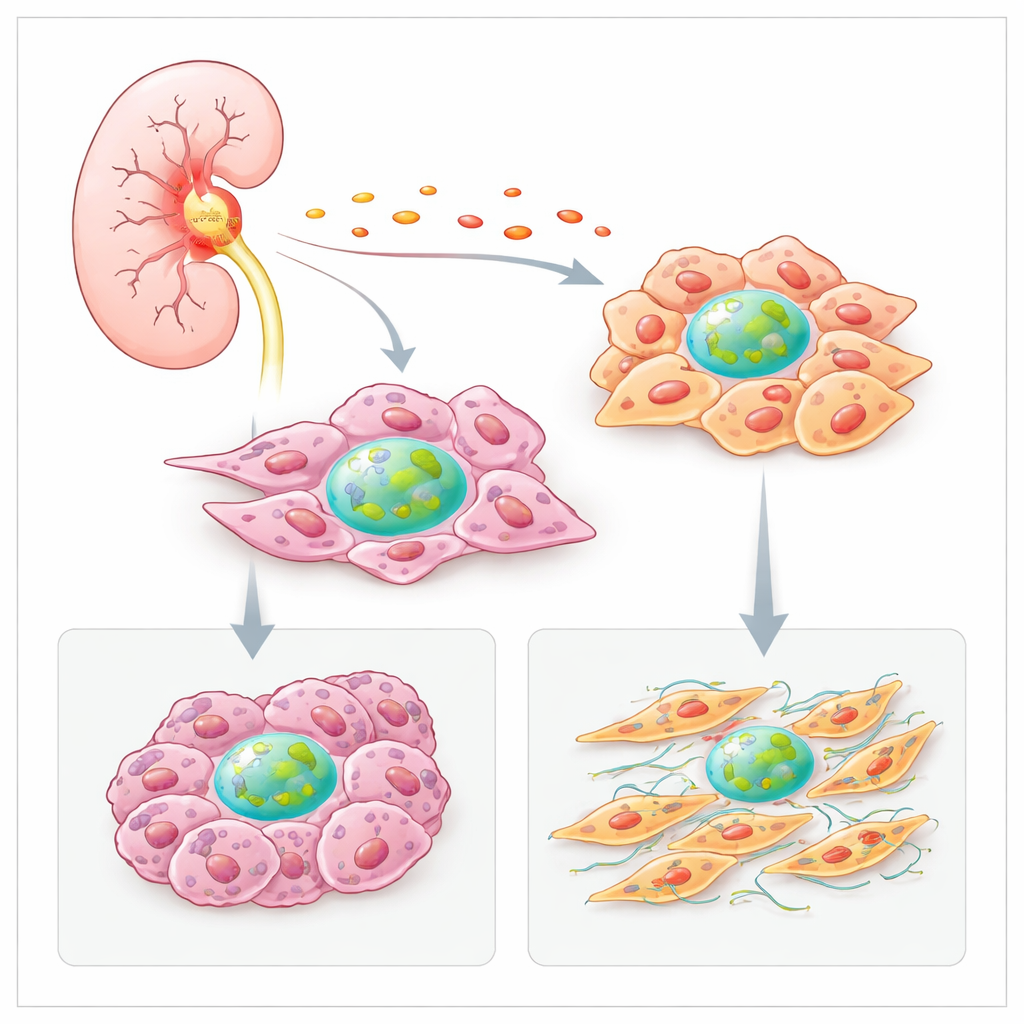
炎症使因子H的产生上调
研究团队首先探究为何肿瘤较健康肾组织产生更多因子H。他们分析了大型癌症数据集和肿瘤切片的空间图谱,发现富含成纤维细胞和癌细胞的区域也含有高表达的因子H基因。这些高表达区常与炎性分子(如细胞因子IL‑6)的特征重叠。在培养的肾癌细胞中,IL‑6强烈促进因子H的产生,而其他炎性信号则在成纤维细胞中上调其表达。这表明,炎症的肿瘤微环境本身促使局部细胞提高自身因子H的产量,从而强化了一个有利于生长与存活的恶性循环。
进入细胞核,帮助细胞忽视停止信号
在细胞内观察时,研究者发现一种较小的、存在于细胞内的因子H形式出现在多个细胞区室,包括细胞核。在那里,它与细胞周期的关键调控者发生物理相互作用,特别是驱动细胞从静止进入分裂状态的转录因子E2F3。当沉默因子H基因时,成纤维细胞与癌细胞的复制速度变慢、在静止期积累,并显示出更活跃的p53——一种能停止生长或触发细胞死亡的“守护者”蛋白。重要的是,仅仅从外部补充正常分泌的因子H不能逆转这种效应,这强调了细胞内储存的因子H是保持p53受抑并允许持续增殖的关键。
重塑细胞骨架以利于生长与运动
在肾癌细胞中(但在成纤维细胞中则不然),细胞内因子H还与肌动蛋白封顶复合体的组分结合,该复合体调节肌动蛋白纤维的生长并稳定细胞的内部支架。当沉默因子H时,癌细胞变得更圆,失去有序的应力纤维,并难以形成紧密的三维球状体——这在实验中常用作肿瘤生长与凝聚力的替代模型。同时沉默因子H和封顶蛋白并未加重缺陷,提示二者在同一信号通路中发挥作用。即便在阻断p53的情况下,这些结构性改变仍然发生,表明因子H独立地支持细胞分裂和有利于侵袭及转移的结构重塑两者。
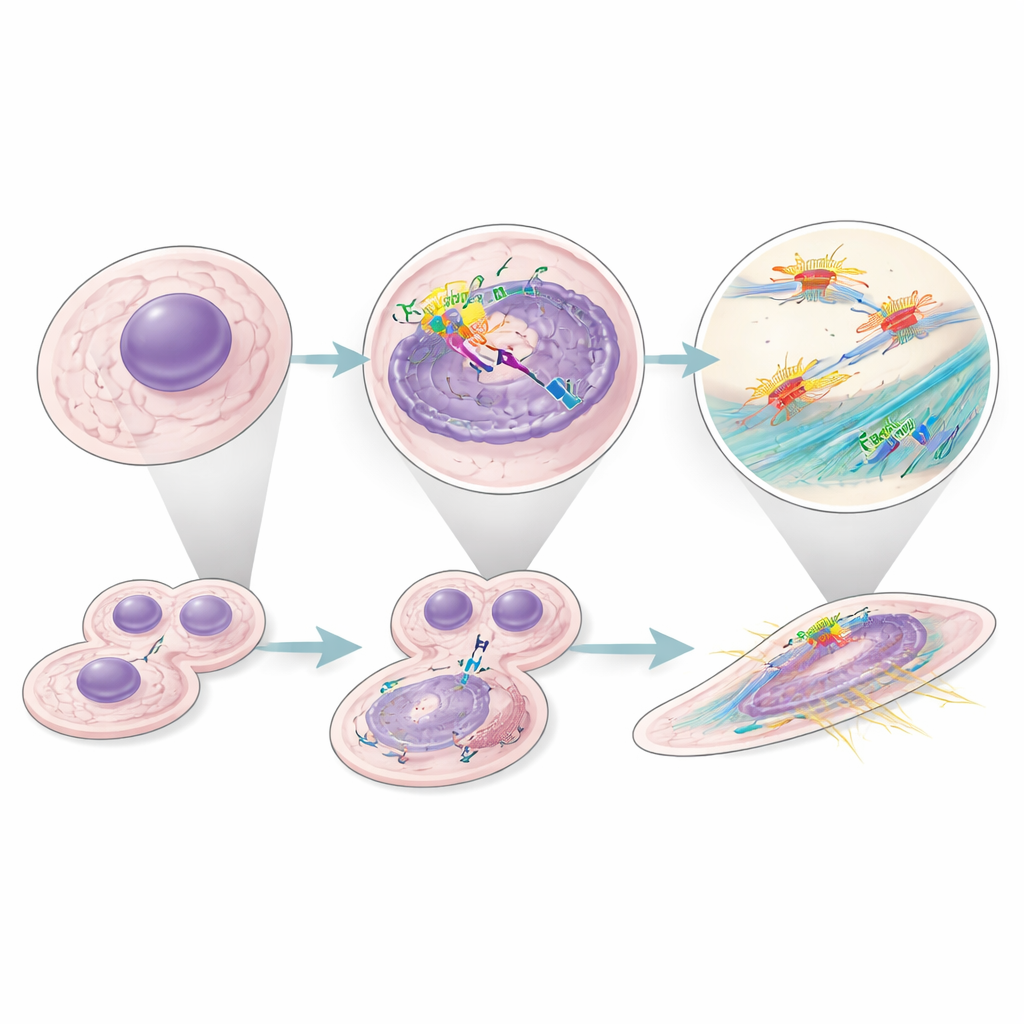
在多种癌症中具有更广泛的影响
为了解这种行为是否只限于肾脏肿瘤,作者挖掘了大量来自人类癌症的单细胞和整体RNA数据集。在因子H高表达预示不良生存期的肿瘤中,成纤维细胞特征也与更差的预后相关。在肾脏肿瘤内,他们鉴定出一种特定的恶性细胞状态,该状态强烈表达因子H,具有活跃的细胞周期程序,并与患者较短的生存期相关。总体而言,这些发现表明,细胞内因子H作为一种广泛的促肿瘤因子,在多种癌症类型中于癌细胞及其支持性成纤维细胞内发挥作用。
这对患者和治疗意味着什么
这项工作推翻了因子H仅仅是循环中免疫反应调节者的观念。相反,它作为一种多任务的细胞内助力者出现,通过帮助细胞通过分裂周期并微调其内部支架以便移动,鼓励肿瘤生长。这有助于解释为何因子H的过表达在癌症中是如此强烈的不良预警信号。它也意味着仅设计用于阻断肿瘤表面或血液中因子H的药物可能无法完全解除其隐蔽的细胞内功能。未来的治疗可能需要同时针对其外部和内部作用,才能有效减缓肿瘤进展。
引用: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
关键词: 补体因子H, 透明细胞肾细胞癌, 与癌症相关的成纤维细胞, 肿瘤微环境, 细胞周期调控