Clear Sky Science · sv
Intracellulärt komplementfaktor H främjar tumörprogression genom modulering av cellcykel och aktincytoskelett
Varför denna dolda cancersamarbetspartner är viktig
Cancer beskrivs ofta som en kamp mellan växande tumörer och immunsystemet. Denna studie visar att ett av immunsystemets egna molekyler, ett protein kallat faktor H, tyst kan byta sida. Istället för att bara arbeta i blodomloppet för att kontrollera inflammation återfinns faktor H inne i tumörceller och i närliggande stödjande celler, där det hjälper cancer att växa, överleva och potentiellt sprida sig. Att förstå detta oväntade ”dubbelliv” öppnar nya möjligheter att förutsäga hur aggressiv en tumör kommer att vara och att utveckla smartare behandlingar.
Ett välbekant protein på en oväntad plats
Faktor H är mest känt som en väktare av komplementsystemet, en del av den medfödda immuniteten som hjälper till att rensa mikrober och skadade celler från blodet. Höga nivåer av faktor H runt tumörer hade redan kopplats till sämre utfall i flera cancerformer, inklusive klarcellig njurcancer. Men dess vanliga, blodburna roll kunde inte fullt ut förklara varför patienter vars tumörer överproducerar faktor H tenderar att ha sämre prognos. Genom att kombinera patientdata, enkelcellssekvensering och cellbiologi visar författarna att många celler inne i njurtumörer—särskilt cancerassocierade fibroblaster och maligna njurceller—aktivt tillverkar sin egen faktor H och behåller en del av den inne i cellen istället för att sekretera den.
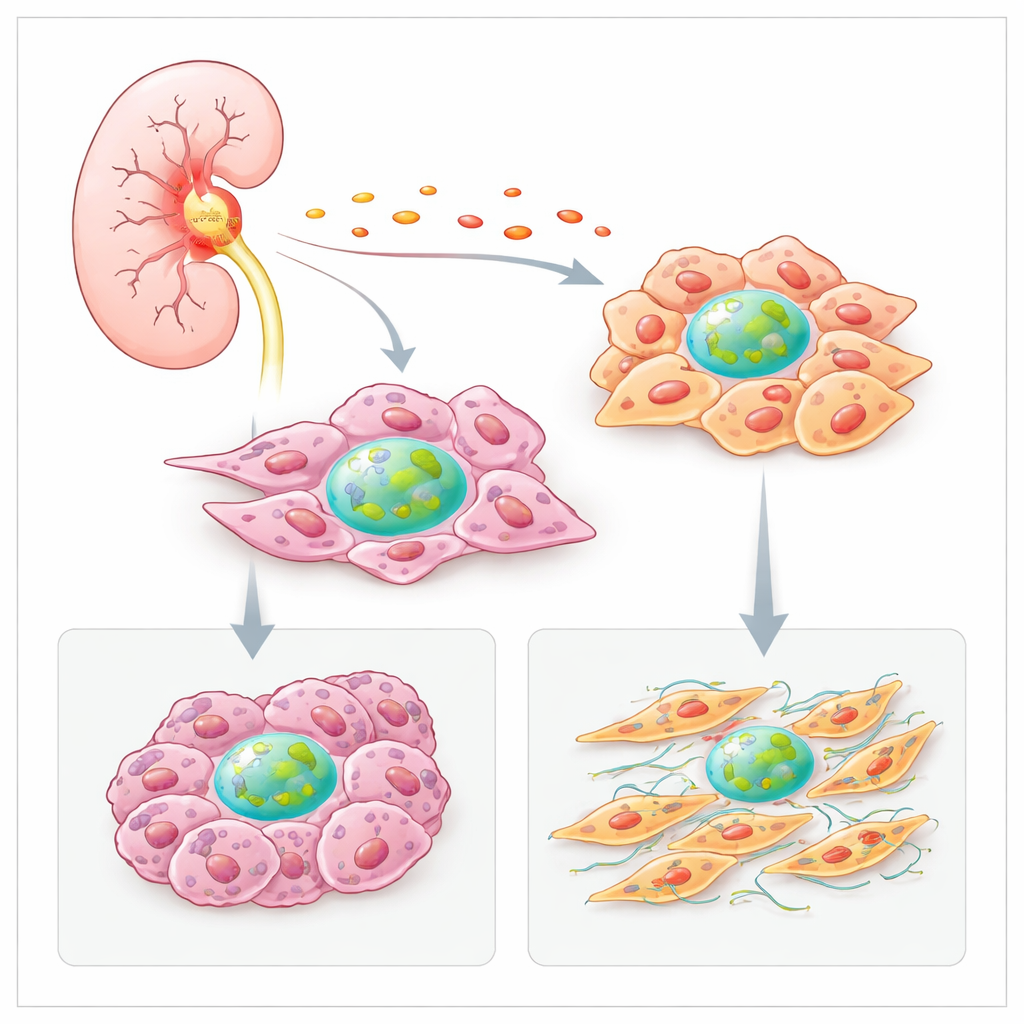
Inflammation ökar produktionen av faktor H
Forskarna frågade först varför tumörer producerar mer faktor H än frisk njurvävnad. De analyserade stora cancer-dataset och spatiala kartor av tumorsnitt och fann att områden rika på fibroblaster och cancerceller också innehöll höga nivåer av genen för faktor H. Dessa heta områden överlappade ofta med signaturer av inflammatoriska molekyler, såsom cytokinen IL‑6. I odlade njurcancerceller ökade IL‑6 kraftigt produktionen av faktor H, medan andra inflammatoriska signaler ökade den i fibroblaster. Det tyder på att den inflammerade tumörmiljön själv driver lokala celler att skruva upp sin egen faktor H, vilket förstärker en ond cirkel av tillväxt och överlevnad.
Inne i kärnan, hjälper celler att ignorera stopp‑signaler
När de tittade in i cellerna upptäckte forskarna en mindre, intracellulär form av faktor H som förekommer i flera kompartment, inklusive kärnan. Där interagerar den fysiskt med nyckelregulatorer av cellcykeln, särskilt en transkriptionsfaktor kallad E2F3 som hjälper celler att gå från vila till delning. När genen för faktor H tystades uppvisade fibroblaster och cancerceller långsammare replikation, samlades i vilofasen och visade mer aktivt p53, ett välkänt ”väktarprotein” som kan stoppa tillväxt eller utlösa celldöd. Viktigt är att enkel tillförsel av normal, sekreterad faktor H utifrån inte räddade denna effekt, vilket understryker att den interna poolen är det som håller p53 i schack och tillåter fortsatt proliferation.
Omarbetning av cellens skelett för tillväxt och rörelse
I njurcancerceller, men inte i fibroblaster, band intracellulärt faktor H också komponenter i aktin‑cappingkomplexet, som reglerar hur aktinfilament växer och stabiliserar cellens interna stomme. När faktor H tystades blev cancerceller rundare, förlorade sina organiserade stressfibrer och hade svårt att bilda kompakta tredimensionella sfäroider—en experimentell modell för tumörtillväxt och sammanhållning. Att samtidigt tysta både faktor H och cappingproteinet förvärrade inte defekterna, vilket tyder på att de verkar i samma väg. Dessa förändringar uppstod även när p53 blockerades, vilket visar att faktor H oberoende stöder både celldelning och de strukturella förändringar som kan gynna invasion och metastasering.
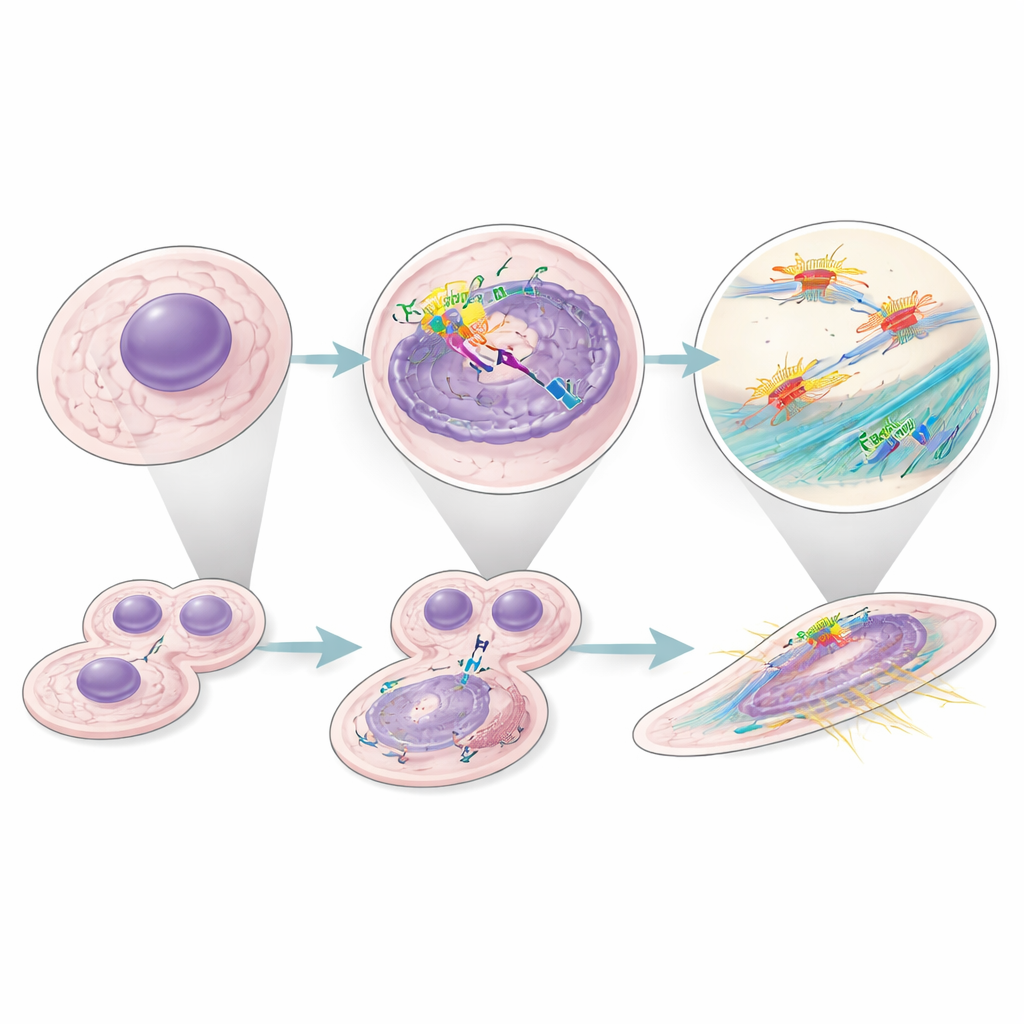
En bredare påverkan över många cancerformer
För att se om detta beteende var unikt för njurtumörer grävde författarna i många enkelcells- och bulk‑RNA‑dataset från mänskliga cancerformer. I tumörer där hög faktor H‑expression förutsade sämre överlevnad var fibroblastsignaturer också kopplade till sämre utfall. Inom njurtumörer identifierade de ett specifikt malignt celltillstånd som starkt uttryckte faktor H, visade aktiva cellcykelprogram och var associerat med kortare patientöverlevnad. Tillsammans tyder dessa fynd på att intracellulärt faktor H fungerar som en bredt pro‑tumör agent, verksam inne i både cancerceller och deras stödjande fibroblaster i flera cancerformer.
Vad detta betyder för patienter och behandlingar
Detta arbete kullkastar idén att faktor H bara är en cirkulerande regulator av immunsvar. I stället framträder det som en multitaskande, intracellulär hjälpare som uppmuntrar tumörer att växa genom att underlätta cellernas passage genom delningscykeln och finjustera deras interna stomme för rörelse. Det hjälper till att förklara varför överuttryck av faktor H är en så tydlig varningssignal vid cancer. Det innebär också att läkemedel utformade för att blockera faktor H på tumörytan eller i blodet kanske inte helt oskadliggör dess dolda, interna funktioner. Framtida terapier kommer sannolikt behöva rikta in sig på både dess externa och interna roller för att effektivt bromsa tumörprogression.
Citering: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Nyckelord: komplementfaktor H, klarcellig njurcancer, cancerassocierade fibroblaster, tumörmikromiljö, reglering av cellcykeln