Clear Sky Science · fr
Le facteur H du complément intracellulaire favorise la progression tumorale en modulant le cycle cellulaire et le cytosquelette d'actine
Pourquoi cet auxiliaire caché du cancer importe
Le cancer est souvent décrit comme un affrontement entre des tumeurs en croissance et le système immunitaire. Cette étude montre que l’un des propres composants du système immunitaire, une protéine appelée facteur H, peut discrètement changer de camp. Au lieu de n’agir que dans le sang pour contrôler l’inflammation, le facteur H se trouve à l’intérieur des cellules tumorales et des cellules de soutien voisines, où il aide les cancers à croître, à survivre et potentiellement à se disséminer. Comprendre cette « double vie » inattendue ouvre de nouvelles pistes pour prévoir l’agressivité d’une tumeur et concevoir des thérapies plus efficaces.
Une protéine familière à un endroit inattendu
Le facteur H est surtout connu comme un protecteur du système du complément, une composante de l’immunité innée qui participe à l’élimination des microbes et des cellules endommagées dans le sang. Des niveaux élevés de facteur H autour des tumeurs avaient déjà été associés à un mauvais pronostic dans plusieurs cancers, y compris le cancer rénal à cellules claires. Pourtant, son rôle habituel, circulant dans le sang, n’expliquait pas entièrement pourquoi les patients dont les tumeurs produisent trop de facteur H ont tendance à évoluer défavorablement. En combinant données de patients, séquençage unicellulaire et biologie cellulaire, les auteurs montrent que de nombreuses cellules à l’intérieur des tumeurs rénales — en particulier les fibroblastes associés au cancer et les cellules rénales malignes — synthétisent activement leur propre facteur H et conservent une partie de celui‑ci à l’intérieur de la cellule plutôt que de le sécréter.
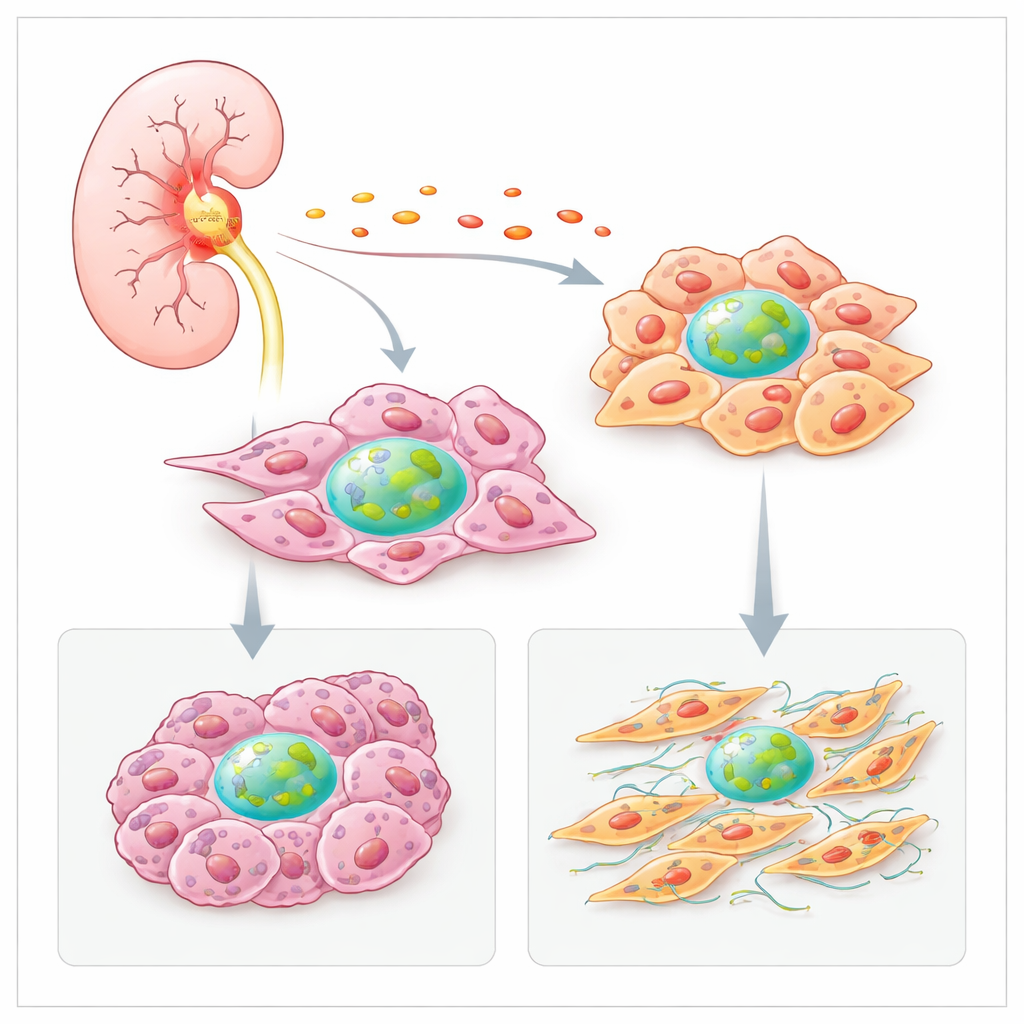
L’inflammation augmente la production de facteur H
L’équipe a d’abord cherché pourquoi les tumeurs produisent plus de facteur H que le tissu rénal sain. Ils ont analysé de larges jeux de données sur le cancer et des cartes spatiales de coupes tumorales et ont constaté que les zones riches en fibroblastes et en cellules cancéreuses contenaient aussi des niveaux élevés du gène du facteur H. Ces zones chaudes recoupaient souvent des signatures de molécules inflammatoires, comme la cytokine IL‑6. En culture de cellules rénales cancéreuses, l’IL‑6 a fortement stimulé la production de facteur H, tandis que d’autres signaux inflammatoires l’ont augmenté dans les fibroblastes. Ces observations suggèrent que l’environnement tumoral inflammatoire pousse les cellules locales à accroître leur propre production de facteur H, renforçant ainsi un cercle vicieux de croissance et de survie.
Dans le noyau, aider les cellules à ignorer les signaux d’arrêt
En observant l’intérieur des cellules, les chercheurs ont découvert une forme plus petite de facteur H intracellulaire qui apparaît dans plusieurs compartiments, y compris le noyau. Là, elle interagit physiquement avec des régulateurs clés du cycle cellulaire, en particulier un facteur de transcription appelé E2F3 qui aide à faire passer les cellules de l’état de repos à l’état de division. Lorsque le gène du facteur H a été réprimé, les fibroblastes et les cellules cancéreuses ralentissaient leur réplication, s’accumulaient en phase de repos et présentaient une activation accrue de p53, une protéine « gardienne » bien connue qui peut arrêter la croissance ou déclencher la mort cellulaire. Il est important de noter que l’ajout externe de facteur H sécrété n’a pas corrigé cet effet, ce qui souligne que la réserve intracellulaire est ce qui maintient p53 sous contrôle et permet une prolifération continue.
Remodeler le squelette cellulaire pour la croissance et le mouvement
Dans les cellules du cancer rénal, mais pas dans les fibroblastes, le facteur H intracellulaire se liaisait également à des composants du complexe de capping de l’actine, qui régule la croissance des filaments d’actine et stabilise l’ossature interne de la cellule. Lorsque le facteur H était réprimé, les cellules cancéreuses devenaient plus rondes, perdaient leurs fibres de tension organisées et peinaient à former des sphéroïdes tridimensionnels compacts — modèle expérimental de la croissance tumorale et de la cohésion. La répression conjointe du facteur H et de la protéine de capping n’aggravait pas les défauts, suggérant qu’ils agissent dans la même voie. Ces changements se produisaient même lorsque p53 était bloqué, indiquant que le facteur H soutient indépendamment à la fois la division cellulaire et les modifications structurelles qui peuvent favoriser l’invasion et les métastases.
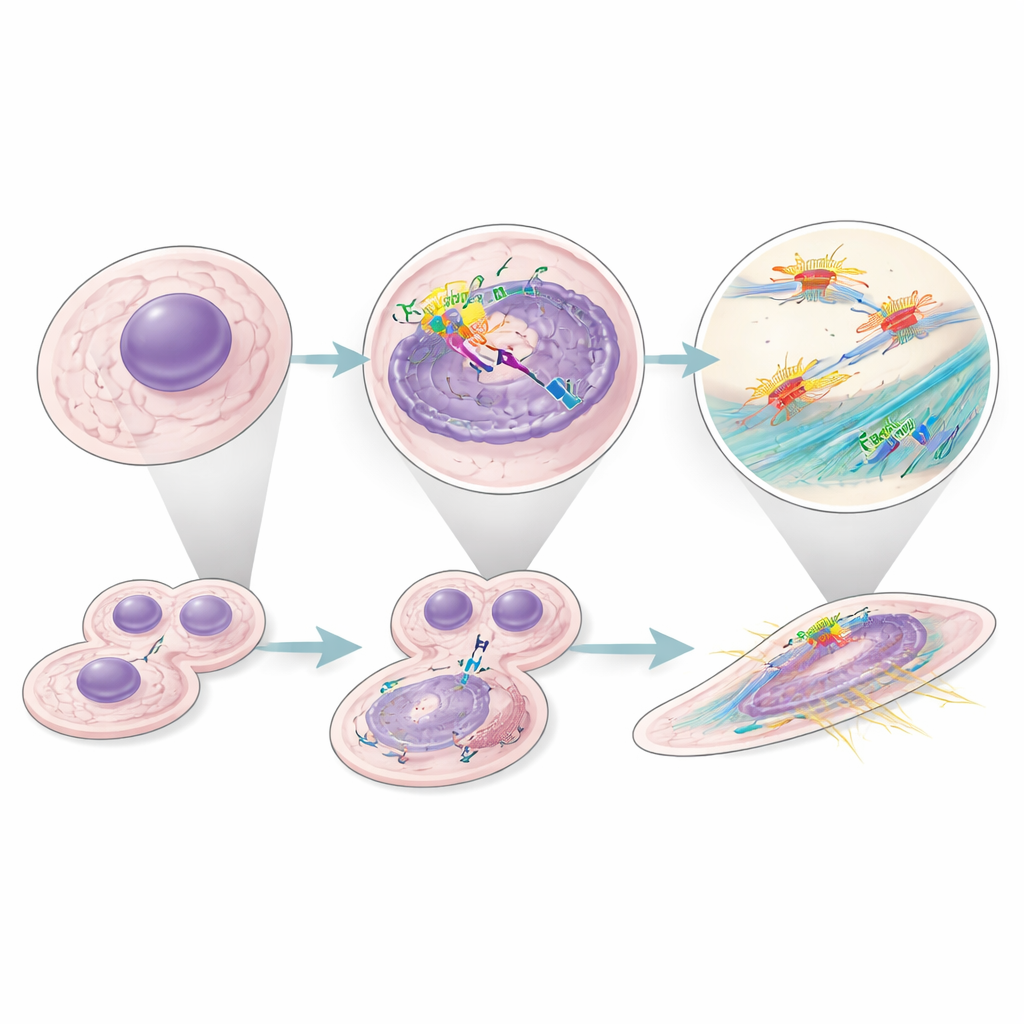
Un impact plus large dans de nombreux cancers
Pour vérifier si ce comportement était spécifique aux tumeurs rénales, les auteurs ont exploité de nombreux jeux de données RNA unicellulaires et en masse issus de cancers humains. Dans les tumeurs où une expression élevée du facteur H prédisait une survie réduite, les signatures de fibroblastes étaient également associées à de moins bons résultats. Au sein des tumeurs rénales, ils ont identifié un état cellulaire malin spécifique exprimant fortement le facteur H, présentant des programmes de cycle cellulaire actifs et étant lié à une survie patient plus courte. Ensemble, ces résultats suggèrent que le facteur H intracellulaire agit comme un agent pro‑tumoral large, opérant à l’intérieur à la fois des cellules cancéreuses et de leurs fibroblastes de soutien dans plusieurs types de cancer.
Ce que cela signifie pour les patients et les traitements
Ce travail remet en cause l’idée selon laquelle le facteur H ne serait qu’un régulateur circulant des réactions immunitaires. Il apparaît plutôt comme un auxiliaire multitâche intracellulaire qui encourage la croissance tumorale en facilitant le passage des cellules par le cycle de division et en ajustant leur ossature interne pour le mouvement. Cela aide à expliquer pourquoi la surexpression du facteur H constitue un signal d’alerte si fort en oncologie. Cela signifie aussi que des médicaments conçus pour bloquer le facteur H à la surface tumorale ou dans le sang risquent de ne pas neutraliser totalement ses fonctions cachées et internes. Les thérapies futures devront probablement cibler à la fois ses rôles externes et internes pour ralentir efficacement la progression tumorale.
Citation: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Mots-clés: facteur H du complément, carcinome rénal à cellules claires, fibroblastes associés au cancer, microenvironnement tumoral, régulation du cycle cellulaire