Clear Sky Science · it
Il fattore H del complemento intracellulare promuove la progressione tumorale attraverso la modulazione del ciclo cellulare e del citoscheletro di actina
Perché questo aiutante nascosto del cancro conta
Il cancro viene spesso descritto come una battaglia tra tumori in crescita e il sistema immunitario. Questo studio rivela che una delle molecole del sistema immunitario, una proteina chiamata fattore H, può silenziosamente cambiare schieramento. Invece di agire solo nel flusso sanguigno per controllare l’infiammazione, il fattore H è presente all’interno delle cellule tumorali e delle cellule di supporto vicine, dove favorisce la crescita, la sopravvivenza e la possibile diffusione dei tumori. Comprendere questa inaspettata “doppia vita” apre nuove possibilità per prevedere l’aggressività di un tumore e progettare terapie più intelligenti.
Una proteina nota in un luogo inaspettato
Il fattore H è meglio conosciuto come guardiano del sistema del complemento, una parte dell’immunità innata che aiuta a rimuovere microbi e cellule danneggiate dal sangue. Livelli elevati di fattore H intorno ai tumori erano già stati associati a esiti peggiori in diversi tumori, incluso il carcinoma renale a cellule chiare. Tuttavia il suo ruolo standard, legato al sangue, non spiegava pienamente perché i pazienti i cui tumori sovraproducono fattore H tendono ad avere una prognosi sfavorevole. Combinando dati di pazienti, sequenziamento a singola cellula e biologia cellulare, gli autori mostrano che molte cellule all’interno dei tumori renali—soprattutto i fibroblasti associati al cancro e le cellule renali maligne—producono attivamente il proprio fattore H e trattengono una parte di esso all’interno della cellula invece di secreterla.
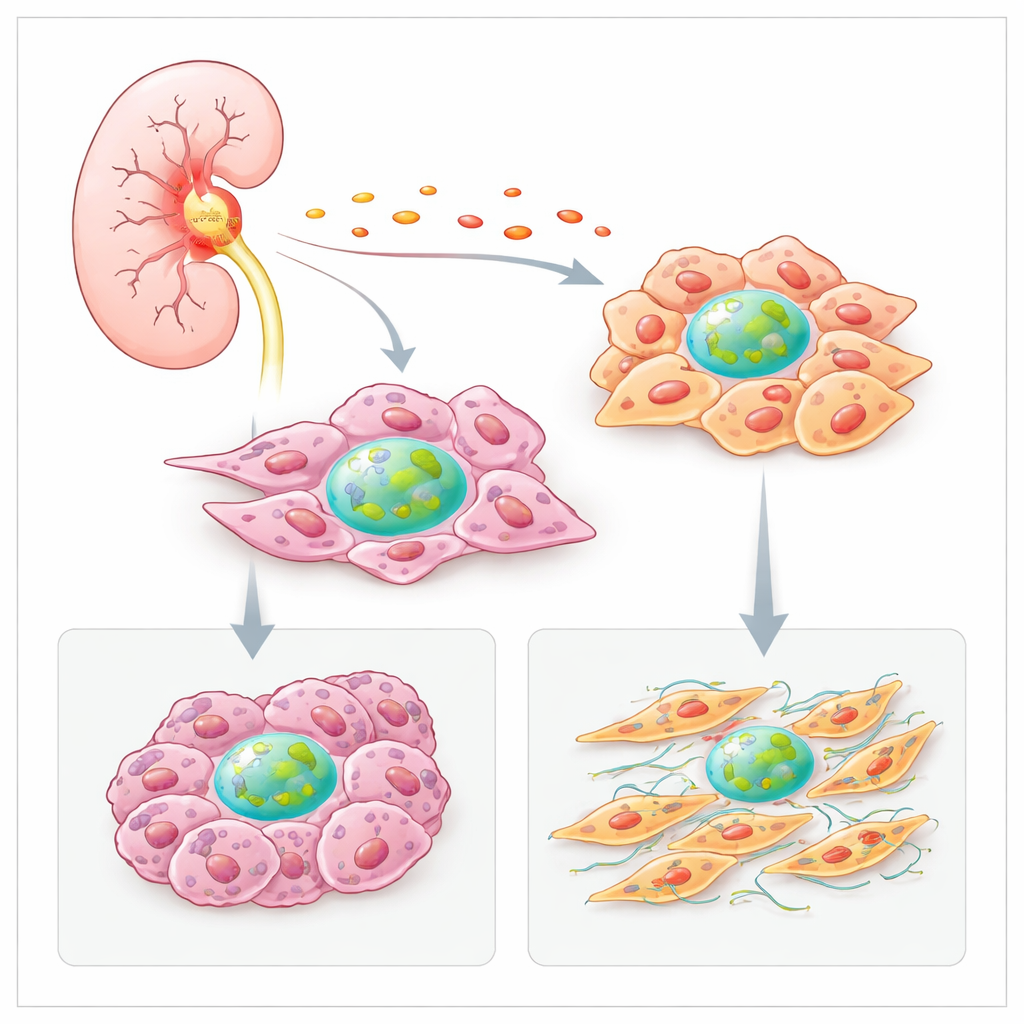
L’infiammazione aumenta la produzione di fattore H
Il gruppo si è prima chiesto perché i tumori producono più fattore H rispetto al tessuto renale sano. Hanno analizzato grandi dataset di cancro e mappe spaziali di sezioni tumorali e hanno trovato che aree ricche di fibroblasti e cellule tumorali contenevano anche alti livelli del gene del fattore H. Queste zone calde spesso coincidevano con firme di molecole infiammatorie, come la citochina IL‑6. In colture di cellule di carcinoma renale, l’IL‑6 aumentava fortemente la produzione di fattore H, mentre altri segnali infiammatori la incrementavano nei fibroblasti. Ciò suggerisce che l’ambiente tumorale infiammato spinge le cellule locali ad alzare la produzione di fattore H, rafforzando un circolo vizioso di crescita e sopravvivenza.
Nel nucleo, aiutando le cellule a ignorare i segnali di stop
Osservando all’interno delle cellule, i ricercatori hanno scoperto una forma più piccola e intracellulare del fattore H che appare in diversi compartimenti, incluso il nucleo. Lì interagisce fisicamente con controllori chiave del ciclo cellulare, in particolare con un fattore di trascrizione chiamato E2F3 che favorisce il passaggio delle cellule dallo stato di riposo alla divisione. Quando il gene del fattore H è stato silenziato, fibroblasti e cellule tumorali rallentavano la replicazione, si accumulavano nella fase di riposo e mostravano un’attività aumentata di p53, una nota proteina “guardiana” che può arrestare la crescita o innescare la morte cellulare. È importante notare che l’aggiunta dall’esterno di fattore H secreto normalmente non compensava questo effetto, sottolineando che è il pool interno a tenere sotto controllo p53 e permettere la proliferazione continua.
Rimodellare lo scheletro cellulare per crescita e movimento
Nelle cellule di carcinoma renale, ma non nei fibroblasti, il fattore H intracellulare si legava anche a componenti del complesso che capisce i filamenti di actina, che regola come i filamenti di actina crescono e stabilizzano l’impalcatura interna della cellula. Quando il fattore H veniva silenziato, le cellule tumorali diventavano più rotonde, perdevano le fibre di tensione organizzate e faticavano a formare sferoidi tridimensionali compatti—un modello sperimentale della crescita e della coesione tumorale. Il silenziamento sia del fattore H sia della proteina capping non peggiorava i difetti, suggerendo che agiscono nella stessa via. Questi cambiamenti si verificavano anche quando p53 era bloccata, indicando che il fattore H sostiene in modo indipendente sia la divisione cellulare sia le modifiche strutturali che possono favorire invasione e metastasi.
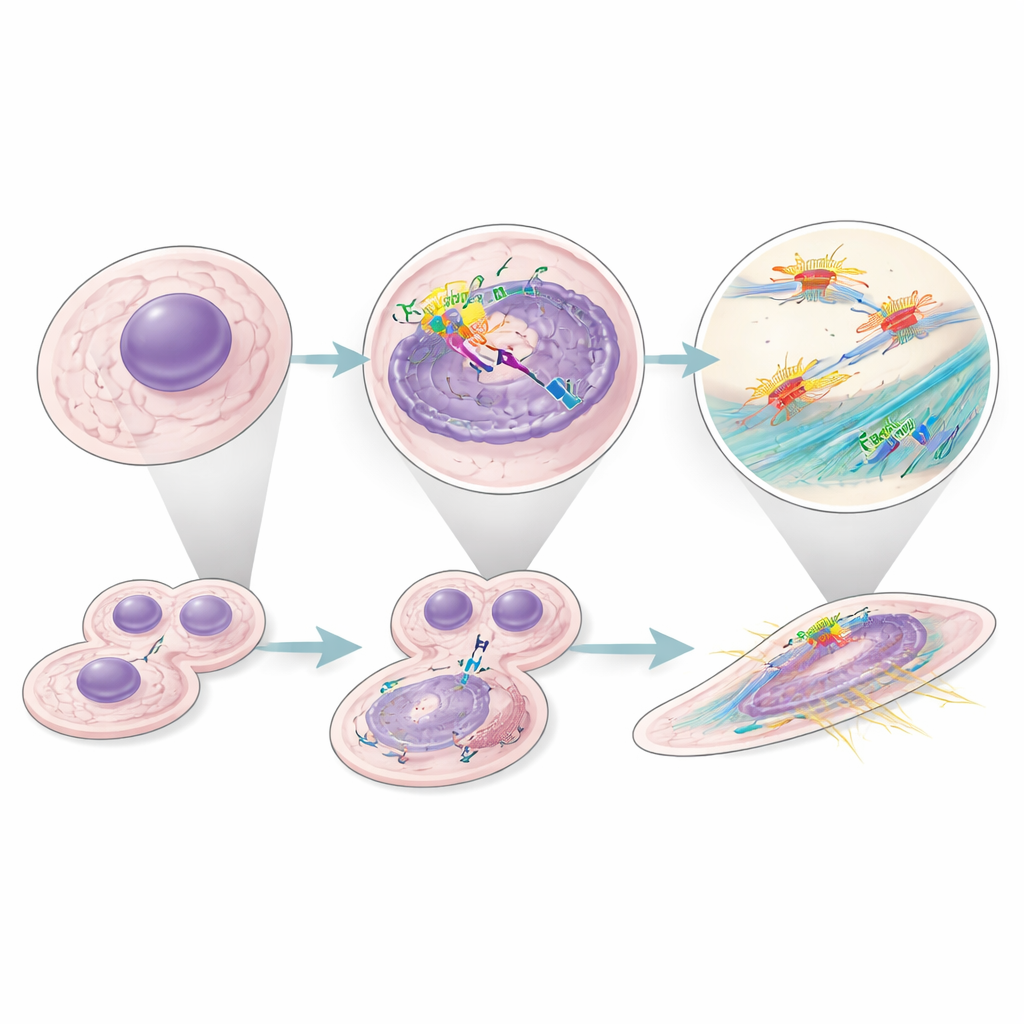
Un impatto più ampio in molti tumori
Per verificare se questo comportamento fosse unico dei tumori renali, gli autori hanno esplorato numerosi dataset di RNA a singola cellula e bulk provenienti da tumori umani. Nei tumori in cui un’alta espressione di fattore H prediceva una sopravvivenza peggiore, anche le firme dei fibroblasti erano collegate a esiti sfavorevoli. Nei tumori renali hanno identificato uno stato cellulare maligno specifico che esprimeva fortemente il fattore H, mostrava programmi attivi del ciclo cellulare ed era associato a una sopravvivenza più breve dei pazienti. Nel complesso, questi risultati suggeriscono che il fattore H intracellulare agisce come un ampio agente pro‑tumorale, operando sia all’interno delle cellule cancerose sia nei fibroblasti di supporto in diversi tipi di cancro.
Cosa significa per i pazienti e le terapie
Questo lavoro rovescia l’idea che il fattore H sia solo un regolatore circolante delle reazioni immunitarie. Al contrario, emerge come un aiutante multitasking intracellulare che incoraggia i tumori a crescere facilitando il passaggio delle cellule attraverso il ciclo di divisione e perfezionando la loro impalcatura interna per il movimento. Questo aiuta a spiegare perché la sovraespressione del fattore H è un segnale così potente nei tumori. Significa anche che farmaci progettati per bloccare il fattore H sulla superficie tumorale o nel sangue potrebbero non disattivare completamente le sue funzioni nascoste e intracellulari. Le terapie future probabilmente dovranno colpire entrambe le sue funzioni, esterne e interne, per rallentare efficacemente la progressione tumorale.
Citazione: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Parole chiave: fattore H del complemento, carcinoma renale a cellule chiare, fibroblasti associati al cancro, microambiente tumorale, regolazione del ciclo cellulare