Clear Sky Science · es
El factor H del complemento intracelular promueve la progresión tumoral mediante la modulación del ciclo celular y el citoesqueleto de actina
Por qué importa este aliado oculto del cáncer
El cáncer se describe a menudo como una batalla entre los tumores en crecimiento y el sistema inmune. Este estudio revela que una de las propias moléculas del sistema inmune, una proteína llamada Factor H, puede cambiar silenciosamente de bando. En lugar de limitarse a actuar en el torrente sanguíneo para controlar la inflamación, el Factor H se encuentra dentro de las células tumorales y en las células de soporte vecinas, donde ayuda a los cánceres a crecer, sobrevivir y potencialmente diseminarse. Comprender esta inesperada “doble vida” abre nuevas vías para predecir la agresividad tumoral y diseñar terapias más inteligentes.
Una proteína conocida en un lugar inesperado
El Factor H es más conocido como guardián del sistema del complemento, una parte de la inmunidad innata que ayuda a eliminar microbios y células dañadas en la sangre. Ya se había relacionado niveles elevados de Factor H alrededor de los tumores con peores pronósticos en varios cánceres, incluido el cáncer renal de células claras. Sin embargo, su papel habitual en la sangre no explicaba completamente por qué los pacientes cuyos tumores sobreproducen Factor H tienden a tener malos resultados. Combinando datos de pacientes, secuenciación de una sola célula y biología celular, los autores muestran que muchas células dentro de los tumores renales —especialmente los fibroblastos asociados al cáncer y las células renales malignas— producen activamente su propio Factor H y retienen una porción dentro de la célula en lugar de secretarla.
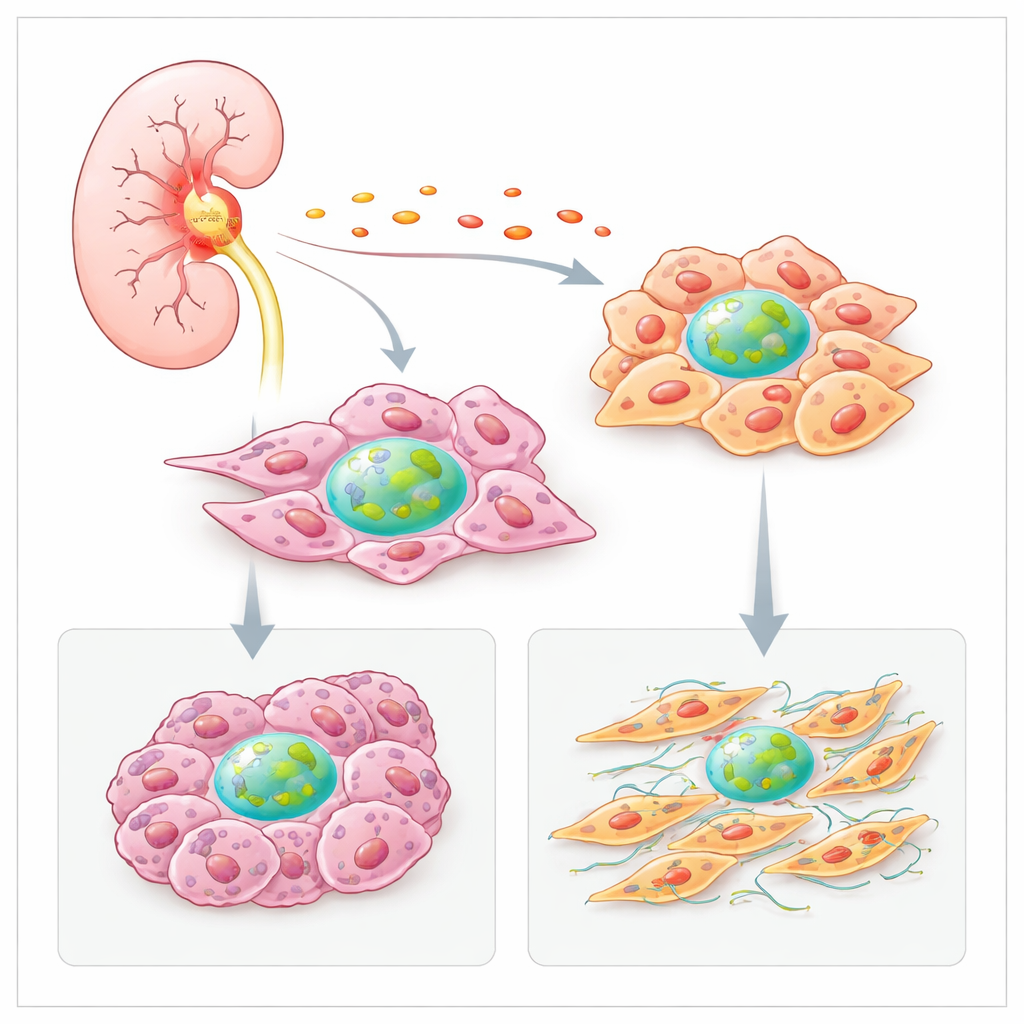
La inflamación incrementa la producción de Factor H
El equipo preguntó primero por qué los tumores producen más Factor H que el tejido renal sano. Analizaron grandes conjuntos de datos de cáncer y mapas espaciales de cortes tumorales y encontraron que las zonas ricas en fibroblastos y células cancerosas también contenían altos niveles del gen de Factor H. Estas áreas calientes coincidían frecuentemente con firmas de moléculas inflamatorias, como la citocina IL‑6. En cultivos de células de cáncer renal, la IL‑6 potenció fuertemente la producción de Factor H, mientras que otras señales inflamatorias la aumentaron en fibroblastos. Esto sugiere que el entorno tumoral inflamado empuja a las células locales a aumentar su propio Factor H, reforzando un círculo vicioso de crecimiento y supervivencia.
Dentro del núcleo, ayudando a las células a ignorar señales de parada
Al mirar dentro de las células, los investigadores descubrieron una forma más pequeña de Factor H intracelular que aparece en varios compartimentos, incluido el núcleo. Allí interactúa físicamente con controladores clave del ciclo celular, en particular con un factor de transcripción llamado E2F3 que ayuda a impulsar a las células de un estado de reposo a la división. Cuando se silenció el gen de Factor H, los fibroblastos y las células cancerosas ralentizaron su replicación, se acumularon en la fase de reposo y mostraron una mayor actividad de p53, una conocida proteína “guardiana” que puede frenar el crecimiento o desencadenar la muerte celular. Es importante que simplemente añadir Factor H normal y secretado desde el exterior no rescató este efecto, lo que subraya que el reservorio interno es el que mantiene a p53 bajo control y permite la proliferación continua.
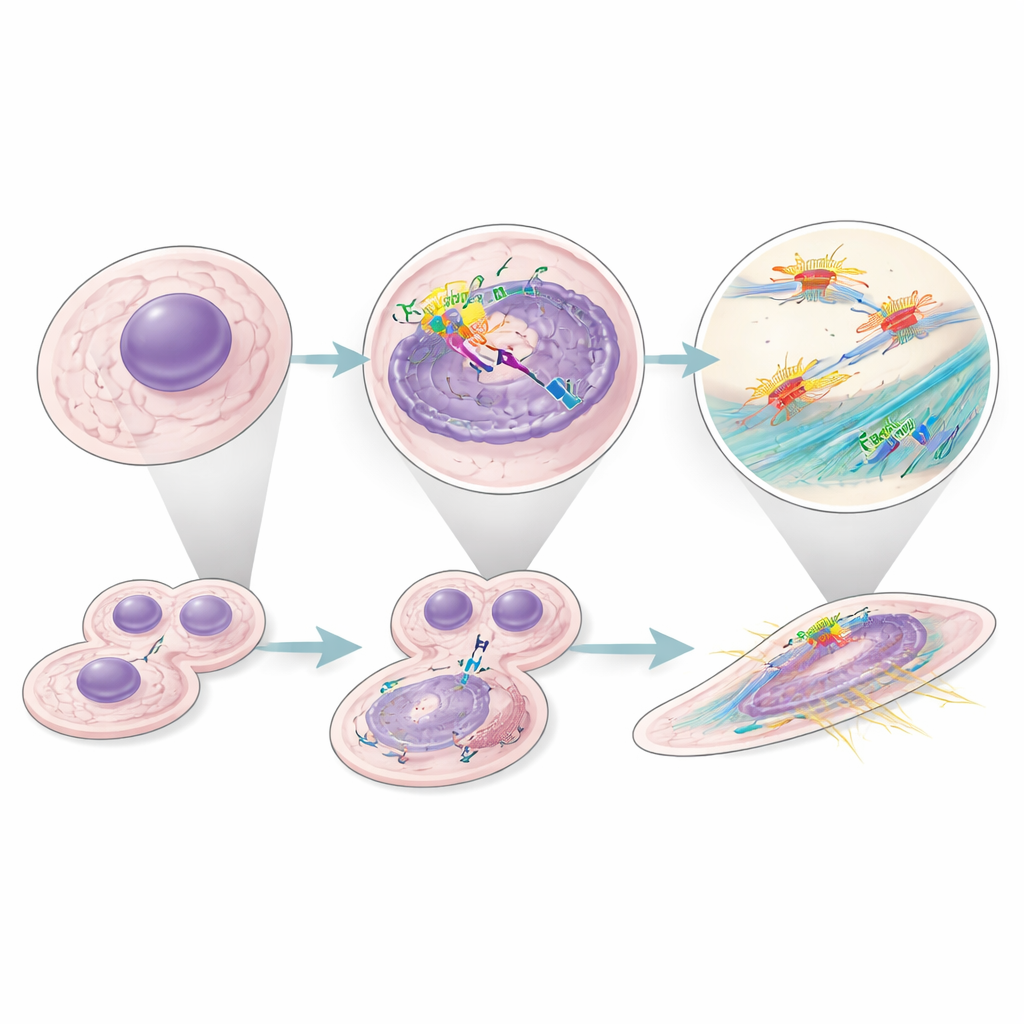
Reconfigurando el esqueleto celular para crecimiento y movimiento
En las células de cáncer renal, pero no en los fibroblastos, el Factor H intracelular también se unió a componentes del complejo caperuzo de la actina, que regula cómo crecen los filamentos de actina y estabilizan el andamiaje interno de la célula. Al silenciar Factor H, las células cancerosas se volvieron más redondeadas, perdieron sus fibras de tensión organizadas y tuvieron dificultades para formar esferoides tridimensionales compactos —un sustituto experimental del crecimiento y la cohesión tumoral. Silenciar tanto Factor H como la proteína caperuza no empeoró los defectos, lo que sugiere que actúan en la misma vía. Estos cambios ocurrieron incluso cuando se bloqueó p53, indicando que Factor H sostiene de forma independiente tanto la división celular como los cambios estructurales que pueden favorecer la invasión y la metástasis.
Un impacto más amplio en muchos cánceres
Para ver si este comportamiento era exclusivo de los tumores renales, los autores analizaron numerosos conjuntos de datos de ARN de una sola célula y de conjunto de diversos cánceres humanos. En tumores donde la alta expresión de Factor H predijo una peor supervivencia, las firmas de fibroblastos también se asociaron con peores resultados. Dentro de los tumores renales, identificaron un estado celular maligno específico que expresaba fuertemente Factor H, mostraba programas activos del ciclo celular y se asociaba con una supervivencia más corta de los pacientes. En conjunto, estos hallazgos sugieren que el Factor H intracelular actúa como un agente pró-tumoral amplio, operando dentro de las células cancerosas y de sus fibroblastos de apoyo en múltiples tipos de cáncer.
Qué significa esto para pacientes y terapias
Este trabajo derriba la idea de que el Factor H es solo un regulador circulante de las reacciones inmunes. En cambio, surge como un ayudante multitarea intracelular que fomenta el crecimiento tumoral al facilitar que las células atraviesen el ciclo de división y al ajustar su andamiaje interno para el movimiento. Esto ayuda a explicar por qué la sobreexpresión de Factor H es una señal de alarma tan potente en el cáncer. También implica que los fármacos diseñados para bloquear Factor H en la superficie tumoral o en la sangre pueden no desactivar por completo sus funciones internas ocultas. Las terapias futuras probablemente deberán dirigirse a sus roles externos e internos para ralentizar eficazmente la progresión tumoral.
Cita: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Palabras clave: factor H del complemento, carcinoma de células claras de riñón, fibroblastos asociados al cáncer, microambiente tumoral, regulación del ciclo celular