Clear Sky Science · pl
Wewnętrzny czynnik dopełniacza H promuje rozwój nowotworu poprzez modulację cyklu komórkowego i cytoszkieletu aktynowego
Dlaczego ten ukryty sprzymierzeniec nowotworu ma znaczenie
Nowotwór często opisuje się jako walkę między rosnącymi guzami a układem odpornościowym. Badanie to ujawnia, że jedna z własnych cząsteczek układu odpornościowego, białko zwane czynnikiem H, może potajemnie zmieniać strony. Zamiast działać wyłącznie we krwi w celu kontrolowania zapalenia, czynnik H występuje wewnątrz komórek nowotworowych i pobliskich komórek wspierających, gdzie pomaga nowotworom rosnąć, przetrwać i potencjalnie się rozprzestrzeniać. Zrozumienie tej nieoczekiwanej „podwójnej roli” otwiera nowe możliwości przewidywania, jak agresywny będzie guz, oraz projektowania mądrzejszych terapii.
Znane białko w nieoczekiwanym miejscu
Czynnik H jest najlepiej znany jako strażnik systemu dopełniacza, części odporności wrodzonej, która pomaga usuwać drobnoustroje i uszkodzone komórki z krwi. Wysokie poziomy czynnika H wokół guzów już wcześniej wiązano z gorszymi wynikami w kilku nowotworach, w tym w jasnokomórkowym raku nerki. Jednak jego standardowa, krążąca rola nie tłumaczyła w pełni, dlaczego pacjenci, których guzy nadprodukują czynnik H, częściej mają gorsze rokowania. Łącząc dane pacjentów, sekwencjonowanie pojedynczych komórek i biologię komórki, autorzy pokazują, że wiele komórek w nerwowych guzach—szczególnie fibroblasty związane z rakiem i złośliwe komórki nerkowe—aktywnie wytwarza własny czynnik H i zatrzymuje jego część wewnątrz komórki zamiast wydzielać ją na zewnątrz.
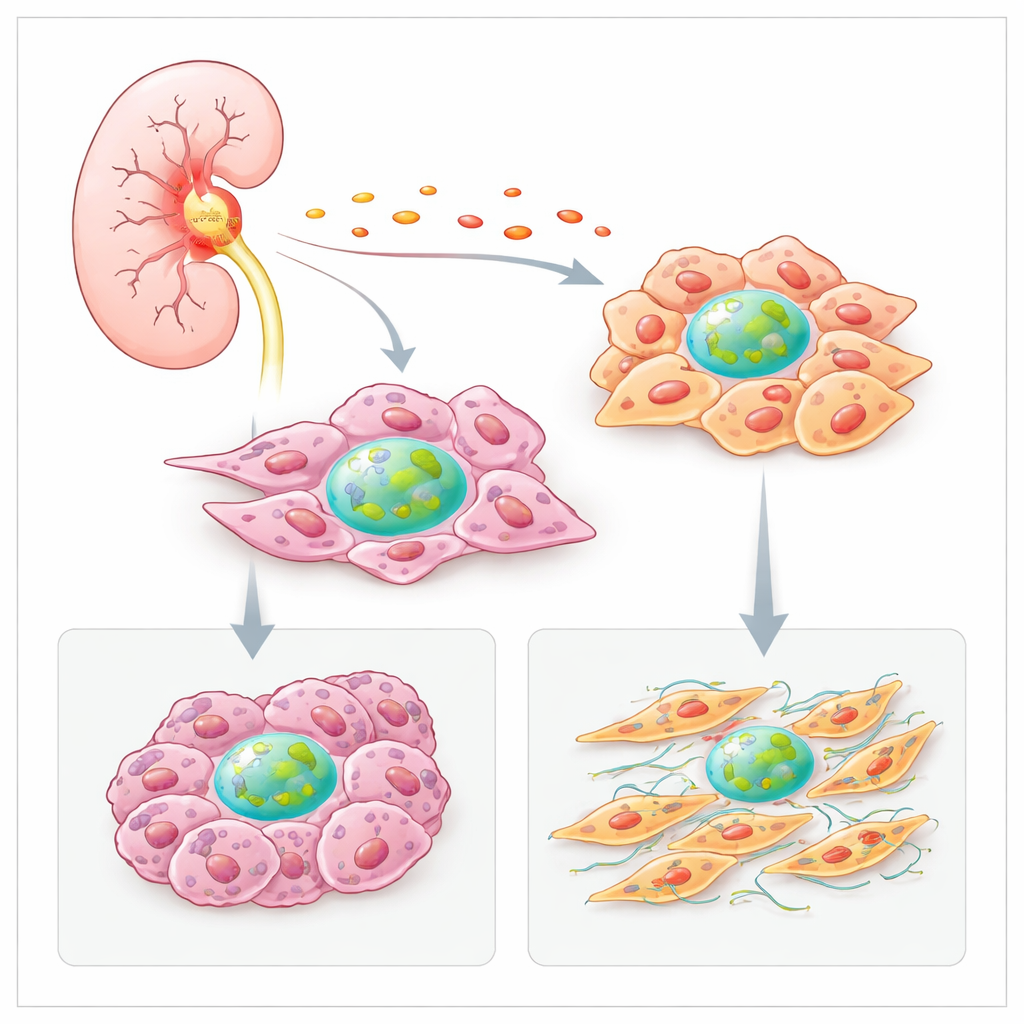
Zapalenie podkręca produkcję czynnika H
Zespół najpierw zapytał, dlaczego guzy produkują więcej czynnika H niż zdrowa tkanka nerkowa. Przeanalizowali obszerne zbiory danych nowotworowych i przestrzenne mapy przekrojów guzów i odkryli, że obszary bogate w fibroblasty i komórki nowotworowe także zawierały wysokie poziomy genu czynnika H. Te „gorące” miejsca często pokrywały się ze śladami cząsteczek zapalnych, takich jak cytokinina IL‑6. W hodowlach komórkowych raka nerkowego IL‑6 silnie zwiększał produkcję czynnika H, podczas gdy inne sygnały zapalne podnosiły ją w fibroblastach. Sugeruje to, że zapalne mikrośrodowisko guza samo w sobie nakłania lokalne komórki do zwiększenia produkcji własnego czynnika H, wzmacniając błędne koło wzrostu i przetrwania.
W jądrze — pomagając komórkom ignorować sygnały zatrzymania
Patrząc wewnątrz komórek, badacze odkryli mniejszą, wewnątrzkomórkową formę czynnika H, która pojawia się w kilku przedziałach, w tym w jądrze komórkowym. Tam fizycznie oddziałuje z kluczowymi regulatorami cyklu komórkowego, szczególnie z czynnikiem transkrypcyjnym E2F3, który pomaga przesuwać komórki ze stanu spoczynku w stan podziału. Gdy gen czynnika H został wyciszony, fibroblasty i komórki nowotworowe spowolniły replikację, gromadziły się w fazie spoczynkowej i wykazywały większą aktywność p53 — dobrze znanego „strażnika”, który może zatrzymać wzrost lub wywołać śmierć komórki. Co ważne, samo dodanie normalnego, wydzielanego czynnika H z zewnątrz nie naprawiło tego efektu, podkreślając, że to wewnętrzna pula odpowiada za powstrzymywanie p53 i umożliwienie ciągłej proliferacji.
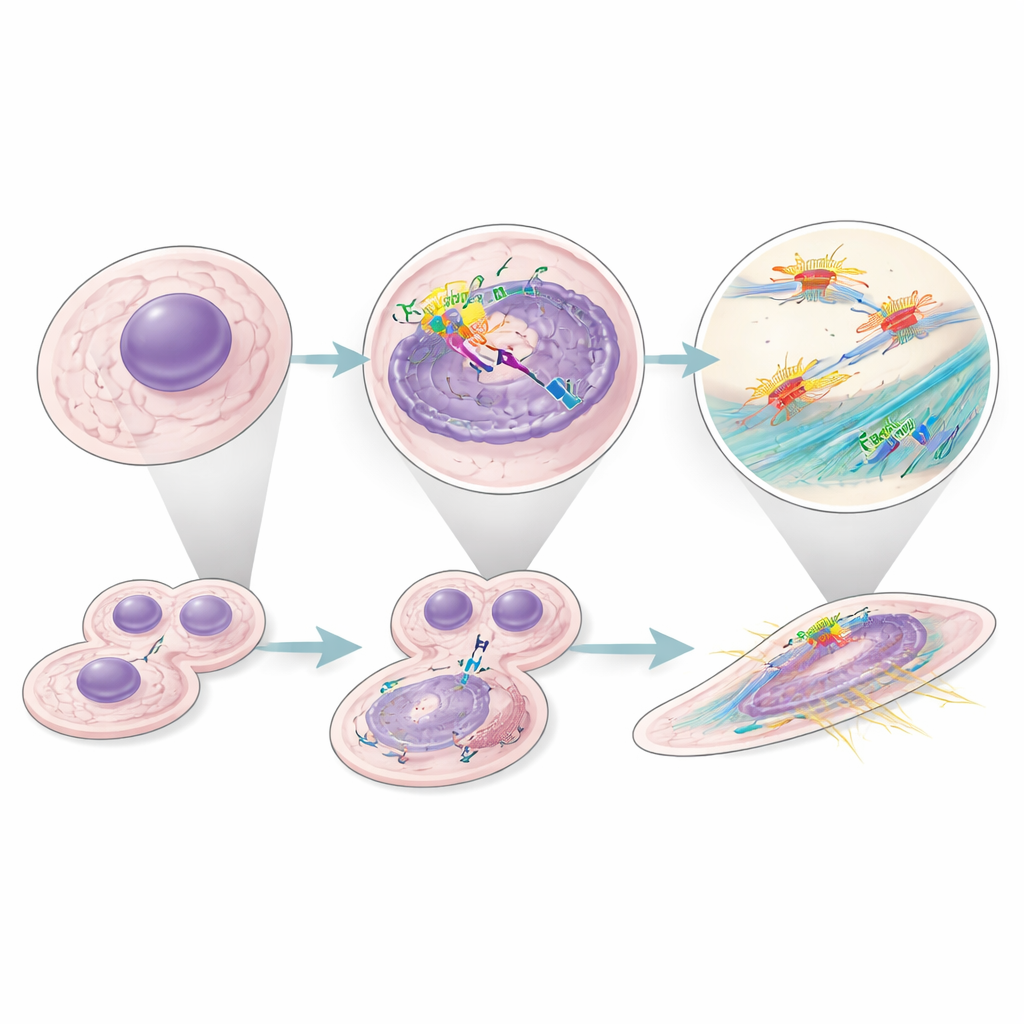
Przekształcanie cytoszkieletu komórkowego dla wzrostu i ruchu
W komórkach raka nerki, ale nie w fibroblastach, wewnątrzkomórkowy czynnik H wiązał również składniki kompleksu ograniczającego aktynę (actin capping complex), który reguluje wzrost włókien aktynowych i stabilizację wewnętrznego rusztowania komórki. Gdy czynnik H był wyciszony, komórki nowotworowe stawały się bardziej zaokrąglone, traciły zorganizowane włókna stresowe i miały trudności z tworzeniem zwartej, trójwymiarowej sferoidy — eksperymentalnego odpowiednika wzrostu guza i jego spójności. Wyciszenie zarówno czynnika H, jak i białka ograniczającego nie pogorszyło defektów, co sugeruje, że działają w tej samej ścieżce. Zmiany te występowały nawet przy blokadzie p53, wskazując, że czynnik H niezależnie wspiera zarówno podział komórek, jak i zmiany strukturalne sprzyjające inwazji i przerzutom.
Szeroki wpływ w różnych nowotworach
Aby sprawdzić, czy to zachowanie jest wyjątkowe dla guzów nerkowych, autorzy przeanalizowali liczne dane RNA z pojedynczych komórek i masowe profile z nowotworów ludzkich. W nowotworach, gdzie wysoka ekspresja czynnika H przewidywała gorsze przeżycie, sygnatury fibroblastów również wiązały się ze słabszymi wynikami. W obrębie guzów nerkowych zidentyfikowali specyficzny stan złośliwych komórek silnie eksprymujących czynnik H, wykazujących aktywne programy cyklu komórkowego i związanych z krótszym przeżyciem pacjentów. Razem te odkrycia sugerują, że wewnątrzkomórkowy czynnik H działa jako szeroko działający promotor nowotworu, funkcjonując wewnątrz zarówno komórek nowotworowych, jak i ich wspierających fibroblastów w różnych typach raka.
Co to znaczy dla pacjentów i terapii
Praca ta obala pogląd, że czynnik H jest tylko krążącym regulatorem reakcji immunologicznych. Zamiast tego wyłania się jako wielozadaniowy, wewnątrzkomórkowy pomocnik, który sprzyja wzrostowi guzów, ułatwiając komórkom przechodzenie przez cykl podziału i dopracowując ich wewnętrzne rusztowanie pod kątem ruchu. Pomaga to wyjaśnić, dlaczego nadekspresja czynnika H jest tak silnym znakiem ostrzegawczym w nowotworach. Oznacza to również, że leki zaprojektowane do blokowania czynnika H na powierzchni guza lub we krwi mogą nie wyłączyć jego ukrytych, wewnętrznych funkcji. Przyszłe terapie prawdopodobnie będą musiały celować zarówno w role zewnętrzne, jak i wewnętrzne, aby skutecznie spowolnić rozwój guza.
Cytowanie: Rezola Artero, M., Minery, A., Revel, M. et al. Intracellular complement Factor H promotes tumor progression through modulation of cell cycle and actin cytoskeleton. Commun Biol 9, 524 (2026). https://doi.org/10.1038/s42003-026-09807-4
Słowa kluczowe: czynnik dopełniacza H, rak jasnokomórkowy nerki, fibroblasty związane z rakiem, mikrośrodowisko guza, regulacja cyklu komórkowego